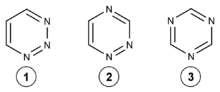
- Triazina
-
Las triazinas son una familia de tres compuestos orgánicos, isómeros entre sí, cuya fórmula empírica es C3H3N3.
Contenido
Estructura
La estructura de la triazina es la de un anillo heterocíclico, análogo al anillo de benceno pero con tres átomos de carbono reemplazados por átomos de nitrógeno. Los tres isómeros de la triazina se distinguen entre sí por la posición de sus átomos de nitrógeno, y reciben el nombre de 1,2,3-triazina, 1,2,4-triazina y 1,3,5-triazina. Otros anillos heterocíclicos aromáticos con nitrógeno son la piridina (con un átomo de nitrógeno), las diazinas (con dos átomos de nitrógeno) y las tetrazinas (que tienen cuatro). Las triazinas son bases más débiles que la piridina.
Usos
El derivado más conocido de la 1,3,5-triazina es la melamina, que tiene tres sustituyentes amino y se emplea en la elaboración de resinas. Otro derivado utilizado con el mismo propósito es la benzoguanamina. También se emplean derivados de la triazina como base para fabricar herbicidas como el cloruro cianúrico (2,4,6-tricloro-1,3,5-triazina). Las triazinas con cloro como sustituyente también se emplean como colorantes reactivos.
Una serie de derivados de la 1,2,4-triazina conocidos como BTP han sido considerados para la extracción líquido-líquido.[1] [2] [3] [4] [5]
Síntesis
- La 1,2,3-triazina se puede sintetizar mediante el reagrupamiento térmico de 2-azidociclopropeno.
- La 1,2,4-triazina se puede elaborar por condensación de compuestos 1,2-dicarbonílicos con amidrazonas. Una síntesis clásica es la síntesis de triazina de Bamberger.
- La 1,3,5-triazina (simétrica) se produce por trimerización de cloruro de cianógeno o cianimida.
Reacciones
Aunque las triazinas son compuestos aromáticos, la energía de resonancia es mucho menor que la del benceno. La sustitución aromática electrófila es difícil, pero la sustitución aromática nucleófila es más frecuente.
La 2,4,6-tricloro-1,3,5-triazina se hidroliza en ácido cianúrico calentándola con agua a temperaturas elevadas. La 2,4,6-tris(fenoxi)-1,3,5-triazina reacciona con las aminas alifáticas en la aminólisis, y de esta reacción se pueden obtener dendrímeros.[6] La pirólisis de la melamina mediante la expulsión de amoníaco produce heptazina (o tri-s-triazina).[7] El cloruro cianúrico se emplea en la amidación de los ácidos carboxílicos[8]
Referencias
- ↑ http://www.nea.fr/html/pt/docs/iem/madrid00/Proceedings/Paper14.pdf
- ↑ http://www-atalante2004.cea.fr/home/liblocal/docs/atalante2000/P3-26.pdf
- ↑ Development Of Electrochemical Separations Of Uranium And Re Elements From Fluoride Melts
- ↑ http://www.rsc.org/delivery/_ArticleLinking/DisplayArticleForFree.cfm?doi=b301178j&JournalCode=DT
- ↑ http://www.tntech.edu/WRC/pdfs/Projects04_05/Ens_Elem.pdf
- ↑ Christian Dreyer, Alfred Blume, Monika Bauer, Jörg Bauer, Jens Neumann-Rodekirch Fourth International Electronic Conference on Synthetic Organic Chemistry (ECSOC-4), September 1-30, 2000 Article
- ↑ Barbara Jürgens, Elisabeth Irran, Jürgen Senker, Peter Kroll, Helen Müller, and Wolfgang Schnick J. Am. Chem. Soc., 125 (34), 10288 -10300, 2003. Abstract
- ↑ Triazine-Promoted Amidation of Various Carboxylic Acids Jeremy Schlarb 1999 Article
- Heterocyclic Chemistry T.L. Gilchrist 1985 ISBN 0-582-01421-2 (1997, ISBN 0-582-27843-0)
Véase también
Categorías:- Azinas
- Químicos explosivos
Wikimedia foundation. 2010.