- N-acetilserotonina
-
N-acetilserotonina
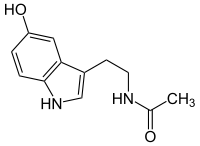
Nombre (IUPAC) sistemático N-[2-(5-hidroxi-1H-indol-3-il)etil]acetamida General Otros nombres N-acetil-5-hidroxitriptamina, N-acetil-5-HT, normelatonina Fórmula molecular C12H14N2O2 Identificadores Número CAS 1210-83-9 PubChem Propiedades físicas Masa molar 218.252 g/mol Punto de fusión 394 K (120,85 °C) Propiedades químicas Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referencias
N-Acetilserotonina (NAS), también llamado normelatonina, es un compuesto químico intermediario de la ruta de síntesis de melatonina a partir de serotonina.[1] [2] Se produce a partir de la serotonina por la enzima serotonina N-acetiltransferasa (AANAT) y que se convierte en melatonina por la Acetilserotonina O-metiltransferasa (ASMT).Como la melatonina, NAS es un agonista de los receptores de melatonina neurotransmisor.[3] [4] [5] [6] Además, NAS se distribuye en algunas áreas de l cerebro donde la serotonina y la melatonina no aparecen, sugiriendo otras nuevas funciones en el sistema nervioso central además de ser meramente el precursor de la síntesis de melatonina.[3]
Recientemente, se ha demostrado que NAS actúa como un potente agonista del receptor TrkB, mientras que la serotonina y la melatonina no tienen ningún efecto.[3] Produce potentes efectos antidepresivos, neuroprotectores, y neurotróficos mediandos por TrkB.[3] Además, el ratón knockout de la AANAT, que no tienen niveles apreciables de NAS, muestra un tiempo de inmovilidad significativamente mayor que los ratones controles en ensayos etológicos para la depresión como el test de natación forzada.[3]
La NAS juega un importante papel en los efectos antidepresivos de los inhibidores de la recaptación de serotonina e inhibidores de la monoaminooxidasa (IMAO).[3] La fluoxetina y la clorgilina regulan al alza la actividad AANAT indirectamente a través de mecanismos serotoninérgicos que permiten aumentar los niveles de NAS levels tras su administración crónica, y se correlaciona con la aparición de los efectos antidepresivos de estos fármacos.[3] [7] Por último, la exposición a la luz inhibe la síntesis de NAS y reduce los efectos antidepresivos de los inhibidores de la MAO.[3] Estos datos apoyan el papel de la NAS en la regulación del estado de ánimo y los beneficios terapéuticos provocados por los antidepresivos.
Además, a través de un mecanismo no identificado en la actualidad, la NAS puede ser la causante de la hipotensión ortostática observada durante el tratamiento clínico con inhibidores de la MAO.[8] [7] Reduce la presión sanguínea en roedores y la pinealectomía (la glándula pineal es el pricipal lugar de síntesis de NAS y melatonina) elimina el efecto hipotensor de la clorgilina.[8] [7] Se desconoce la razón de por qué la hipotensión ortostática se observa comúnmente en el tratamiento con inhibidores de la MAO pero no con inhibidores de la recaptación de serotonina, aunque ambos tratamientos aumentan los niveles de NAS.
Véase también
Referencias
- ↑ AXELROD J, WEISSBACH H (April 1960). «Enzymatic O-methylation of N-acetylserotonin to melatonin». Science (New York, N.Y.) 131: pp. 1312. PMID 13795316. http://www.sciencemag.org/cgi/pmidlookup?view=long&pmid=13795316.
- ↑ WEISSBACH H, REDFIELD BG, AXELROD J (September 1960). «Biosynthesis of melatonin: enzymic conversion of serotonin to N-acetylserotonin». Biochimica Et Biophysica Acta 43: pp. 352–3. PMID 13784117.
- ↑ a b c d e f g h Jang SW, Liu X, Pradoldej S, et al. (February 2010). «N-acetylserotonin activates TrkB receptor in a circadian rhythm». Proceedings of the National Academy of Sciences of the United States of America. doi:. PMID 20133677. http://www.pnas.org/cgi/pmidlookup?view=long&pmid=20133677.
- ↑ Zhao H, Poon AM, Pang SF (March 2000). «Pharmacological characterization, molecular subtyping, and autoradiographic localization of putative melatonin receptors in uterine endometrium of estrous rats». Life Sciences 66 (17): pp. 1581–91. PMID 11261588. http://linkinghub.elsevier.com/retrieve/pii/S0024320500004781.
- ↑ Nonno R, Pannacci M, Lucini V, Angeloni D, Fraschini F, Stankov BM (July 1999). «Ligand efficacy and potency at recombinant human MT2 melatonin receptors: evidence for agonist activity of some mt1-antagonists». British Journal of Pharmacology 127 (5): pp. 1288–94. doi:. PMID 10455277. PMC 1566130. http://dx.doi.org/10.1038/sj.bjp.0702658.
- ↑ Paul P, Lahaye C, Delagrange P, Nicolas JP, Canet E, Boutin JA (July 1999). «Characterization of 2-[125Iiodomelatonin binding sites in Syrian hamster peripheral organs]». The Journal of Pharmacology and Experimental Therapeutics 290 (1): pp. 334–40. PMID 10381796. http://jpet.aspetjournals.org/cgi/pmidlookup?view=long&pmid=10381796.
- ↑ a b c Oxenkrug GF (1999). «Antidepressive and antihypertensive effects of MAO-A inhibition: role of N-acetylserotonin. A review». Neurobiology (Budapest, Hungary) 7 (2): pp. 213–24. PMID 10591054.
- ↑ a b Oxenkrug GF (1997). «[N-acetylserotonin and hypotensive effect of MAO-A inhibitors]» (en ruso). Voprosy Medit͡sinskoĭ Khimii 43 (6): pp. 522–6. PMID 9503569.
Categorías:- Triptaminas
- Antioxidantes
- Fenoles
Wikimedia foundation. 2010.
