- Síntesis de indoles de Bischler-Möhlau
-
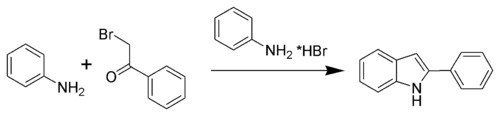
La Síntesis de indoles de Bischler-Möhlau indol es un método de síntesis orgánica en el que se forma un 2-aril-indol a partir de la α-bromo-acetofenona y una anilina en exceso.[1] [2] [3] [4] [5]
A pesar de su larga historia, esta reacción clásica ha recibido relativamente poca atención en comparación con otros métodos para la síntesis de indol, tal vez debido a las condiciones severas de reacción que requiere. Recientemente, métodos más suaves se han desarrollado, incluyendo el uso de bromuro de litio como un catalizador y un procedimiento mejorado que implica el uso de la irradiación de microondas.[6] [7] [8]
Mecanismo de reacción
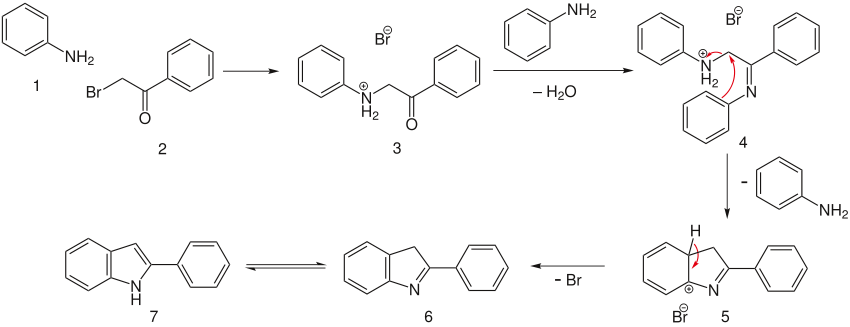
Los dos primeros pasos implican la reacción de la α-bromo-acetofenona con dos moléculas de la anilina (Una por SN2 y la otra para obtener la N-fenilcetimina) para formar el intermediario 4. El catión anilinio forma un grupo saliente para el ataque electrofílico del otro anillo aromático para formar el intermediario 5, que rápidamente se aromatiza y tautomeriza para dar el indol deseado (7).
Referencias
- ↑ Bischler, A. et al.; Ber. 1892, 25, 2860.
- ↑ Bischler, A. et al.; Ber. 1893, 26, 1336.
- ↑ Möhlau, R.; Ber. 1881, 14, 171.
- ↑ Möhlau, R.; Ber. 1882, 15, 2480.
- ↑ Fischer, E.; Schmitt, T. Ber. 1888, 21, 1071.
- ↑ Pchalek, K.; Jones, A. W.; Wekking, M. M. T.; Black, D. S. C. Tetrahedron 2005, 61, 77.
- ↑ Sridharan, V.; Perumal, S.; Avendaño, C.; Menéndez, J. C. Synlett 2006, 91.
- ↑ Vara et al 2008
Véase también
Categoría:- Reacciones químicas orgánicas
Wikimedia foundation. 2010.