- Enantiómero
-
Enantiómero
En la ciencia de la química se dice que dos estereoisómeros son enantiómeros si la imagen especular de uno no puede ser superpuesta con la del otro. Dicho de otra forma: un enantiómero es una imagen especular no superponible de sí mismo. Tienen las mismas propiedades físicas y químicas, excepto por la interacción con el plano de la luz polarizada o con otras moléculas quirales. Son moléculas quirales. La mezcla en cantidades equimolares de cada enantiómero en una solución se denomina mezcla racémica y es ópticamente inactiva.
Contenido
Características
Las moléculas que contienen un estereocentro (carbono asimétrico, centro esterogénico o centro quiral) son siempre ópticamente activas (quirales). Aunque esto no es cierto necesariamente para algunas moléculas con más de un esterocentro. Éste es el caso de las formas meso. Los enantiómeros tienen las mismas propiedades químicas y físicas, a excepción de su respuesta ante la luz polarizada (actividad óptica). Por ello se les denomina isómeros ópticos.
Las moléculas aquirales son ópticamente inactivas.
La rotación específica de la luz polarizada, que se mide por medio de un polarímetro, es una propiedad física característica de la estructura de cada enantiómero, de su concentración y del disolvente empleado en la medición.
La medida de la rotación específica indica la composición enantiomérica del producto.
Enantiómero Imagen: Enantiómero Imagen: Imagen:Imagen11.gif
(-)-2-Bromobutano-23.1º Imagen:Enantiomer.png
(+)-2-Bromobutano+23.1º Imagen:Imagen13.gif Ácido (-)-2-
aminopropanoico
(-)-Alanina-8.5º Imagen:Imagen14.gif Ácido (+)-2-
aminopropanoico
(+)-Alanina+8.5º Imagen:Imagen15.gif Ácido (+)-2-
hidroxipropanoico
Ácido (+)-láctico+3.8º Imagen:Imagen16.gif Ácido (-)-2-
hidroxipropanoico
Ácido (-)-láctico-3.8º Imagen:/Imagen17.gif (+)-Limoneno
+94º Imagen:Imagen18.gif (-)-Limoneno
-94º Representación
Por comodidad los enantiómeros se suelen representar por medio de la proyección de Fisher. Ésta consiste en imaginar que se observa la molécula, de tal manera, que dos de los enlaces están hacia adelante y los otros dos hacia atrás. De esta manera se forma una especie de cruz, con el carbono asimétrico en el centro de ésta, mostrándose como la intersección de las líneas. Los grupos que se encuentren en la línea horizontal están hacia delante, y los verticales en la parte de atrás.
Nomenclatura
Enantiómeros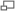
Un enantiómero que rota el plano de la luz polarizada hacia la derecha (en el sentido de las agujas del reloj), se dice que es dextrorrotatorio o dextrógiro, y suele colocársele al nombre de éste una letra de minúscula (d), o un signo positivo (+). Si lo hace hacia la izquierda, es levorrotatorio o levógiro y suele colocársele al nombre una letra ele minúscula (l), o un signo negativo (-).
Una forma no experimental para nombrarlos es la ideada por Prelog-Ingold-Cahn: Consiste en numerar a los grupos o átomos enlazados al carbono asimétrico, de acuerdo a su prioridad (el número 1 al más importante y el 4 al de menor importancia), si según el orden de las manecillas del reloj (sin contar al de menor importancia) este sigue su misma dirección se coloca una ere mayúscula (R), mientras que si es en sentido contrario a las agujas del reloj una ese minúscula (s). En el caso que el grupo o átomo con menor prioridad se encuentre adelante según la proyección de Fisher (en la horizontal), se considera que se está viendo desde atrás de la molécula, por lo que se considera al revés. En otras palabras si según Prelog-Ingold-Cahn, es R se debe considerar como S. En el caso en que exista más de un carbono asimétrico debe colocarse junto a la letra R o S, el número del carbono correspondiente. La Prioridad del átomo es definida en primera instancia por su número atómico o peso atómico en orden creciente (normalmente el de menor prioridad resulta ser un hidrógeno), y en segunda instancia por el número atómico de los átomos a los que esta enlazado, considerando dobles enlaces como si estuviera unido a dos de esos átomos y de manera análoga los triples enlaces como si estuviera unido a tres de esos átomos.
Separación de enantiómeros
La separación de enantiómeros presentes en una mezcla racémica se realiza mediante la técnica denominada resolución. Los métodos de resolución más utilizados son
- La resolución química, la cual consiste en la separación de los enantioméros mediante la conversión de la mezcla racémica en una mezcla dediastereoisómeros. Para ello, la mezcla de enantiómeros se hace reaccionar con el compuesto quiral que recibe el nombre de agente de resolución; con la cual se transforman los enantiómeros en diasteroisómeros, los cuales se pueden separar mediante destilación, cristalización o cromatografía. Una vez separados, se procede a la eliminación del agente de resolución para obtener cada uno de los enantiómeros puros.
- La resolución cromatográfica, la cual se basa en la utilización de técnicas cromatográficas que emplean como fase estacionaria un compuesto quiral. La separación se basa en las débiles interacciones que forman los enantiómeros con la fase estacionaria quiral. Estas interacciones tienen diferentes propiedades físicas y por tanto diferentes energías de enlace. Así, el enantiómero que forma complejos más estables con la fase estacionaria quiral se mueve más lentamente que los enantiómeros que forman complejos menos estables; y debido a ello eluyen a diferentes velocidades y separándose a lo largo de la columna.
Categoría: Estereoquímica
Wikimedia foundation. 2010.

![{ \left [ \alpha \right ] }_D^{25^\circ}](/pictures/eswiki/52/49fc242d78e0bdd56ea68931ec79b248.png)