- Candesartan
-
Candesartan
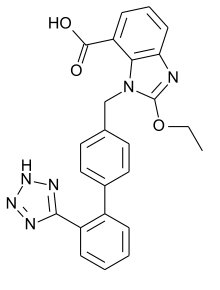 Candesartan
Candesartan
Nombre (IUPAC) sistemático Ácido 3-((2'-(2H-tetrazol-5-il)
bifenoil-4-il)metil)-2-etoxi-
3H-benzo[d]imidazol-4-carboxílicoIdentificadores Número CAS 139481-59-7 Código ATC C09CA06 PubChem 2541 DrugBank APRD00420 ChEBI ? Datos químicos Fórmula C=24 Peso mol. 440.45 gr/mol Farmacocinética Biodisponibilidad 15% (candesartan cilexetilo) Metabolismo Candesartan cilexetilo: pared intestinal; candesartan: hepatica (CYP2C9) Vida media 5.1–10.5 horas Excreción Renal 33%, fecal 67% Consideraciones terapéuticas Cat. embarazo ?
Estado legal Solo Rx
Vías adm. Oral El Candesartan (rINN) es un antagonista del receptor de la angiotensina II usado principalmente para el tratamiento de la hipertensión. El profármaco es candesartan cilexetilo es comercializado por Laboratorios Almirall,AstraZeneca y Takeda Pharmaceuticals, comúnmente bajo el nombre comercial de Parapres, Atacand, Amias y Ratacand.
Contenido
estructura
Estructura molecular del Candesartan Uso clínico
Indicaciones
Como todos los antagonistas del receptor de la angiotensina II, el candesartan está indicado para el tratamiento de la hipertensión. Los resultados del estudio CHARM a principios de 2000 demostraron los beneficios del candesartan en la reducción de la morbilidad y la mortalidad cuando se usa como principio terapéutico en la insuficiencia cardíaca.[1] Así pues, mientras que los IECAS aún son considerados como terapia de primera línea en el fallo cardiaco, el candesartan es una alternativa en pacientes que tienen intolerancia a estos últimos.
Combinación con diureticos
El Candesartan también está disponible en una formulación combinada con una dosis baja de diurético tipo tiazida, hidroclorotiazida invariable, para lograr un efecto aditivo antihipertensivo. Las preparaciones combinadas de Candesartan/hidroclorotiazida se comercializan bajo varios nombres comerciales incluidos Atacand HCT, Hytacand and Ratacand Plus.
Química y farmacocinética
El Candesartan está comercializado en la forma de ciclohexil 1-hidroxietil carbonato (cilexetil) éster, conocido como candesartan cilexetilo. El Candesartan cilexetilo se metaboliza completamente por esterasa en la pared intestinal durante la absorción a su forma activa como candesartan. El uso de la forma profármaco incrementa la biodisponibilidad del candesartano. A pesar de esto, la biodisponibilidad absoluta es relativamente pobre y va desde el 15% (tabletas de candesartan cilexetilo) hasta el 40% (solución de candesartan cilexetilo).
Ensayos aleatorios controlados
- Tras un periodo de cuatro años, se desarrolló una hipertensión en estadio 1 en casi dos tercios de los pacientes con hipertensión sin tratamiento (el grupo placebo). El tratamiento de la hipertensión con candesartan parecía estar bien tolerado y redujo el riesgo de incidencia de la hipertensión durante el perio de estudio. Así pues el tratamiento de la hipertensión parece ser factible.[1]
Contraindicaciones
En pacientes con alteración hepática se debe cuidar la dosis puesto que la metabolización es hepática. En pacientes con alteración renal se debe tener cuidado con la dosificación puesto que en su mecanismo se observa una alteración del sistema angiotensina-aldosterona, pudiendo afectar directamente alriñón y pudiendo causar un fallo renal a pacientes que previamente tenían una pequeña lesión.
Interacciones
Se debe evitar el uso concomitante con nifedipina,digoxina,enalapril, warfarina,y anticonceptivos puesto que la metabolización de uno de ellos interfiere a los otros.
Sobredosificación
No es letal, aunque puede causar hipotensión y taquicardia
Referencias
- ↑ Pfeffer M, Swedberg K, Granger C, Held P, McMurray J, Michelson E, Olofsson B, Ostergren J, Yusuf S, Pocock S (2003). «Effects of candesartan on mortality and morbidity in patients with chronic heart failure: the CHARM-Overall programme.» Lancet. Vol. 362. n.º 9386. pp. 759–66. PMID 13678868.
Enlaces externos
- Atacand web site or Atacand US, run by AstraZeneca
- Candesartan
Categorías: Código ATC C | Antagonistas de los receptores de angiotensina II
Wikimedia foundation. 2010.