- Simetría molecular
-
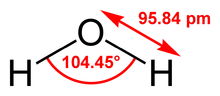 Simetría del agua.
Simetría del agua.
En química, la simetría molecular describe la simetría de las moléculas y utiliza este criterio para su clasificación. La simetría molecular es un concepto fundamental en química, pues muchas de las propiedades químicas de una molécula, como su momento dipolar y las transiciones espectroscópicas permitidas (basadas en reglas de selección como la regla de Laporte) pueden predecirse o ser explicadas a partir de la simetría de la molécula.
Aunque existen varios marcos teóricos en los que la simetría molecular puede estudiarse, la teoría de grupos es el principal. Existen muchas técnicas para establecer empíricamente la simetría molecular, incluyendo la cristalografía de rayos X y varias formas de espectroscopia.
Contenido
Elementos de simetría
La simetría de una molécula puede describirse según 5 tipos de elementos de simetría:
- El eje de simetría (Cn) es un eje alrededor del cual una rotación por
 resulta en una molécula indistinguible de la original. El C2 en el agua y el C3 en el amoníaco son dos ejemplos. Una molécula puede tener varios ejes de simetría. Aquel con un n más alto se denomina eje principal, y se le asigna el eje z en el sistema de coordenadas cartesiano.
resulta en una molécula indistinguible de la original. El C2 en el agua y el C3 en el amoníaco son dos ejemplos. Una molécula puede tener varios ejes de simetría. Aquel con un n más alto se denomina eje principal, y se le asigna el eje z en el sistema de coordenadas cartesiano. - El plano de simetría o plano especular (σ) es un plano de reflexión a través del cual se obtiene una copia idéntica a la molécula original. El agua tiene dos: uno en el plano de la misma molécula y otro perpendicular a él. Un plano de simetría puede identificarse también por su orientación cartesiana: (xz) o (yz).
- El centro de simetría (i) es aquel por el que, para cualquier átomo en la molécula, existe un átomo idéntico diametralmente opuesto.
- El eje de rotación-reflexión (Sn) es un eje alrededor del cual, una rotación por
 , seguida de una reflexión en el plano perpendicular a él, deja la molécula sin cambio.
, seguida de una reflexión en el plano perpendicular a él, deja la molécula sin cambio. - La identidad (E) consiste en ningún cambio. Toda molécula tiene este elemento, y aunque parece físicamente trivial, su consideración es necesaria para la teoría de grupos.
Operaciones
Una operación de simetría es un movimiento de un cuerpo de tal manera que tras el movimiento se obtienen puntos equivalentes o iguales a los que había antes del movimiento.Los 5 elementos de simetría tienen asociados 5 operaciones de simetría. Así, Ĉn es la rotación de una molécula alrededor de un eje y Ê es la operación de identidad. Un elemento de simetría puede tener más de una operación de simetría asociada. Puesto que C1 es equivalente a E, S1 a σ y S2 a i, todas las operaciones de simetría pueden clasificarse como rotaciones propias o impropias.
Grupos puntuales
- Véase también: Grupo de simetría
Un grupo puntual es un conjunto de operaciones de simetría que forman un grupo matemático para el que al menos un punto permanece fijo bajo todas las operaciones del grupo. En tres dimensiones hay 32 grupos, 30 de los cuales son relevantes en química.
Teoría de grupos
Un grupo se forma a partir de un conjunto de operaciones de simetría cuando:
- El resultado de la aplicación consecutiva de dos operaciones cualquiera es también un miembro del grupo (cierre)
- La aplicación de las operaciones es asociativa: A(BC) = AB(C)
- El grupo contiene la operación de identidad (E) tal que AE = EA = A para cualquier operación A en el grupo.
- Para toda operación A en el grupo, existe un elemento inverso A-1 en el grupo para el que AA-1 = A-1A = E
El orden de un grupo es el número de operaciones de simetría para tal grupo.
Por ejemplo, el grupo puntual para la molécula de agua es C2v, con las operaciones de simetría E, C2, σv y σv'. Su orden es, por tanto, 4. Cada operación es su propia inversa. Como ejemplo de cierre, una rotación C2 seguida de una reflexión σv es una operación de simetría σv':
- C2*σv = σv'
Representaciones
Las operaciones de simetría pueden representarse de muchos modos. Una representación conveniente es por matrices, donde la composición de operaciones corresponde a la multipicación de matrices. En el ejemplo C2v:
Aunque existe un número infinito de estas representaciones, normalmente se utilizan las representaciones irreducibles, pues las otras representaciones del grupo pueden describirse como combinaciones lineales de las representaciones irreducibles.
Tablas de caracteres
Para cada grupo puntual, una tabla de caracteres resume la información sobre sus operaciones de simetría y sobre sus representaciones. Dado que siempre existe un número idéntico de representaciones de simetría y de clases de operaciones de simetría, las tablas son cuadradas.
La tabla consiste en una serie de caracteres que representan cómo una representación irreducible se transforma cuando se aplica una cierta operación de simetría. Cualquier operación de simetría aplicada a una molécula en su grupo puntual la dejará sin ningún cambio. Cuando actúa sobre una entidad general, como un vector espacial o un orbital, este no ha de ser el caso necesariamente. El vector puede cambiar de signo o dirección, y el orbital puede cambiar de tipo. Para grupos puntuales simples, los valores son 1 o −1: 1 significa que el signo o fase del vector u orbital no cambia bajo la operación de simetría (es simétrico), y −1 denota un cambio de signo (asimétrico).
Las representaciones se nombran de acuerdo a un conjunto de convenciones:
- A, cuando la rotación alrededor del eje principal es simétrica
- B, cuando la rotación alrededor del eje principal es asimétrica
- E y T son representaciones doble y triplemente degeneradas respectivamente.
- Cuando el grupo puntual tiene un centro de inversión, el subíndice 'g'(del alemán gerade or even) señala ningún cambio en el signo, y el subíndice 'u' (ungerade or uneven) un cambio en el signo, en relación con la inversión.
- Con los grupos puntuales C∞v and D∞h los símbolos se toman prestados de la descripción del momento angular: Σ, Π, Δ.
Las tablas recogen también información sobre cómo los vectores cartesianos de base, las rotaciones alrededor de ellos y las funciones cuadráticas de los mismos transforman mediante la simetría operaciones del grupo, fijándose en que la irreductible representación se transforma del mismo modo. Estas indicaciones están normalmente en la parte derecha de las tablas. Esta información es importante, pues orbitales químicamente importantes (en particular, los orbitales p yd) tienen las mismas simetrías que estas entidades.
La tabla de carácter para el grupo de simetría puntual C2v es:
C2v E C2 σv(xz) σv'(yz) A1 1 1 1 1 z x2, y2, z2 A2 1 1 −1 −1 Rz xy B1 1 −1 1 −1 x, Ry xz B2 1 −1 −1 1 y, Rx yz En el ejemplo C2v, consideremos los orbitales atómicos del agua: el 2px está orientado perpendicularmente al plano de la molécula y cambia de signo con una operación C2 y σv'(yz), pero no cambia con las otras dos operaciones. Este conjunto de caracteres del orbital es, por tanto, {1, −1, 1, −1}, correspondiente a la representación irreducible B1. Del mismo modo, se entiende que el orbital 2pz tiene la simetría de la representación irreducible A1, 2py B2, y el oribital 3dxy A2.
Historia
Hans Bethe utilizó los caracteres de las operaciones de grupos puntuales en su estudio de la teoría del campo del ligando en 1929. Eugene Wigner utilizó la teoría de grupos para explicar la vibración molecular. La primera tabla de caracteres fue compilada por László Tisza en 1933 en el contexto de los espectros de vibraciones. E. Bright Wilson los utilizó en 1934 para predecir la simetría de modos normales.[1] El conjunto completo de los 32 grupos puntuales fue publicado en 1936 por Rosenthal y Murphy.[2]
Enlaces externos
Referencias
- ↑ Correcting Two Long-Standing Errors in Point Group Symmetry Character Tables Randall B. Shirts J. Chem. Educ. 2007, 84, 1882. Abstract
- ↑ Group Theory and the Vibrations of Polyatomic Molecules Jenny E. Rosenthal and G. M. Murphy Rev. Mod. Phys. 8, 317 - 346 (1936) doi 10.1103/RevModPhys.8.317
- El eje de simetría (Cn) es un eje alrededor del cual una rotación por
Wikimedia foundation. 2010.

