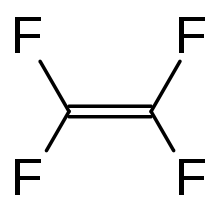
- Tetrafluoroetileno
-
Tetrafluoroetileno
Nombre (IUPAC) sistemático Tetrafluoroetileno General Otros nombres tetrafluoroetano, perfluoroetileno Fórmula molecular C2F4 Identificadores Número CAS 116-14-3 Propiedades físicas Estado de agregación Gas Masa molar 100.02 g/mol Punto de fusión 131 K (-142,15 °C) Punto de ebullición 197 K (-76,15 °C) Propiedades químicas Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl tetrafluoroetileno (TFE), también conocido como tetrafluoroeteno o perfluoroetileno, es un compuesto químico formado por carbono y flúor con la fórmula molecular C2F4. Se utiliza como materia prima en la preparación industrial de polímeros. En química orgánica, el tetrafluoroetileno es un potente dienófilo.
Contenido
Propiedades químicas
El TFE es un derivado del etileno en el cual cada uno de los cuatro átomos de hidrógeno se ha reemplazado con flúor. El tetrafluoroetileno es un gas ligeramente tóxico, incoloro e inodoro. Resulta altamente inflamable cuando es expuesto al calor o al fuego, y explosivo bajo ciertas condiciones. Como todos los fluorocarbonos es susceptible de ataque nucleofilico.
Uso industrial
La polimerización del tetrafluoroetileno se emplea para obtener polímeros como el politetrafluoretileno (PTFE), teflón, y el fluón. El PTFE es uno de las tres resinas fluorocarbonadas compuestas exclusivamente de flúor y carbono. Las otras resinas de este grupo son resinas perfluoroalcoxilos (PFA) y politetrafluoroetilenos (FEP). El TFE se utiliza también en la preparación de copolímeros como el ETFE.
Obtención
El TFE se obtiene a partir del cloroformo. El cloroformo es fluorado a través de la reacción con fluoruro de hidrógeno con el fin de producir clorodifluorometano. El TFE surge de la pirólisis del clorodifluorurometano.
- CHCl3 + 2 HF → CHClF2 + 2 HCl
- 2 CHClF2 → C2F4 + 2 HCl
Seguridad
El TFE es un agente alquilante, por lo tanto se cree que el TFE es un carcinógeno si bien todavía no se han realizado estudios concretos que establezcan la relación entre el cáncer humano y la exposición al TFE. LD50 (inhalación) = 40.000 ppm. El compuesto se maneja mejor diluida con un gas inerte porque el calentamiento localizado puede provocar la descomposición explosiva de C y CF4.Cuando se trabaja con el TFE el oxigeno debe ser escrupulosamente excluidos, ya que cataliza una autopolimerizacion, que puede llevarse a cabo con gran fuerza. También hay peligro de explosión cuando se trabaja con TFE, a causa de la compresión adiabática. Si el TFE presurizado es alojado en un recipiente a una presión más baja, el calor generado por la compresión puede ser suficiente para incendiar el TFE, causando una descomposición explosiva. En la industria, estos recipientes se lavan con nitrógeno a presión, antes de la introducción de TFE, tanto para eliminar el oxígeno como para evitar la compresión adiabática.
Categorías:- Compuestos químicos
- Compuestos de flúor
Wikimedia foundation. 2010.