- Tiocianógeno
-
Tiocianógeno

Nombre (IUPAC) sistemático n/d General Fórmula molecular n/d Identificadores Número CAS n/d Propiedades físicas Masa molar n/d Propiedades químicas Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
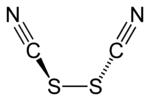
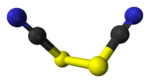
Exenciones y referenciasEl tiocianógeno, (SCN)2, es un pseudohalógeno derivado del pseudohaluro tiocianato, [SCN]−. Este compuesto hexatómico exhibe un grupo de simetría C2 y tiene la conectividad NCS-SCN.[1] Es atacado por el agua y aparentemente solo se ha obtenido como solución.
Originalmente fue preparado por la reacción del yodo con una suspensión de tiocianato de plata en éter dietílico,[2] pero esta reacción sufre de competir equilibrio atribuido al poder oxidante del yodo. Un método mejorado para la generación de tiocianógeno implica la oxidación de tiocianato plumboso, que precipita cuando las soluciones acuosas del nitrato de plomo (II) y tiocianato de sodio se combinan. Una suspensión de Pb(SCN)2 anhidro se trata con bromo en ácido acético que permite una solución de 0.1M de tiocianógeno que es estable por varios días.[3]
- Pb(SCN)2 + Br2 → (SCN)2 + PbBr2
Thiocyanogen adds to alkenes to give 1,2-bis(thiocyanato) compounds.
Referencias
- ↑ Jensen, James (2005). «Vibrational frequencies and structural determination of thiocyanogen». Journal of Molecular Structure: THEOCHEM 714 (2-3): pp. 137–141. doi:.
- ↑ Söderbäck, Erik (1919). «Studien über das freie Rhodan». Justus Liebig's Annalen der Chemie 419: pp. 217–322. doi:.
- ↑ Gardner, William Howlett; Weinberger, Harold (1939). «Thiocyanogen Solution». Inorganic Syntheses 1: pp. 84–86. doi:.
- Este artículo fue creado a partir de la traducción del artículo Thiocyanogen de la Wikipedia en inglés, bajo licencia Creative Commons Atribución Compartir Igual 3.0 y GFDL.
Categorías:- Compuestos inorgánicos de azufre
- Compuestos inorgánicos de carbono
- Sulfuros
Wikimedia foundation. 2010.
