- Cloruro de nitroblue tetrazolium
-
Cloruro de Nitroblue tetrazolium
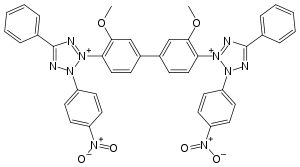
Nombre (IUPAC) sistemático dicloruro de 2-[2-metoxi-4-[3-metoxi-4-[3-(4-nitrofenil)-5-feniltetrazol-2-ium-2-il]fenil]fenil]-3-(4-nitrofenil)-5-feniltetrazol-2-ium General Otros nombres NBT Fórmula molecular C40H30Cl2N10O6 Identificadores Número CAS 298-83-9 PubChem Propiedades físicas Masa molar 817,64 g/mol Propiedades químicas Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl cloruro de nitroblue tetrazolium, también conocido como nitroazul de tetrazolio o mas comunmente nombrado por sus siglas NBT; es un compuesto químico de fórmula molecular C40H30Cl2N10O6. Está formado por la unión de dos grupos tetrazol. Entre otros usos tiene aplicaciones en immunología experimental y en inmunoensayos, donde es ampliamente utilizado para detectar la formación de anión superóxido y combinado con 5-bromo-4-cloro-3'-indolfosfato para marcar el sitio de actividad de la enzima fosfatasa alcalina.
En ambas reacciones el NBT cumple el rol de oxidante, el estado reducido del NBT se llama formazán y es un compuesto insoluble en agua de color azul muy intenso prácticamente negro. También tiene aplicaciones en el ensayo del estallido respiratorio de las células fagocíticas y como sustrato indicador de numerosos ELISA.
Contenido
Reacciónes donde se utiliza el NBT
El NBT es un oxidante poderoso en medio acuoso, en especial en condiciones ácidas, por lo que debe ser tratado con mucho cuidado para evitar su reducción una vez disuelto, manteniéndolo al abrigo de la luz y el calor. La reacción se encuentra favorecida por la formación de un precipitado insoluble que inclina el equilibrio hacia la derecha.
El NBT es comunmente utilizado como un indicador redox, en las reacciones en las que participa normalmente acepta cuatro electrones y dos protones para pasar a su forma reducida insoluble el formazán que es de color azul intenso.
Bajo determinadas condiciones esta reacción es reversible (medio básico oxidante).
El uso mas frecuente del NBT es como sustrato indicador de la formación de superóxido,[1] aunque puede ser acoplado a otras reacciones de oxido reducción como por ejemplo en las técnicas que aprovechan la actividad de la fosfatasa alcalina.

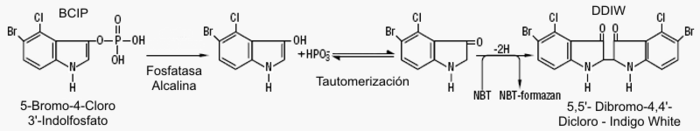
En esta última reacción se utiliza un sustrato orgánico fosfatado el BCIP, que bajo la acción de la enzima pierde su grupo fosfato. El bromo-cloro indol liberado del grupo fosfato sufre primero una reacción de tautomerización y luego es oxidado por el NBT a DDIW (5,5'-dibromo-4,4'-dicloro indigo white) un tinte también insoluble de un intenso color violeta, la combinación de ambas reacciones aumenta la definición y la sensibilidad de los test. La reacción NBT/BCIP se utiliza también para ensayos colorimétricos o espectrofotométricos de la actividad enzimática de muchas oxidoreductasas. Es el sustrato preferido en los ensayos de tipo ELISPOT.
Otra de las aplicaciones es en ensayos de tipo inmunoblot por ejemplo en el coloreo enzimático que permite la detección de determinadas enzimas en una electroforesis en gel, por ejemplo para determinar cada una de las componentes en los complejos enzimáticos de la cadena transportadora de electrones de las mitocondrias.[2]
Utilidad clínica
Inmunohistoquímica
En inmunohistoquímica tiene una amplia aplicación el uso de anticuerpos conjugados con enzimas que funcionan como marcadores, entre las enzimas que mas frecuentemente se utilizan se encuentran la peroxidasa de rábano picante (HRP por HorseRadish Peroxidase) y la fosfatasa alcalina. En ambos casos se aprovecha la formación de un producto coloreado que revela el sitio de union al anticuerpo.[3]
Test de funcionalidad del estallido respiratorio
El NBT es utilizado también en un ensayo,[4] particularmente efectivo para el diagnóstico de enfermedad granulomatosa crónica y de otras enfermedades causadas por desórdenes en el mecanismo del estallido respiratorio de las células fagocíticas. En estas enfermedades existe un defecto en la oxidasa de NADPH, por el cual las células fagocíticas son incapaces de producir especies reactivas de oxígeno (H2O2, HO2) o los radicales (HO-) necesarios para matar a los microorganismos fagocitados, como resultado los microorganismos continúan vivos dentro del fagocito, lo que causa entre otras cosas infecciones recurrentes y la formación de granulomas.[5]
Las células que son capaces de producir el estallido respiratorio son capaces también de reducir el NBT, principio en el cual se basa el test. Las células se exponen a una solucion que contiene NBT y un estimulante de la fagocitosis tal como por ejemplo el PMA y luego se observan al microscopio, las células que produjeron el estallido respiratorio muestran gránulos intensamente coloreados de negro (las vesículas fagocíticas donde se produjo la reducción del NBT). El test hace un recuento del porcentaje de células fagocíticas coloreadas sobre el número de células fagocíticas total; a mayor número de células coloreadas, mejor es la funcionalidad microbicida del paciente. Los intervalos de referencia para esta técnica usualmente varían entre 80% y 100% de células activadas luego del ensayo. Porcentajes menores probablemente indiquen un defecto en la capacidad de producción de especies reactivas de oxígeno.[6]
Véase también
- Inmunohistoquímica
- ELISA
- ELISPOT
- Estallido respiratorio
- Enfermedad granulomatosa crónica
Referencias
- ↑ Hyung Sim Choia, Jun Woo Kima, Young‐Nam Chaa & Chaekyun Kima (2006). «A Quantitative Nitroblue Tetrazolium Assay for Determining Intracellular Superoxide Anion Production in Phagocytic Cells». J Immunoassay Immunochem. 27 (1): pp. 31-44. doi:. PMID 16450867.
- ↑ Nisimoto Y, Wilson E, Heyl BL, Lambeth JD (5 de enero de 1986). «NADH dehydrogenase from bovine neutrophil membranes. Purification and properties». J. Biol. Chem. 261 (1): pp. 285–90. PMID 3941077. http://www.jbc.org/cgi/pmidlookup?view=long&pmid=3941077.
- ↑ Trinh le A, McCutchen MD, Bonner-Fraser M, Fraser SE, Bumm LA, McCauley DW (June 2007). «Fluorescent in situ hybridization employing the conventional NBT/BCIP chromogenic stain». BioTechniques 42 (6): pp. 756–9. doi:. PMID 17612300.
- ↑ Freeman, R; King B (October 1972). «Technique for the performance of the nitro-blue tetrazolium (NBT) test». Journal of Clinical Pathology 25 (10): pp. 912–914. doi:. PMID 4119008.
- ↑ Arango Rincón JC, Gámez Díaz LY, López Quintero JA. (2010). «Sistema NADPH-Oxidasa: nuevos retos y perspectivas.». Iatreia 23 (4): pp. 362-372. Resumen
- ↑ Nathan DG, Baehner RL, Weaver DK (October 1969). «Failure of nitro blue tetrazolium reduction in the phagocytic vacuoles of leukocytes in chronic granulomatous disease». J. Clin. Invest. 48 (10): pp. 1895–904. doi:. PMID 5387730.
Categorías:- Tetrazoles
- Inmunoensayos
Wikimedia foundation. 2010.