- Polaridad (química)
-
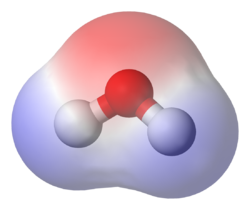 Un ejemplo común de compuesto polar es el agua (H2O). Los electrones en los átomos de hidrógeno del agua son fuertemente atraídos por el átomo de oxígeno y están, en realidad, más cerca del núcleo del oxígeno que de los del hidrógeno. Por esto, la molécula de agua tiene una carga negativa en el centro (color rojo) y una carga positiva en sus extremos (tono azul).
Un ejemplo común de compuesto polar es el agua (H2O). Los electrones en los átomos de hidrógeno del agua son fuertemente atraídos por el átomo de oxígeno y están, en realidad, más cerca del núcleo del oxígeno que de los del hidrógeno. Por esto, la molécula de agua tiene una carga negativa en el centro (color rojo) y una carga positiva en sus extremos (tono azul).
La polaridad química o solo polaridad es una propiedad de las moléculas que representa la separación de las cargas eléctricas en la misma. Esta propiedad está íntimamente relacionada con otras propiedades como la solubilidad, punto de fusión, punto de ebullición, fuerzas intermoleculares, etc. Una molecula polar puede ser NaCl que es muy polar y puede disociar con agua que a la vez es sumamente polar.
Al formarse una molécula de modo enlace ionico el par de electrones tiende a desplazarse hacia el átomo que tiene mayor electronegatividad. Esto origina una densidad de carga desigual entre los núcleos que forman el enlace (se forma un dipolo eléctrico). El enlace es más polar cuanto mayor sea la diferencia entre las electronegatividades de los átomos que se enlazan; así pues, dos átomos iguales atraerán al par de electrones covalente con la misma fuerza (establecida por la Ley de Coulomb) y los electrones permanecerán en el centro haciendo que el enlace sea apolar.
Pero un enlace polar no requiere siempre una molécula polar; para averiguar si una molécula es polar hay que atender a la cantidad de enlaces polares y la estructura de la molécula. Para ello es necesario determinar un parámetro físico llamado momento dipolar eléctrico del dipolo eléctrico. Se define como una magnitud vectorial con módulo igual al producto de la carga q por la distancia que las separa d, cuya dirección es la recta que las une, y cuyo sentido va de la carga negativa a la positiva. Esta magnitud es, por tanto, un vector; y la polaridad será la suma vectorial de los momentos dipolares de los enlaces.
De esta manera una molécula que solo contiene enlaces apolares es siempre apolar, ya que los momentos dipolares de sus enlaces son nulos. En moléculas diatómicas son apolares las moléculas formadas por un solo elemento o elementos con diferencia de electronegatividad muy reducida.
Serán también apolares las moléculas simétricas por el mismo motivo. El agua, por ejemplo, es una molécula fuertemente polar ya que los momentos dipolares de los enlaces dispuestos en "V" se suman ofreciendo una densidad de carga negativa en el oxígeno y dejando los hidrógenos casi sin electrones.
La polaridad es una característica muy importante ya que puede ayudarnos a reconocer moléculas (por ejemplo a diferenciar el trans-dicloroetano que es apolar y el cis-dicloroetano que es fuertemente polar). También es importante en disoluciones ya que un disolvente polar solo disuelve otras sustancias polares y un disolvente apolar solo disuelve sustancias apolares ("semejante disuelve a semejante"). Aunque la polaridad de un disolvente depende de muchos factores, puede definirse como su capacidad para solvatar y estabilizar cargas. Por último la polaridad influye en el estado de agregación de las sustancias así como en termodinámica, ya que las moléculas polares ofrecen fuerzas intermoleculares (llamadas fuerzas de atracción dipolo-dipolo) además de las fuerzas de dispersión o fuerza de London.
Moléculas apolares
Las moléculas apolares son aquellas moléculas que se producen por la unión entre átomos que poseen igual electronegatividad, por lo que las fuerzas con las que los átomos que conforman la molécula atraen los electrones del enlace son iguales, produciéndose así la anulación de dichas fuerzas. Un ejemplo de una molécula apolar es la molécula de Oxígeno (O2). En esta molécula cada átomo de Oxígeno atrae a los electrones compartidos hacia sí mismo con una misma intensidad pero en sentidos opuestos, por lo que se anulan las fuerzas de atracción y la molécula no se convierte, se tranforma en un dipolo.
Importancia biológica
Las moléculas anfipáticas tienen regiones polares y regiones apolares, de manera que una parte de la molécula (la polar) interacciona con el agua y la otra (la apolar) no. Esta propiedad es fundamental en los sistemas biológicos, ya que son la base de las bicapas lipídicas que forman la membrana plasmática de las células. Las principales moléculas anfipáticas de las membranas celulares son los fosfolípidos que, en un entorno acuoso, se autoorganizan en micelas o bicapas.
Referencias
- [1]Estructura atómica y enlace químico Escrito por Jaume Casabó i Gispert ( books.google.es )
Categorías:- Fisicoquímica
- Propiedades químicas
- Enlace químico
Wikimedia foundation. 2010.
