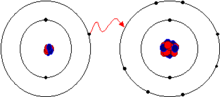
- Enlace iónico
-
La definición química de un enlace iónico es la una unión de átomos que resulta de la presencia de atracción electrostática entre los iones de distinto signo, es decir, uno fuertemente electropositivo (baja energía de ionización) y otro fuertemente electronegativo (alta afinidad electrónica). Eso se da cuando en el enlace, uno de los átomos capta electrones del otro.
Dado que los elementos implicados tienen elevadas diferencias de electronegatividad, este enlace suele darse entre un compuesto metálico y uno no metálico. Se produce una transferencia electrónica total de un átomo a otro formándose iones de diferente signo. El metal dona uno o más electrones formando iones con carga positiva o cationes con una configuración electrónica estable. Estos electrones luego ingresan en el no metal, originando un ion cargado negativamente o anión, que también tiene configuración electrónica estable. Son estables pues ambos, según la regla del octeto adquieren 8 electrones en su capa más exterior. La atracción electrostática entre los iones de carga opuesta causa que se unan y formen un compuesto.
Los compuestos iónicos forman redes cristalinas constituidas por iones de carga opuesta, unidos por fuerzas electrostáticas. Este tipo de atracción determina las propiedades observadas. Si la atracción electrostática es fuerte, se forman sólidos cristalinos de elevado punto de fusión e insolubles en agua; si la atracción es menor, como en el caso del NaCl, el punto de fusión también es menor y, en general, son solubles en agua e insolubles en líquidos apolares como el benceno.[1]
Contenido
Definición
Se denomina enlace iónico al enlace químico de dos o más átomos cuando éstos tienen una diferencia de electronegatividad de ΔEN = 2 o mayor. Este tipo de enlace fue propuesto por Walther Kossel en 1916.
En una unión de dos átomos por enlace iónico, un electrón abandona el átomo menos electronegativo y pasa a formar parte de la nube electrónica del más electronegativo. El cloruro de sodio (la sal común) es un ejemplo de enlace iónico: en él se combinan sodio y cloro, perdiendo el primero un electrón que es capturado por el segundo:
-
- NaCl → Na+Cl-
De esta manera forman dos iones de carga contraria: un catión (de carga positiva) y un anión (de carga negativa). La diferencia entre las cargas de los iones provoca entonces una fuerza de interacción electromagnética entre los átomos que los mantiene unidos. El enlace iónico es la unión en la que los elementos involucrados aceptarán o perderán electrones.
En una solución, los enlaces iónicos pueden romperse y se considera entonces que los iones están disociados. Es por eso que una solución fisiológica de cloruro de sodio y agua se marca como: Na+ + Cl-, mientras que los cristales de cloruro de sodio se marcan: Na+Cl- o simplemente NaCl.
Características
Algunas características de este tipo de enlace son:
- Ruptura de nucleo masivo.
- Son sólidos de estructura cristalina en el sistema cúbico.
- Altos puntos de fusión (entre 300 °C o 1000 °C)[2] y ebullición.
- Son enlaces resultantes de la interacción entre los metales de los grupos I y II y los no metales de los grupos XVI y XVII.
- Son solubles, como en agua y otras disoluciones acuosas.
- Una vez fundidos o en solución acuosa, sí conducen la electricidad.
- En estado sólido no conducen la electricidad. Si utilizamos un bloque de sal como parte de un circuito en lugar del cable, el circuito no funcionará. Así tampoco funcionará una bombilla si utilizamos como parte de un circuito un cubo de agua, pero si disolvemos sal en abundancia en dicho cubo, la bombilla del circuito se encenderá. Esto se debe a que los iones disueltos de la sal son capaces de acudir al polo opuesto (a su signo) de la pila del circuito y por ello éste funciona.
Clasificación
Los iones se clasifican en dos tipos:
a) Anión: Es un ion con carga negativa, lo que significa que los átomos que lo conforman tienen un exceso de electrones. Comúnmente los aniones están formados por no metales, aunque hay ciertos aniones formados por metales y no metales. Los aniones más conocidos son (el número entre paréntesis pauatata indica la carga):
- F(-) fluoruro.
- Cl(-) cloruro.
- Br(-) bromuro.
- I(-) yoduro.
- S(2-) sulfuro.
- SO4(2-) sulfato.
- NO3(-) nitrato.
- PO4(3-) fosfato.
- ClO(-) hipoclorito.
- ClO2(-) clorito.
- ClO3(-) clorato.
- ClO4(-) perclorato.
- CO3(2-) carbonato.
- BO3(3-) borato.
- MnO4(-) permanganato.
- CrO4(2-) cromato.
- Cr2O7(2-) dicromato.
b) Catión: Al contrario que los aniones, los cationes son especies químicas con déficit de electrones, lo que les otorga una carga eléctrica positiva. Los más comunes se forman a partir de metales, pero hay ciertos cationes formados con no metales.
- Na(+) sodio.
- K(+) potasio.
- Ca(2+) calcio.
- Ba(2+) bario.
- Mg(2+) magnesio.
- Al(3+) aluminio.
- Pb(2+) plomo(II) o plumboso.
- Zn(2+) zinc (ó cinc).
- Fe(2+) hierro(II) o ferroso.
- Fe(3+) hierro(III) o férrico.
- Cu(+) cobre(I) o cuproso (aunque en verdad, este ion es Cu2(2+).
- Cu(2+) cobre(II) o cúprico.
- Hg(+) mercurio(I) o mercurioso (aunque en verdad, este ion es Hg2(2+).
- Hg(2+) mercurio(II) o mercúrico.
- Ag(+) plata.
- Cr(3+) cromo(III).
- Mn(2+) manganeso(II).
- Co(2+) cobalto(II) o cobaltoso.
- Co(3+) cobalto(III) o cobáltico.
- Ni(2+) níquel(II) o niqueloso.
- Ni(3+) níquel(III) o niquélico.
- NH4(+) amonio.
- NO2(+) nitronio.
- H3O(+) hidronio.
Referencias
- ↑ Jimeno, et. al. 1999. Biologia II. Santillana, Barcelona. ISBN 84-7911-813-X
- ↑ [1] Química I. UNED. Página 245. (books.google.es).
Categorías:- Enlace químico
- Iones
-
Wikimedia foundation. 2010.