- Mano EF
-
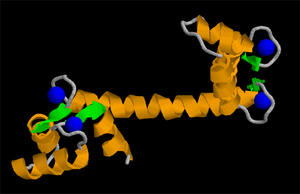
La mano EF es un dominio estructural de proteínas de tipo hélice-bucle-hélice que se encuentra en una gran familia de proteínas de unión a calcio. Consta de dos hélices alfa situado aproximadamente perpendicular el uno al otro y unidos por un corto circuito región (por lo general alrededor de 12 aminoácidos) que normalmente se une a iones de calcio. El motivo toma su nombre de la nomenclatura tradicional utilizada para describir la proteína parvalbúmina, que contiene tres de estos motivos, y está probablemente involucrada en la relajación muscular a través de su actividad de unión a calcio.Las manos EF figuran también en cada dominio estructural de la calmodulina y las proteínas de señalización en la proteína muscular troponina-C.
Contenido
Sitio de unión
El ion calcio está unido a ambas columnas de la proteína y por aminoácidos de las cadenas laterales, concretamente por los de los residuos de aminoácidos ácidos, aspartato y glutamato. Estos residuos están cargados negativamente y tendrán una interacción con los iones calcio de carga positiva. El motivo mano EF fue uno de los primeros motivos estructurales cuyos requerimientos de secuencia se analizaron en detalle. Cinco de los residuos del bucle se unen al calcio y por lo tanto tiene una marcada preferencia por las cadenas laterales que contienen oxígeno, especialmente aspartato y glutamato. El sexto de residuos en el bucle debe ser necesariamente una glicina debido a los requerimientos conformacionales de la columna. El resto de residuos son típicamente hidrofóbicos y forman un núcleo hidrofóbico que une y estabiliza las dos hélices.
En un bucle de una mano EF, el ion de calcio está coordinado en una configuración bipiramidal pentagonal. Los seis residuos que participan en la unión se encuentran en las posiciones 1, 3, 5, 7, 9 y 12; estos residuos se indican como X, Y, Z,-Y,-X y-Z. La Asp o Glu invariante en la posición 12 provee de dos oxígenos para enlazar con el calcio.
Clasificación
Las manos EF pueden dividirse en dos clases: las proteínas de señalización y proteínas de tampón/transporte. El primer grupo es el más grande e incluye a los más conocidos miembros de la familia como la calmodulina, troponina C y S100B. Estas proteínas suelen sufrir cambios conformacionales dependientes de calcio que exponen el sitio de unión. El último grupo está representado por la calbindina D9k y no cambia su conformación por calcio.
Lectura complementaria
- Branden C, Tooze J. (1999). Introduction to Protein Structure 2nd ed. Garland Publishing: New York, NY.
- Evolution of EF-hand calcium-modulated proteins. II. Domains of several subfamilies have diverse evolutionary histories. Nakayama S, Moncrief ND, Kretsinger RH; J Mol Evol 1992;34:416-448. PMID 1602495
- Comparison of terbium (III) luminescence enhancement in mutants of EF hand calcium binding proteins. Hogue CW, MacManus JP, Banville D, Szabo AG; J Biol Chem 1992;267:13340-13347. PMID 1618836
- EF-hand motifs in inositol phospholipid-specific phospholipase C. Bairoch A, Cox JA; FEBS Lett 1990;269:454-456.PMID 2401372
- The evolving model of calmodulin structure, function and activation. Finn BE, Forsen S; Structure 1995;3:7-11. PMID 7743133
Enlaces externos
Categoría:- Dominios de proteínas
Wikimedia foundation. 2010.