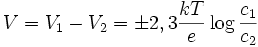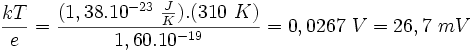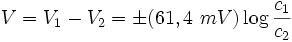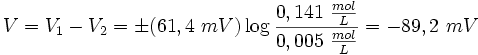- Potencial de Nernst
-
Potencial de Nernst
El potencial de reposo de una célula es producido por diferencias en la concentración de iones dentro y fuera de la célula y por diferencias en la permeabilidad de la membrana celular a los diferentes iones. El potencial de equilibrio de Nernst relaciona la diferencia de potencial a ambos lados de una membrana biológica en el equilibrio con las características relacionadas con los iones del medio externo e interno y de la propia membrana.
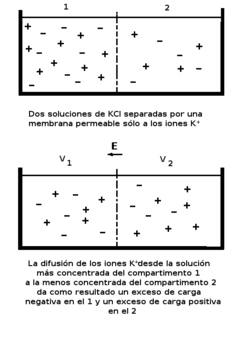
El potencial de Nernst se establece entre disoluciones separadas por una membrana semipermeable. Por ejemplo, KCL (cloruro de potasio), una sal, en medio acuoso se disocia en K+y Cl- en relación 1:1, compensando las cargas positivas de los cationes potasio con las negativas de los aniones cloruro, por lo que la disolución será electricamente neutra. De existir una membrana biológica selectivamente permeableal K+ en el interior de la solución, los K+ difundirán libremente a un lado y a otro de la membrana. Sin embargo, como hay más iones en el compartimento 1, inicialmente fluirán más iones K+ del 1 al 2 que del 2 al 1. Como el Cl- no puede difundir a través de la membrana, pronto hay un exceso de carga positiva en el compartimento 2 y un exceso de carga negativa en el 1. El fluido en cada compartimento permanece con una carga neutra, si bien las cargas en exceso se concentran a lo largo de la membrana. Las capas de carga positiva y negativa a cada lado de la membrana producen una diferencia de potencial V = V1 − V2 a través de la membrana y un campo eléctrico E, que retarda el flujo de iones positivos del compartimento 1 al 2 y que acelera su flujo del compartimento 2 al 1.
En este sistema, tras un tiempo se alcanzará el equilibrio dinámico en el que exista un flujo de K+ idéntico del 2 al 1 como del 1 al 2. Este equilibrio depende de la diferencia de concentración que favorece el movimiento del 1 al 2 y dela diferencia de potencial que favorece la difusión del 2 al 1. La diferencia de potencial V en el equilibrio viene dada, en función de las concentraciones c1 y c2 de los iones de K+ en los dos compartimentos, mediante:
Éste es el potencial de equilibrio de Nernst. Posee un valor negativo cuando la membrana es permeable a los iones positivos, y positivo cuando lo es a los aniones. Aquí k es la constante de Boltzmann y la T la temperatura absoluta. La magnitud kT es proporcional a la energía cinética media de los iones en solución y
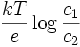 es proporcional al flujo neto de iones debido a la diferencia de concentración. La magnitud eV es proporcional al flujo neto de iones debido a la diferencia de potencial. Así, la ecuación antes citada es la condición para que estos dos flujos sean iguales y opuestos.
es proporcional al flujo neto de iones debido a la diferencia de concentración. La magnitud eV es proporcional al flujo neto de iones debido a la diferencia de potencial. Así, la ecuación antes citada es la condición para que estos dos flujos sean iguales y opuestos.Contenido
Modificaciones: Temperatura de 37 ºC
A la temperatura corporal de 37 ºC el valor de
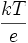 es:
es:de modo que el potencial de Nernst es
Potencial de la membrana plasmática
La membrana plasmática de una célula nerviosa separa un citoplasma con una concentración de iones K + de 0,141 mol/L de un fluido extracelulular de únicamente 0,005 mol/L del mismo ion. Considerando que ambas concentraciones estén en equilibrio, y aplicando la fórmula anterior podemos deducir el potencial de membrana en reposo:
donde este -89,5 mV teórico coincide aproximadamente con las mediciones en reposo efectuadas por técnicas de medición por microelectrodos en células vivas, de lo cual se deduce que las concentraciones de K + están casi en equilibrio. Sin embargo, para el mantenimiento de estas características se requiere una bomba iónica que propulse de forma dependiente de energía los cationes K + al interior celular.
Transmisión del impulso nervioso
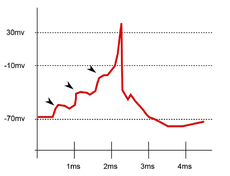
Además, los procesos de despolarización e hiperpolarización de la membrana durante, por ejemplo, la transmisión del impulso nervioso por parte de los potenciales de acción o la contracción muscular implican a un gran número de proteínas de membrana que intervienen en el flujo iónico bidireccional. De ahí que varíe tanto el potencial de membrana en estos casos: por ejemplo, una neurona pude despolarizarse hasta 30 mV, incrementando el potencial en más de 120 mV.
Véase también
Referencias
- Cromer, A.H. (1996). Física para ciencias de la vida. Reverté ediciones. ISBN para España 84-291-1808-X.
Categorías: Wikipedia:Fusionar | Fisicoquímica | Fisiología celular | Biología molecular
Wikimedia foundation. 2010.