- X-gal
-
X-gal
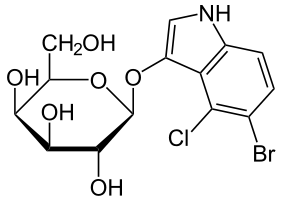
Nombre (IUPAC) sistemático 5-bromo-4-cloro-3-indolil-β-D-galactopiranósido General Fórmula molecular C14H15BrClNO6 Identificadores Número CAS 7240-90-6 Propiedades físicas Apariencia polvo blanco Masa molar 408.63 g/mol Punto de fusión 503,15 K (230 °C) Punto de ebullición 971,15 K (698 °C) Propiedades químicas Peligrosidad Punto de inflamabilidad 649,05 K (376,05 °C) Frases S S24/25 Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl compuesto orgánico X-gal (5-bromo-4-cloro-3-indolil-β-D-galactopiranósido o también BCIG) está formado, estructuralmente, por un grupo indol enlazado covalentemente a un galactósido.
Contenido
Usos
Clonación
En experimentos de clonación génica, este compuesto es usado como indicador de aquellas células que expresan la enzima β-galactosidasa, codificada en el gen lacZ del operón lac.
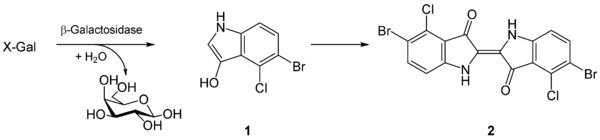
X-gal es hidrolizado por la β-galactosidasa a galactosa y 5-bromo-4-cloro-3-hidroxindol. Este último es oxidado a 5,5'-dibromo-4,4'-dicloro-índigo, un compuesto azul insoluble. De este modo, si X-gal y un inductor de la β-galactosidasa (normalmente IPTG) son disueltos en el medio de agar de una placa de cultivo, las colonias crecidas en la placa que posean un gen lacZ funcional podrán ser claramente distinguidas por su coloración azul. Además de su color característico, la volatilización del grupo indol produce un mal olor característico.
Cuando el clonaje de un gen en un vector plasmídico se está realizando en un laboratorio, X-gal es usado de esta manera para visualizar las colonias de bacterias transformadas que han captado el vector con el gen. Habitualmente se utilizan para este fin células de la bacteria E. coli, que no pueden producir la enzima β-galactosidasa. Una vez transformadas, las bacterias que portan el plásmido son capaces de producir la enzima β-galactosidasa y pueden por tanto romper el X-gal presente en el agar del medio, tornándose sus colonias de color azul. Las bacterias que no han sido transformadas, no pueden procesar X-gal y permanecen con su coloración blanca natural.
El vector plasmídico que porta el operón lac, se puede diseñar de modo que la secuencia del gen de interés a clonar se coloque específicamente en el marco de lectura del gen lacZ. Al insertar la secuencia de esta manera, se interrumpe el gen lacZ y el operón se vuelve incapaz de sintetizar la enzima β-galactosidasa funcional. De este modo, las bacterias que porten el plásmido sin la secuencia recombinante insertada, producirán β-galactosidasa activa y serán de color azul, mientras que las que no porten el plásmido o aquellas que lleven el vector recombinante, serán blancas. De las blancas, las primeras, las no transformantes, se eliminan añadiendo un antibiótico al medio (ampicilina, kanamicina, etc.) para el cual el plásmido aporta resistencia, de modo que podemos seleccionar las colonias recombinantes que portan el vector con nuestra secuencia, sencillamente por su color.
Muchos vectores de clonación comerciales como los pGem-T, portan el gen lacZα, una forma truncada de la β-galactosidasa. Estos vectores requieren formas específicas de E. coli como transformantes (tales como la cepa DH5α) para expresar una forma funcional de β-galactosidasa por un mecanismo denominado complementación α.
Sistema de doble híbrido
- Artículo principal: Sistema de doble híbrido
El gen lacZ puede ser usado como indicador (o gen reportero, del inglés "reporter") en experimentos de doble híbrido. Estos experimentos se utilizan para determinar la existencia de interacción entre dos proteínas. Para ello, se utiliza un factor de transcripción que se divide cuidadosamente en dos fragmentos cada uno de los cuales conserva su función original. El factor de transcripción es activo si ambos fragmentos llegan a encontrarse en el interior de la célula, activándose así la transcripción del gen reportero.
Si el promotor del ADN al que se une el factor de transcripción es enlazado al gen lacZ y con cada uno de los fragmentos se hacen dos proteínas de fusión (o quimeras) con dos diferentes proteínas de interés, la interacción entre estas dos proteínas se revela por la producción del pigmento azul en las colonias.[1] Dada la naturaleza manual del conteo de las colonias positivas, esta técnica se ve limitada a situaciones en las que el análisis necesario no supere el de un millón de colonias, aproximadamente.[1]
Análisis de aguas
Además de su uso en biología molecular, X-gal es usado para determinar la presencia de E. coli y otras bacterias coliformes en muestras de agua potable.
Referencias
- ↑ a b Joung J, Ramm E, Pabo C (2000). «A bacterial two-hybrid selection system for studying protein-DNA and protein-protein interactions». Proc Natl Acad Sci USA 97 (13): pp. 7382–7. doi:. PMID 10852947. http://www.pnas.org/cgi/content/full/97/13/7382.
Véase también
- IPTG.
Categoría:- Glucósidos
Wikimedia foundation. 2010.