- Carbonato de sodio
-
Carbonato de sodio
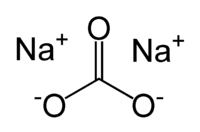
Nombre (IUPAC) sistemático Carbonato de sodio General Otros nombres Barrilla
natrón
sosa Solvay
ceniza de soda
sosa
E-500
sosa calcinada
soda ash
cristales de soda
xoda lavadaFórmula semidesarrollada Na2CO3 Fórmula molecular n/d Identificadores Número CAS 497-19-8 Número RTECS VZ4050000 Propiedades físicas Estado de agregación Sólido Apariencia Sólido blanco Densidad 2540 kg/m3; 2,54 g/cm3 Masa molar 105.9885 g/mol Punto de fusión 1124 K (851 °C) Punto de ebullición 1873 K (1600 °C) Propiedades químicas Solubilidad en agua 10,9 g por cada 100 g de agua Termoquímica ΔfH0líquido -1102 kJ/mol ΔfH0sólido -1131 kJ/mol S0sólido 135 J·mol-1·K-1 Peligrosidad NFPA 704 Frases R R36 Frases S (S2), S22, S26 Número RTECS VZ4050000 Riesgos Ingestión Causa irritación. Inhalación Dañina, deben evitarse especialmente exposiciones prolongadas. Piel Irritaciones y posiblemente quemaduras. Ojos Irritación grave, posiblemente con heridas graves. Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl carbonato sódico es una sal blanca y translúcida de fórmula química Na2CO3, usada entre otras cosas en la fabricación de jabón, vidrio y tintes. Es conocido comúnmente como barrilla, natrón, soda Solvay, ceniza de soda y sosa (no confundir con la sosa cáustica o la soda cáustica).
Puede hallarse en la naturaleza u obtenerse artificialmente, gracias a un proceso ideado y patentado en 1791 por el médico y químico francés Nicolás Leblanc. El método Leblanc implicaba las siguientes reacciones químicas:
- Reacción de la sal común con el ácido sulfúrico: 2 NaCl + H2SO4 → Na2SO4 + 2 HCl
- Reacción de calcinación del Na2SO4 con caliza y carbón: Na2SO4 + CaCO3 + 2 C → Na2CO3 + CaS + 2 CO2
Más adelante este método fue sustituido por ideado por el químico belga Ernest Solvay. Solvay fundó en 1863 la compañía Solvay donde utilizó profusamente su método que conseguía abaratar aún más el proceso y eliminar algunos de los problemas que presentaba el método Leblanc. Éste método utiliza como materias primas el cloruro sódico (sal común), el amoníaco y el carbonato cálcico (piedra caliza).
En 1915 se cerró la última fábrica de sosa Leblanc.
Contenido
Usos
El carbonato de sodio es usado para tostar (calentar bajo una ráfaga de aire) el cromo y otros extractos y disminuye el contenido de azufre y fósforo de la fundición y del acero. En la fabricación de detergentes, el carbonato de sodio es indispensable en las formulaciones al objeto de asegurar el correcto funcionamiento del resto de sustancias que lo componen, enzimas, tensioactivos, etc. durante las diferentes fases del lavado. No es de menos importancia el empleo del carbonato de sodio en aquellos procesos en los que hay que regular el pH de diferentes soluciones, nos referimos al tratamiento de aguas de la industria, así como en los procesos de flotación. Cerámica, jabones, limpiadores, ablandador de aguas duras, refinación de petróleos, producción de aluminio, textiles, pulpa y papel. Procesamiento metalúrgico, preparación de farmacéuticos, soda cáustica, bicarbonato de sodio, nitrato de sodio y varios otros usos. El carbonato de sodio y sus derivados se usan para bajar el punto de fusión del silicio y poder trabajarlo mejor, también aporta el sólido necesario para formar la red. Es comunmente usado en las palmas de las manos para evitar la sudoracion.
Propiedades
- Toxicologicas: irritación de la piel y ojos
- Apariencia: polvo blanco inodoro.
- Punto de fusión: 851 °C
- Masa molecular: 106 g/mol
- Estabilidad: es estable siempre y cuando no se lo junte con metales alcalinotérreos, aluminio, compuestos orgánicos nitrogenados, óxidos no metálicos, ácido sulfúrico concentrado, óxidos del fósforo.
Véase también
Enlaces externos
 Wikimedia Commons alberga contenido multimedia sobre Carbonato de sodio. Commons
Wikimedia Commons alberga contenido multimedia sobre Carbonato de sodio. Commons
Categorías:- Compuestos de sodio
- Carbonatos
- Gasificantes
- Productos químicos usados en fotografía
Wikimedia foundation. 2010.

