- Acetaldehído
-
Acetaldehído
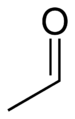
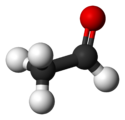
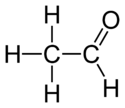
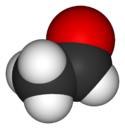
Nombre (IUPAC) sistemático Acetaldehído General Otros nombres Etanal
Aldehído acético
Aldehído etílicoFórmula estructural CHO-CH3 Fórmula molecular C2H4O Identificadores Número CAS 75-07-0 PubChem Propiedades físicas Estado de agregación Líquido incoloro con olor a frutas. Densidad 788 kg/m3; 0,788 g/cm3 Masa molar 44,05 g/mol Punto de fusión 150 K (-123,15 °C) Punto de ebullición 293 K (19,85 °C) Viscosidad ~0,215 Índice de refracción 1,3316 Propiedades químicas Solubilidad en agua completamente miscible Momento dipolar 2,7 D Compuestos relacionados Aldehídos Formaldehído
PropionaldehídoOtros compuestos Óxido de etileno Bioquímica Familia Aldehídos Peligrosidad Punto de inflamabilidad 234,15 K (-38,85 °C) NFPA 704 Temperatura de autoignición 458,15 K (185,15 °C) Frases R R12, R36/37, R40 Frases S S2, S16, S33, S36/37 Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl etanal o acetaldehído es un compuesto orgánico de fórmula CH3CHO. Es un líquido volátil, incoloro y con un olor característico ligeramente afrutado.
Contenido
Datos fisicoquímicos
- Límites de explosividad: 4 - 57 % Vol en aire
- Concentración máxima permitida en lugares de trabajo: 50 ppm (90 mg/m3)
Síntesis
Técnicamente se obtiene el etanal por hidratación del acetileno en presencia de sales de mercurio (II):

En el laboratorio se puede obtener por oxidación de etanol. Se forma por ejemplo con dicromato de potasio, reacción que es utilizada en la detección del etanol en el aire espirado.
Historia
El etanal fue sintetizado por primera vez en 1782 por Scheele mediante la oxidación de etanol con dióxido de manganeso (MnO2). Su fórmula fue averiguada por primera vez por Liebig en 1835 que le dio el nombre de acetaldehido.
Aplicaciones
En presencia de ácidos el acetaldehido forma oligómeros. El trímero (paraldehído) ha sido utilizado de somnífero. El tetrámero se utiliza como combustible sólido.
El etanal es producto de partida en la síntesis de plásticos, pinturas, lacas, en la industria del caucho, de papel y la curtición del cuero. Incluso se utiliza como conservante de carnes u otros productos alimenticios.
Toxicología
La oxidación del etanol a etanal en el metabolismo del cuerpo humano se considera como principal factor para la aparición de la resaca tras la ingesta de bebidas alcohólicas, también provoca varios efectos negativos sobre el organismo, por lo que el mismo intenta eliminarlo a través de la piel, el aliento, la metabolización hepática y la excreción del compuesto a través la orina, el etanal también se transforma en grasa en la parte abdominal del cuerpo, lo cual provoca obesidad en personas que son consumidoras de cerveza en forma frecuente.
Véase también
Categorías:- Aldehídos
- Conservantes
- Carcinógenos
Wikimedia foundation. 2010.

