- Xantina oxidasa
-
Xantina oxidasa 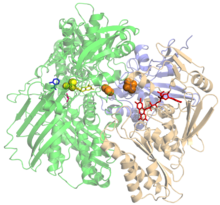
Estructura cristalográfica de la xantina oxidasa bovina.[1]HUGO 12805 Símbolo XDH Datos genéticos Locus Cr. 2 p23.1 Bases de datos Número EC 1.17.3.2 Entrez 7498 OMIM 607633 PDB 1FIQ RefSeq NM_000379 UniProt P47989 La xantina oxidasa (XO, es una forma de xantina oxidoreductasa que produce especies reactivas del oxígeno[2] ) es una enzima que cataliza la oxidación de hipoxantina a xantina y puede luego catalizar la oxidación de xantina en ácido úrico. Esta enzima juega un papel importante en el catabolismo de purinas en algunas especies, incluyendo humanos.[3] [4]
La xantina oxidasa puede ser convertida a xantina dehidrogenasa a través de una oxidación reversible con sulfhidrilo.[5]
Contenido
Reacción
Las siguientes reacciones químicas son catalizadas por la xantina oxidasa:
- hipoxantina + H2O + O2
 xantina + H2O2
xantina + H2O2 - xantina + H2O + O2
 ácido úrico + H2O2
ácido úrico + H2O2
-
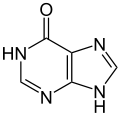
Hipoxantina (un átomo de oxígeno)
-
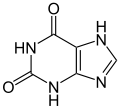
Xantina (dos átomos de oxígeno)
-
Ácido úrico (tres átomos de oxígeno)
Estructura
Es una proteína grande, con un peso molecular de 270,000, y tiene 2 moléculas de flavina (unidas como FAD), 2 átomos de molibdeno, y 8 átomos de hierro por unidad enzimática. Los átomos de molibdeno se encuentran como cofactores de molibdopterina y son los sitios activos de la enzima. Los átomos de hierro son parte de la ferredoxina de los centro hierro-azufre [2Fe-2S] y participan en reacciones de transferencia de electrones.
Mecanismo catalítico
El sitio activo de la xantina oxidasa está compuesto por una unidad de molibdopterina con el átomo de molibdeno también en coordinación con el oxígeno terminal, átomos de azufre y un hidróxido terminal.[6] En la reacción con xantina para formar ácido úrico, un átomo de oxígeno es transferido del molibdeno a la xantina. La reformación del centro activo de molibdeno ocurre por la adición de agua. Al igual que otras oxidoreductasas conteniendo molibdeno, el átomo de oxígeno introducido al substrato por la xantina oxidasa se origina del agua en lugar del dioxígeno (O2).
Importancia clínica
En humanos, la xantina oxidasa es encontrada normalmente en el hígado y no libre en la sangre. Durante un daño severo al hígado, la xantina oxidasa es liberada a la sangre, por lo cual un ensayo para xantina oxidasa en sangre es una forma de determinar is ha ocurrido daño hepático.
Debido a que la xantina oxidasa es una ruta metabólica para la formación de ácido úrico, el inhibidor de xantina oxidasa, alopurinol es utilizado en el tratamiento de la gota. Como la xantina oxidasa está involucrada en el metabolismo de la 6-mercaptopurina, se deben tomar recaudos antes de aministrar alopurinol en conjunto con 6-mercaptopurina, o su prodroga azatioprina.
La xantinuria es una enfermedad genética poco común, donde la ausencia de xantina oxidasa lleva a una elevada concentración de xantina en sangre y puede provocar problemas de salud tales como una falla renal. No existe un tratamiento específico para este desorden, a los enfermos se le indica evitar los alimentos ricos en purinas y mantener una alta ingesta de líquidos.
Se ha propuesto la inhibición de xantina oxidasa como un mecanismo para mejorar la salud cardiovascular y los síntomas ligados al síndrome de Lesch Nyhan.[7]
Inhibidores
Dentro de los inhibidores de la xantina oxidasa se encuentra el alopurinol,[8] oxipurinol,[9] y ácido pítico.[10]
Referencias
- ↑ Enroth C, Eger BT, Okamoto K, Nishino T, Nishino T, Pai EF (septiembre 2000). «Crystal structures of bovine milk xanthine dehydrogenase and xanthine oxidase: structure-based mechanism of conversion». Proc. Natl. Acad. Sci. U.S.A. 97 (20): pp. 10723–8. doi:. PMID 11005854. PMC 27090. http://www.pnas.org/content/97/20/10723.abstract.
- ↑ Ardan T, Kovaceva J, Cejková J (2004). «Comparative histochemical and immunohistochemical study on xanthine oxidoreductase/xanthine oxidase in mammalian corneal epithelium». Acta Histochem 106 (1): pp. 69–75. doi:. PMID 15032331.
- ↑ Hille R (2005). «Molybdenum-containing hydroxylases». Arch. Biochem. Biophys. 433 (1): pp. 107–16. doi:. PMID 15581570.
- ↑ Harrison R (2002). «Structure and function of xanthine oxidoreductase: where are we now?». Free Radic. Biol. Med. 33 (6): pp. 774–97. doi:. PMID 12208366.
- ↑ «Entrez Gene: XDH xanthine dehydrogenase».
- ↑ Hille R. (2006). «Structure and Function of Xanthine Oxidoreductase». European Journal of Inorganic Chemistry 2006 (10): pp. 1905–2095. doi:.
- ↑ Dawson J, Walters M (octubre 2006). «Uric acid and xanthine oxidase: future therapeutic targets in the prevention of cardiovascular disease?». British Journal of Clinical Pharmacology 62: pp. 633. doi:. PMID 17052251.
- ↑ Pacher P, Nivorozhkin A, Szabó C (marzo 2006). «Therapeutic effects of xanthine oxidase inhibitors: renaissance half a century after the discovery of alopurinol». Pharmacol. Rev. 58 (1): pp. 87–114. doi:. PMID 16507884.
- ↑ Spector T (enero 1988). «Oxypurinol as an inhibitor of xanthine oxidase-catalyzed production of superoxide radical». Biochem. Pharmacol. 37 (2): pp. 349–52. doi:. PMID 2829916.
- ↑ Muraoka S, Miura T (febrero 2004). «Inhibition of xanthine oxidase by phytic acid and its antioxidative action». Life Sci. 74 (13): pp. 1691–700. doi:. PMID 14738912.
Categorías:- Genes del cromosoma 2
- Enzimas
- hipoxantina + H2O + O2
Wikimedia foundation. 2010.