- Ácido hipoyodoso
-
Ácido hipoyodoso
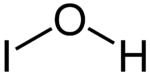
Nombre (IUPAC) sistemático Ácido monoxoyódico (I) General Otros nombres Monoxoyodato (I) de hidrógeno Fórmula semidesarrollada HIO Fórmula molecular n/d Identificadores Número CAS 14332-21-9 Propiedades físicas Masa molar 143,9118 g/mol Propiedades químicas Acidez (pKa) 10,64[1] Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl ácido hipoyodoso es un ácido oxácido inorgánico de fórmula molecular HIO, cuya molécula está formada por un átomo de yodo con estado de oxidación 1+, un átomo de oxígeno y un átomo de hidrógeno.
Contenido
Obtención
La obtención del ácido hipoyodoso es similar a la del ácido hipocloroso y el ácido hipobromoso aunque es mucho más inestable que ellos: la reacción de yodo molecular con agua permite obtener algo de ácido hipoyodoso en disolución pero la constante de dicho equilibrio de formación es muy baja (K=3·10-13 por lo que las cantidades obtenidas son muy escasas.[2]
Para desplazar el equilibrio de esta reacción hacia la derecha y aumentar el rendimiento, la reacción se realiza en presencia de mercurio(II). Se lleva a cabo cuando el yodo reacciona con una suspensión de óxido de mercurio (II) en agua con lo que se forma un aducto de yoduro de mercurio (II) con óxido de mercurio (II) que precipita en la disolución.[1] [3]
Reactividad
El ácido hipoyodoso es un ácido volátil, que tiende a la dismutación en dos etapas para dar yodo y ácido yódico.[1]
Las sales derivadas del ácido hipoyodoso son los hipoyoditos, también inestables.
Enlaces externos
- http://www.chemievorlesung.uni-kiel.de/grund/12_iod.pdf (Datos sobre el compuesto, en alemán)
Referencias
- ↑ a b c Holleman-Wiberg">A.F.Holleman, E.Wiberg, Lehrbuch der Anorganischen Chemie, Walter de Gruyter & Co. Berlín, 1995, 101. Auflage, ISBN 3-11-012641-9.
- ↑ Reactions of non-metallic inorganic compounds. Comprehensive chemical kinetics. C. H. Bamford, Charles Frank Howlett Tipper. Elsevier, 1972. ISBN: 9780444409447. Pág. 488
- ↑ Concise encyclopedia Chemistry. Mary Eagleson. Ed. Walter de Gruyter, 1994. ISBN: 3110114518. Pág. 520
Categorías:- Oxácidos con yodo
- Compuestos de yodo
Wikimedia foundation. 2010.



