- Pila (electricidad)
-
Pila (electricidad)
Una pila eléctrica es un dispositivo que convierte energía química en energía eléctrica por un proceso químico transitorio, tras de lo cual cesa su actividad y han de renovarse sus elementos constituyentes, puesto que sus características resultan alteradas durante el mismo. Se trata de un generador primario. Esta energía resulta accesible mediante dos terminales que tiene la pila, llamados polos, electrodos o bornes. Uno de ellos es el polo negativo o ánodo y el otro es el polo positivo o cátodo.
Véase también: Acumulador eléctricoEn Argentina la pila volta es una pila común. En castellano ha venido siendo costumbre llamarla así, mientras que al dispositivo recargable o acumulador, se ha venido llamando batería. Tanto pila como batería son términos provenientes de los primeros tiempos de la electricidad, en los que se juntaban varios elementos o celdas —en el primer caso uno encima de otro, "apilados", y en el segundo adosados lateralmente, "en batería"— como se sigue haciendo actualmente, para así aumentar la magnitud de los fenómenos eléctricos y poder estudiarlos sistemáticamente. De esta explicación se desprende que cualquiera de los dos nombres serviría para cualquier tipo, pero la costumbre ha fijado la distinción.
La estructura fundamental de una pila consiste en piezas de dos metales diferentes introducidas en un líquido conductor de la electricidad o electrolito.
Contenido
Principios de funcionamiento
Aunque la apariencia de cada una de estas celdas sea simple, la explicación de su funcionamiento dista de serlo y motivó una gran actividad científica en los siglos XIX y XX, así como diversas teorías.
Las pilas básicamente son dos electrodos metálicos sumergidos en un líquido, sólido o pasta que se llama electrolito. El electrólito es un conductor de iones.
Cuando los electrodos reaccionan con el electrolito, en uno de los electrodos (el ánodo) se producen electrones (oxidación), y en el otro (cátodo) se produce un defecto de electrones (reducción). Cuando los electrones sobrantes del ánodo pasan al cátodo a través de un conductor externo a la pila se produce una corriente eléctrica.
Como vemos, en el fondo Se trata de una reacción de oxidación y otra de reducción que se producen simultáneamente.
Características, propiedades y forma de utilización de las pilas
Voltaje
El voltaje, tensión o diferencia de potencial que produce un elemento electroquímico viene determinado completamente por la naturaleza de las sustancias de los electrodos y del electrolito, así como por su concentración. Walther Nernst obtuvo el premio Nobel de química de 1920 por haber formulado cuantitativamente y demostrado las leyes que rigen este fenómeno. La conexión de elementos en serie permite multiplicar esta tensión básica cuanto se quiera.
Las propiedades puramente eléctricas de una pila se representan mediante el modelo adjunto. En su forma más sencilla está formado por una fuente de tensión perfecta —es decir, con resistencia interna nula— en serie con un resistor que representa la resistencia interna. El condensador de la versión más compleja es enormemente grande y su carga simula la descarga de la pila. Además de ello entre los terminales también aparece una capacitancia, que no suele tener importancia en las aplicaciones de corriente continua.
 Símbolo de una pila (izquierda); modelo eléctrico simplificado (centro); modelo más elaborado (derecha).
Símbolo de una pila (izquierda); modelo eléctrico simplificado (centro); modelo más elaborado (derecha).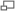
Una vez fijada la tensión, la ley de Ohm determina la corriente que circulará por la carga y consecuentemente el trabajo que podrá realizarse, siempre naturalmente que esté dentro de las posibilidades de la pila, que no son infinitas, viniendo limitadas fundamentalmente por el tamaño de los electrodos —lo que determina el tamaño externo de la pila completa— y por su separación. Estos condicionamientos físicos se representan en el modelo de generador como una resistencia interna por la que pasaría la corriente de un generador ideal, es decir, de uno que pudiese suministrar una corriente infinita al voltaje predeterminado.
Conforme la célula se va gastando, su resistencia interna va aumentando, lo que hace que la tensión disponible sobre la carga vaya disminuyendo, hasta que resulte insuficiente para los fines deseados, momento en el que es necesario reemplazarla. Para dar una idea, una pila nueva de las ordinarias de 1,5 V tiene una resistencia interna de unos 0,35 Ω, mientras que una vez agotada puede tener varios. Esta es la razón de que la mera medición de la tensión con un voltímetro no sirva para indicar el estado de una pila; en circuito abierto incluso una pila gastada puede indicar 1,4 V, dada la carga insignificante que representa la resistencia de entrada del voltímetro, pero, si la medición se hace con la carga que habitualmente soporte, la lectura bajará a 1,0 V o menos, momento en que esa pila ha dejado de tener utilidad. Las actuales pilas alcalinas tienen una curva de descarga más suave que las previas de carbón; su resistencia interna aumenta proporcionalmente más despacio.
Cuando se necesita una corriente mayor que la que puede suministrar un elemento único, siendo su tensión en cambio la adecuada, se pueden añadir otros elementos en la conexión llamada en paralelo, es decir, uniendo los polos positivos de todos ellos, por un lado, y los negativos, por otro. Este tipo de conexión tiene el inconveniente de que si un elemento falla antes que sus compañeros, o se cortocircuita, arrastra irremisiblemente en su caída a todos los demás.
Como todas las reacciones químicas, las que se producen dentro de una pila son sensibles a la temperatura, acelerándose normalmente cuando ésta aumenta, lo que se traducirá en un pequeño aumento de la tensión. Más importante es el caso de la bajada, pues cuando se alcanzan las de congelación muchas pilas pueden dejar de funcionar o hacerlo defectuosamente, cosa que suelen advertir los fabricantes. Como contrapartida, si se almacenan las pilas refrigeradas, se prolongará su buen estado.Duración fuera de servicio
Lo ideal sería que las reacciones químicas internas no se produjeran más que cuando la pila esté en servicio, pero la realidad es que las pilas se deterioran por el mero transcurso del tiempo, aunque no se usen, pues los electrodos resultan atacados en lo que se conoce con el nombre de acción local. Puede considerarse que una pila pierde unos 6 mV por mes de almacenamiento, influyendo mucho en ello la temperatura. Actualmente esto no constituye un problema serio pues, dado el enorme consumo que hay de los tipos corrientes, las que se ofrecen en el comercio son de fabricación reciente. Algunos fabricantes han empezado a imprimir en los envases la fecha de caducidad del producto, lo que es una práctica encomiable.
Historia
La primera pila eléctrica fue dada a conocer al mundo por Volta en 1800, mediante una carta que envió al presidente de la Royal Society londinense. Se trataba de una serie de pares de discos (apilados) de cinc y de cobre (o también de plata), separados unos de otros por trozos de cartón o de fieltro impregnados de agua o de salmuera, que medían unos 3 cm de diámetro. Cuando se fijó una unidad de medida para la diferencia de potencial, el voltio (precisamente en honor de Volta) se pudo saber que cada uno de estos elementos suministra una tensión de 0,75 V aproximadamente, pero ninguno de estos conceptos estaba disponible entonces. Su apilamiento conectados en serie permitía aumentar la tensión a voluntad, otro descubrimiento de Volta. El invento constituía una novedad absoluta y gozó de un éxito inmediato y muy merecido, ya que inició la era eléctrica en que actualmente vivimos, al permitir el estudio experimental preciso de la electricidad, superando las enormes limitaciones que presentaban para ello los generadores electrostáticos, únicos disponibles con anterioridad. Otra disposición también utilizada y descrita por Volta para el aparato estaba formada por una serie de vasos con líquido (unos junto a otros, en batería), en los que se sumergían las tiras de los metales, conectando externamente un metal con otro.
Inmediatamente empezaron a hacerse por toda Europa y América innumerables pruebas con diversos líquidos, metales y disposiciones, tratando de mejorar las características del aparato original, cosa que pocas veces se consiguió, pero que originó una infinidad de distintos tipos de pilas, de los cuales no ha quedado memoria más que de los más notables.
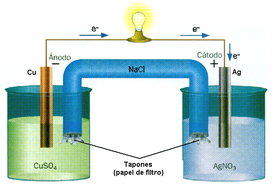
La pila Daniell, dada a conocer en 1836 y de la que luego se han usado ampliamente determinadas variantes constructivas, está formado por un electrodo de Zinc sumergido en una disolución de sulfato de Zinc y otro electrodo de cobre sumergido en una disolución concentrada de sulfato de cobre. Ambos electrolitos están separados por una pared porosa para evitar su reacción directa. En esta situación la tensión de disolución del zinc es mayor que la presión de los iones Zn++ y el electrodo se disuelve, emitiendo Zn++ y quedando cargado negativamente, proceso en el que se liberan electrones y que recibe el nombre de oxidación. En la disolución de sulfato de cobre, debido a su gran concentración de iones Cu++, se deposita Cu sobre el electrodo de este metal que de este modo queda cargado positivamente, mediante el proceso denominado reducción, que implica la incorporación de electrones. Esta pila presenta una diferencia de potencial de entre 1,07 y 1,14 V entre sus electrodos. Su gran ventaja respecto a otras de su tiempo fue la constancia del voltaje generado, debido a la elaborada disposición, que facilita la despolarización, y a la reserva de electrolito, que permite mantener su concentración durante más tiempo.
La pila Grove (1839) utiliza como despolarizador el ácido nítrico NO3H. Su fuerza electromotriz es de 1,9 a 2,0 V. Originariamente utilizaba platino para el ánodo, pero Cooper y Bunsen lo sustituyeron luego por carbón; el cátodo era de zinc tratado con mercurio. Fue muy apreciado por su estabilidad y su mayor energía, a pesar del gran inconveniente que representa la emisión de humos corrosivos. El mismo Grove y en el mismo año elaboró una pila que producía energía eléctrica por medio de la recombinación de hidrógeno y de oxígeno, lo que constituye el precedente de los generadores contemporáneos conocidos como pilas de combustible.
La pila Leclanché (1868) utiliza una solución de cloruro amónico en la que se sumerjen electrodos de cinc y de carbón, rodeado éste último por una pasta de dióxido de manganeso y polvo de carbón como despolarizante. Suministra una tensión de 1,5 V y su principal ventaja es que se almacena muy bien, pues el cinc no es atacado más que cuando se extrae corriente del elemento.
Este tipo de pila sirvió de base para el importante avance que constituyó la pila denominada seca, al que pertenecen prácticamente todas las utilizadas hoy. Los tipos hasta ahora descritos eran denominados húmedos, pues contenían líquidos, que no sólo hacían inconveniente su transporte, sino que solían emitir gases peligrosos y olores desagradables. Las pilas secas, en cambio, estaban formadas por un recipiente cilíndrico de zinc, que era el polo negativo, relleno de una pasta electrolítica, y por una barra de carbón en el centro (electrodo positivo), todo ello sellado para evitar fugas. Previamente se habían realizado otro tipo de pilas secas, como la de Zamboni (1812), pero eran dispositivos puramente experimentales, que no proporcionaban ninguna corriente útil. La sequedad es relativa, en primer lugar porque un elemento rigurosamente seco no suministraría electricidad alguna, de modo que lo que se encuentra en el interior de las pilas es una pasta o gel, cuya humedad se procura por todos los medios conservar, pero además porque el uso y el paso del tiempo tienden a corroer el contendedor, de modo que la pila puede verter parte de su electrolito al exterior, donde puede atacar a otros metales. Por esta razón se recomienda extraerlas cuando no se utilizan durante mucho tiempo o cuando ya han trabajado mucho. Este inconveniente está muy atenuado en los productos de finales del siglo XX gracias a la utilización de recipientes de acero inoxidable, pero todavía se produce alguna vez.
Importantes en otro sentido han sido las pilas patrón, destinadas a usos de calibración y determinación de unidades, como la pila Clark (1870), de zinc y mercurio, cuya tensión era de 1,457 V, y la pila Weston (1891), de cadmio y mercurio, con 1,018 V. Estas tensiones se miden en vacío, es decir, sin tener ninguna carga externa conectada, y a una temperatura constante de 20º C.
Tipos corrientes de pilas
La distinción entre pilas que utilizan un electrolito y las que utilizan dos, o entre pilas húmedas y secas, son exclusivamente de interés histórico y didáctico, pues todas las pilas que se utilizan actualmente son prefabricadas, estancas y responden a tipos bastante fijos, lo que facilita su comercialización y su uso.
Las pilas eléctricas y algunos acumuladores se presentan en unas cuantas formas normalizadas. Las más frecuentes comprenden la serie A (A, AA, AAA, AAAA), A B, C, D, F, G, J y N, 3R12, 4R25 y sus variantes, PP3, PP9 y las baterías de linterna 996 y PC926. Las características principales de todas ellas y de otros tipos menos habituales se incluyen en la tabla siguiente (que también puede verse separadamente).
Tipos de pila estandarizados
USA IEC ANSI Otros Forma Voltaje PRISMA RECTANGULAR linterna, 996 prisma 68 mm × 68 mm × 115 mm 6 V (nota) radio, linterna, PC926 prisma 127 mm × 136,5 mm × 73 mm alto, terminales rosca 12 V (nota) 3R12 GP312S prisma 67 mm × 62 mm × 22 mm 4,5 V 4R25X 908 radio, MN908 prisma 67,7 mm × 67,7 mm × 110 mm, terminales de muelle 6 V (nota) 4R25 915 radio prisma 67,7 mm × 67,7 mm × 110 mm, terminales rosca 6 V (nota) 4LR25-2 918A MN918 prisma 127 mm × 136,5 mm × 73 mm, terminales rosca 6 V (nota) PP3 6LR61 1604A 6F22, 6R61, MN1604, 9V prisma 48 mm × 25 mm × 15mm 9 V (nota) PP6 6F22 1602 6F50-2, Energizer 246 prisma 69,9mm × 34,5mm × 34,5mm 9 V (nota) PP9 6F100 1603 prisma 51,6mm × 65,1 mm × 80,2 mm 9 V (nota) A alimentación de filamentos de receptores de radio antiguos prisma de varios tamaños 6 V B alimentación de placa de receptores de radio antiguos prisma de varios tamaños, a veces con tomas intermedias 45 V, 60 V, 90 V, etc. C polarización de rejilla de receptores de radio antiguos prisma de varios tamaños, a veces con tomas intermedias 4,5 V, 6 V, 9 V, etc. CILINDRICAS AAAA 25A MN2500 cilindro L 42 mm, D 8 mm 1,5 V AAA LR03 24A R03, MN2400, AM4, UM4, HP16, Micro cilindro L 44,5 mm, D 10,5 mm 1,5 V 1/3 AAA cilindro, L 20,5mm, D 10,5mm 1,5V 2/3 AAA cilindro, L 30mm, D 10,5mm 1,5V 4/3 AAA cilindro, L 60mm, D 10,5mm 1,5V 5/3 AAA cilindro, L 67mm, D 10,5mm 1,5V 1/4 AAA cilindro, L 14mm, D 10,5mm 1,5V 5/4 AAA cilindro, L 50mm, D 10,5mm 1,5V AA LR06 15A R06, MN1500, AM3, UM3, HP7, Mignon cilindro L 50 mm, D 14,2 mm 1,5 V 1/3 AA cilindro, L 17,5mm, D 14,2mm 1,5V 2/3 AA cilindro, L 28,7mm, D 14,2mm 1,5V 4/3 AA cilindro, L 65,2mm, D 14,2mm 1,5V 4/5 AA cilindro, L 43mm, D 14,2mm 1,5V A cilindro L 50 mm, D 17 mm 1,5 V 1/3 A cilindro, L 21mm, D 17mm 1,5V 2/3 A cilindro, L 28.5mm, D 17mm 1,5V 4/5 A cilindro, L 43mm, D 17mm 1,5V C LR14 14A R14, UM2, MN1400, HP11, Baby cilindro L 46 mm, D 26 mm 1,5 V 2/3 C cilindro, L 31mm, D 26mm 1,5V Sub C cilindro, L 43 mm, D 23 mm 1,5 V 2/3 Sub C cilindro, L 28mm, D 23mm 1,5V 4/3 Sub C cilindro, L 50mm, D 23mm 1,5V 4/5 Sub C cilindro, L 34mm, D 23mm 1,5V D LR20 13A R20, MN1300, UM1, HP2, Mono cilindro L 58 mm, D 33 mm 1,5 V 1/2 D cilindro, L 37mm, D 33mm 1,5V 4/3 D cilindro, L 89mm, D 33mm 1,5V F cilindro L 87 mm, D 32 mm 1,5 V G cilindro L 105 mm, D 32 mm 1,5 V J cilindro L 150 mm, D 32 mm 1,5 V N LR1 910A Lady y las de la calculadora HP-41 cilindro L 30,2 mm, D 12 mm 1,5 V CR123A cilindro L 34,5 mm, D 16 mm 3 V BOTON GRANDE CR 1616 botón, H 1,6mm, D 16mm 3V CR 1620 botón, H 2mm, D 16mm 3V CR 2016 botón, H 1,6mm, D 20mm 3V CR 2025 botón, H 2,5mm, D 20mm 3V CR 2032 botón, H 3,2mm, D 20mm 3V CR 2430 botón, H 3mm, D 24,5mm 3V CR 2450 botón, H 5mm, D 24,5mm 3V BOTON LR44 Alcalina botón, H 5,4mm, D 11,6mm 1,5V PX28 Óxido mercúrico; ya no se fabrica botón, H 25,2mm, D 13mm 6V PX28S Óxido de plata; sustituto de PX28 botón, H 25,2mm, D 13mm 6,2V PX28L L544 Iones de litio; sustituto de PX28 botón, H 25,2mm, D 13mm 6V
OTRAS nota: Las pilas de 6 V, 9 V y 12 V suelen fabricarse mediante múltiplos de elementos de 1.5 V en serie. Cuando se utilizan acumuladores (NiMH o NiCd), el voltaje total ha de multiplicarse por 0.83, ya que cada elemento suministra 1,24 V en vez de 1,5 V. Hay acumuladores alcalinos que suministran 1,5 V.
La norma europea aplicable es IEC 60086-1 Primary batteries - Part 1: General (Norma inglesa: BS397).
La serie LR-xx indica que son pilas alcalinas. Las de zinc-carbón no llevan "L": R-6, R-20, etc.
La norma norteamericana aplicable es ANSI C18.1 American National Standard for Dry Cells and Batteries-Specifications.
Hay abundantes artículos sobre muchos aspectos de las pilas y de su utilización en equipos portátiles en Buchmann.ca.
Pueden encontrarse datos interesantes sobre los códigos de los distintos fabricantes y sus equivalencias en [1] y en [2].
Las pilas y el ambiente
Los metales y productos químicos constituyentes de las pilas pueden resultar perjudiciales para el medio ambiente, produciendo contaminación química. Es muy importante no tirarlas a la basura (en algunos países no está permitido), sino llevarlas a centros de reciclado. En algunos países, la mayoría de los proveedores y tiendas especializadas también se hacen cargo de las pilas gastadas. Una vez que la envoltura metálica que recubre las pilas se daña, las sustancias químicas que contienen se ven liberadas al medio ambiente causando contaminación. Con mayor o menor grado, las sustancias son absorbidas por la tierra pudiéndose filtrar hacia los mantos acuíferos y de éstos pueden pasar directamente a los seres vivos, entrando con esto en la cadena alimenticia.
Estudios especializados indican que una micro pila de mercurio, puede llegar a contaminar 600.000 litros de agua, una de zinc-aire 12.000 litros y una de óxido de plata 14.000 litros.
Las pilas son residuos peligrosos por lo que desde el momento en que se empiezan a reunir, deben ser manejadas por personal capacitado que siga las precauciones adecuadas empleando todos los procedimientos técnicos y legales del manejo de residuos peligrosos.
Referencias
Véase también
Enlaces externos
 Wikimedia Commons alberga contenido multimedia sobre Pila (electricidad).
Wikimedia Commons alberga contenido multimedia sobre Pila (electricidad).- Pilas: un enemigo en casa
- barrapunto.com: Cómo alargar la vida de las baterías
- barrapunto.com: Encuesta y comentarios sobre baterías
- CEMPRE Uruguay, Compromiso empresarial para el reciclaje, página sobre la gestión de pilas y baterías en Uruguay
Categoría: Pilas eléctricas
Wikimedia foundation. 2010.