- Ácido etilendiaminotetraacético
-
Ácido etilendiaminotetraacético 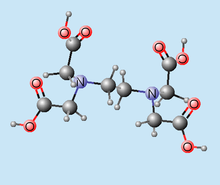
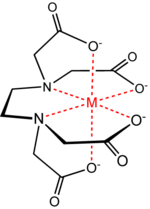
Nombre (IUPAC) sistemático Ácido etilendiaminotetraacético o EDTA Identificadores Número CAS 60-00-4 Código ATC V03AC V03 AC PubChem 6049 Datos químicos Fórmula C10H16N2O8 Peso mol. 292.24564 g/mol Farmacocinética Vida media 25 horas Excreción Orina 90-95%, heces 5%. Datos clínicos Cat. embarazo ? Estado legal ? Vías de adm. Oral, parenteral, El ácido etilendiaminotetraacético[1] o EDTA, es una sustancia utilizada como agente quelante que puede crear complejos con un metal que tenga una estructura de coordinación octaédrica. Coordina a metales pesados de forma reversible por cuatro posiciones acetato y dos amino, lo que lo convierte en un ligando hexadentado, y el más importante de los ligandos quelatos.
Contenido
Importancia biomédica
El EDTA y sus derivados tienen la valiosa propiedad química de combinarse con iones metálicos polivalentes en solución para formar complejos coordinados cíclicos de anillo (no iónicos), solubles en agua y virtualmente no disociables. A estos complejos se les conoce como quelatos.
Importancia química
Titulación de complejos
EDTA, ácido etilendiaminotetraacético, tiene cuatro carboxilo y dos grupos amino; grupos que pueden actuar como donantes de pares electrones, o bases de Lewis. La capacidad de EDTA para potencialmente donar sus seis pares de electrones para la formación de enlaces covalentes coordinados a cationes metálicos hace al EDTA un ligando hexadentado. Sin embargo, en la práctica EDTA suele estar parcialmente ionizado, y, por tanto, formar menos de seis enlaces covalentes coordinados con cationes metálicos.
El Disodio EDTA se utiliza comúnmente para estandarizar las soluciones acuosas de cationes de metales de transición. Tenga en cuenta que la forma abreviada de Na4-xHxY se puede utilizar para representar a cualquier especie de EDTA, con la designación de x número de protones ácidos enlazados a la molécula de EDTA.
EDTA forma un complejo octaédrico con la mayoría de cationes metálicos 2+, M2+, en solución acuosa. La razón principal de que el EDTA se utiliza de manera amplia en la normalización de los cationes metálicos de soluciones es que la constante de formación para la mayoría de complejos cationes metálicos con EDTA es muy alta, lo que significa que el equilibrio de la reacción:
- M2+ + H4Y → MH2Y + 2H+
se encuentra ahora a la derecha. Llevar a cabo la reacción en una solución tampón básico elimina H+ , cuando este se forma, lo que también favorece la formación de los complejos de EDTA con cationes metalicos como producto de la reacción. Para la mayoría de los propósitos se puede considerar que la formación de los complejos EDTA con cationes metálicos es completa, y esta es la principal razón por el cual el EDTA se utiliza en valoraciones/estandarizaciones de este tipo [1].
Farmacología
El EDTA y sus sales sódicas derivadas se utilizan para precipitar metales pesados tóxicos de manera que puedan ser excretados por la orina. La fijación de plomo, cadmio, níquel por el EDTA, muestra una relación favorable en el cuerpo humano, sin embargo, la unión a cobre, hierro y cobalto no es tan fuerte.
El EDTA quela óptimamente dentro de un estrecho margen de pH, dentro del cual están el pH de la sangre y de los líquidos tisulares. Para ser útil, el EDTA y cualquier agente quelante, deben tener un grado de pH de óptima actividad fijadora para cada metal.
Farmacocinética y modo de acción
El EDTA puede ser aplicado intravenosa o tópicamente. Aunque se puede dar oralmente y su absorción en la vía digestiva es buena, se prefiere administrar intravenosamente en virtud de ser más eficaz para aumentar la tasa de excreción urinaria de los quelatos. Tras la administración IV el fármaco se absorbe y después de 6 horas puede detectarse en orina de un 60 a un 90% de la cantidad administrada. A las 25 horas puede recuperarse hasta un 99%. El resto aparece en las heces fecales. Los efectos farmacológicos del EDTA resultan de la formación de quelatos con metales divalentes y trivalentes en el cuerpo. En la forma de edetato de calcio disódico se aplica para quelar metales con gran afinidad al quelante más que al calcio iónico. Es de gran utilidad para quelar el plomo que se encuentra en hueso. En sangre, el fármaco puede encontrarse en plasma y debido a que se excreta por vía urinaria, el paciente debe ser evaluado cuidadosamente y certificar que tiene una función renal adecuada. Se ha detectado un pequeño porcentaje en el fluido espinal.
Toxicidad
La principal toxicidad del EDTA es en el riñón. Las dosis repetidas puede causar anomalías en el túbulo contorneado distal. Cuando se detectan estos efectos, la descontinuación de la terapia favorece la desaparición de los efectos anormales2.
Derivados del EDTA
Entre los derivados del EDTA se encuentran el ácido hidroxietiletilendiaminotriacético (HEDTA), el ácido dihidroxietiletilendiaminodiacético, el ácido dietilentriaminopentaacético (DTPA), el ácido trietilentetraminohexaacético (TTHA) y el etilendiaminotetraacetato de calcio y disodio (CaNa2EDTA). EL uso en niños del CaNa2EDTA para el tratamiento de la encefalopatía por plomo ha dado buenos resultados.[2]
Indicaciones terapéuticas
EL EDTA es muy utilizado para quelación del plomo en la intoxicación por este metal. Regularmente se utiliza en la forma de CaNa2EDTA porque el EDTA sódico, cuando se utiliza solo, puede causar tetania por hipocalcemia.[3]
En Odontología, el EDTA se utiliza como como ensanchador químico en Endodoncia, ampliamente difundido entre las soluciones utilizadas con mayor frecuencia para la irrigación y aprovechando su propiedad de quelante, capta el Calcio de los tejidos dentarios. También puede ser combinado con Cetrimide para formar EDTAC (se agrega a la composición un bromuro cuaternario amoniado, para reducir la tensión superficial y así favorecer la penetración) logrando remover el barrillo dentinario o smear layer.
Notas
- ↑ Se utiliza aquí el nombre completo del fármaco porque el acrónimo EDTA se utiliza por convencionalismo. Esto se hace para estar en conformidad con los textos de farmacología y farmacopeas, en donde las cabeceras de los artículos y capítulos se utiliza el nombre completo, mientras que en el cuerpo del texto se usa el acrónimo.
- ↑ Versenato de calcio disódico en el tratamiento de la encefalopatía por plomo. Autores: Karpinski, F.E.; F, Rieders y L.S. Girsh. Journal of Pediatrics, 1953
- ↑ The Pharmacological Basis of Therapeutics. Goodman & Gilman. 8th Edition. ISBN 0-02-946568-0
Enlaces
- Titulación de complejos (en inglés)[1]
Categorías:- Agentes quelantes
- Toxicología
- Antídotos
- Productos químicos usados en fotografía
Wikimedia foundation. 2010.