- Ácido perclórico
-
Ácido perclórico
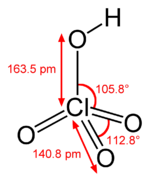
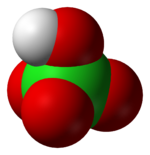
Nombre (IUPAC) sistemático Ácido tetraoxoclórico (VII) General Otros nombres Clorato (VII) de hidrógeno Fórmula semidesarrollada HClO4 Fórmula molecular n/d Identificadores Número CAS 7601-90-3 Propiedades físicas Densidad 1670 kg/m3; 1,67 g/cm3 Masa molar 100.46 g/mol Punto de fusión 161 K (-112 °C) Punto de ebullición 292 K (19 °C) Propiedades químicas Solubilidad en agua Miscible Compuestos relacionados Compuestos relacionados Ácido cloroso
Ácido hipocloroso
Ácido clóricoPeligrosidad NFPA 704 Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasÁcido perclórico es la denominación que se le otorga al ácido que resulta de la unión del óxido perclórico con H2O. Recibe tal nombre debido a que el cloro actúa con el estado de oxidación +7, que es el mayor de los cinco que posee (−1, +1, +3, +5 y +7).
Es un ácido fuerte, por lo que en disolución acuosa se disocia totalmente y hay que tener precauciones a la hora de manejarlo. A concentraciones superiores al 72% es inestable y puede resultar explosivo.
Fórmula química
La fórmula del ácido perclórico es HClO4, y se obtiene por los siguientes pasos:
- Formación del óxido:
- 2 Cl + 7 O2 → 2 Cl2O7
- Formación del ácido:
- Cl O7 + H2O → 2 HClO4
Categoría:- Oxácidos con cloro
- Formación del óxido:
Wikimedia foundation. 2010.

