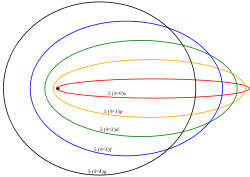
- Modelo atómico de Sommerfeld
-
El modelo atómico de Sommerfeld es un modelo atómico hecho por el físico alemán Arnold Sommerfeld (1868-1951) que básicamente es una generalización relativista del modelo atómico de Bohr (1913).
Contenido
Insuficiencias del modelo de Bohr
El modelo atómico de Bohr funcionaba muy bien para el átomo de hidrógeno, sin embargo, en los espectros realizados para átomos de otros elementos se observaba que electrones de un mismo nivel energético tenían distinta energía, mostrando que existía un error en el modelo. Su conclusión fue que dentro de un mismo nivel energético existían subniveles, es decir, energías ligeramente diferentes. Además desde el punto de vista teórico, Sommerfeld había encontrado que en ciertos átomos las velocidades de los electrones alcanzaban una fracción apreciable de la velocidad de la luz. Sommerfeld estudió la cuestión para electrones relativistas.
Características del modelo
En 1916, Sommerfeld perfeccionó el modelo atómico de Bohr intentando paliar los dos principales defectos de éste. Para eso introdujo dos modificaciones básicas: Órbitas casi-elípticas para los electrones y velocidades relativistas. En el modelo de Bohr los electrones sólo giraban en órbitas circulares. La excentricidad de la órbita dio lugar a un nuevo número cuántico: el número cuántico azimutal, que determina la forma de los orbitales, se lo representa con la letra l y toma valores que van desde 0 hasta n-1. Las órbitas con:
- l = 0 se denominarían posteriormente orbitales s o sharp
- l = 1 se denominarían p o principal.
- l = 2 se denominarían d o diffuse.
- l = 3 se denominarían f o fundamental.
Para hacer coincidir las frecuencias calculadas con las experimentales, Sommerfeld postuló que el núcleo del átomo no permanece inmóvil, sino que tanto el núcleo como el electrón se mueven alrededor del centro de masas del sistema, que estará situado muy próximo al núcleo al tener este una masa varios miles de veces superior a la masa del electrón.
Para explicar el desdoblamiento de las líneas espectrales, observando al emplear espectroscopios de mejor calidad, Sommerfeld supone que las órbitas del electrón pueden ser circulares y elípticas. Introduce el número cuántico secundario o azimutal, en la actualidad llamado l, que tiene los valores 0, 1, 2,…(n-1), e indica el momento angular del electrón en la órbita en unidades de
 , determinando los subniveles de energía en cada nivel cuántico y la excentricidad de la órbita.
, determinando los subniveles de energía en cada nivel cuántico y la excentricidad de la órbita.Resumen
En 1916, Arnold Sommerfeld, con la ayuda de la relatividad de Albert Einstein, hizo las siguientes modificaciones al modelo de Bohr:
- Los electrones se mueven alrededor del núcleo en órbitas circulares o elípticas.
- A partir del segundo nivel energético existen dos o más subniveles en el mismo nivel.
- El electrón es una corriente eléctrica minúscula.
En consecuencia el modelo atómico de Sommerfeld es una generalización del modelo atómico de Bohr desde el punto de vista relativista, aunque no pudo demostrar las formas de emisión de las órbitas elípticas, solo descartó su forma circular.
Véase también
 Portal:Física. Contenido relacionado con Física.
Portal:Física. Contenido relacionado con Física.- Modelo atómico de Thomson
- Modelo atómico de Rutherford
- Modelo atómico de John Dalton
- Número cuántico
Categoría:- Modelos atómicos
Wikimedia foundation. 2010.