- Reacción de eliminación
-
Reacción de eliminación
En química orgánica, una reacción de eliminación es el proceso inverso a una reacción de adición. Es una reacción orgánica en la que dos sustituyentes son eliminados de una molécula, creándose también una insaturación, ya sea un doble o triple enlace, o un anillo. En el caso particular de que los dos grupos sean eliminados de un mismo centro el resultado sería un carbeno :CR2.[1]
Las reacciones de eliminación más importantes son aquellas en las que los dos grupos que se eliminan están situados en átomos adyacentes, dando lugar a una nueva insaturación en la forma de un alqueno, un alquino o un carbonilo.
Contenido
Eliminación bimolecular
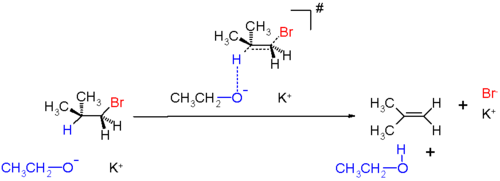
La eliminación bimolecular o E2 consiste en un mecanismo concertado de abstracción de un protón por parte de una base fuerte y la salida simultánea de un grupo saliente situado en β, en el carbono contiguo, formándose una insaturación (doble enlace).
Características generales:
- Proceso de eliminación en una sola etapa con, por tanto, un único estado de transición.
- Velocidad de reacción influida tanto por el sustrato, cuanto mejor grupo saliente más rápida, como la base. Cinética de segundo orden.
- Típica de haluros de alquilo, u otros derivados alquílicos con un buen grupo saliente, primarios, secundarios y terciarios. Aunque en el caso de primarios mejor si la base es impedida.
- Bases fuertes.
- El impedimento estérico favorece la E2 frente a la SN2.
- En el caso de derivados alquílicos primarios y secundarios competencia con SN2. Se favorece la eliminación frente a la sustitución con el empleo de bases impedidas (voluminosas).
- En el caso de derivados alquílicos terciarios E1 si la concentración de base es baja.
- La abstracción del protón y salida del grupo saliente tiene lugar en una conformación anti. Esta disposición permite un solapamiento más efectivo entre los dos orbitales sp³ que se están convirtiendo en p en el estado de transición para formar el nuevo enlace π, además también es más favorable que un estado de transición con una disposición sin eclipsada de mayor energía. Esto hace que sea una reacción estereoespecífica.
Eliminación unimolecular
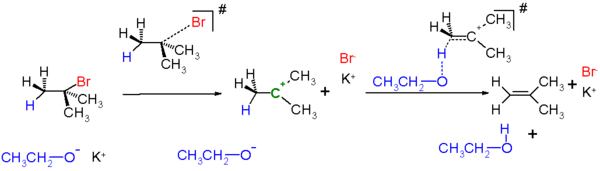
La eliminación unimolecular o E1 tiene lugar sobre derivados alquílicos secundarios o terciarios según un mecanismo de dos étapas. En la primera se produce la salida del grupo saliente para formar el carbocatión y a continuación la pérdida de un protón en β para formar un doble enlace.
Características generales:
- Proceso de eliminación en dos etapas, ionización y desprotonación.
- Ionización: Disociación del carbono y el grupo saliente para dar un carbocatión intermedio
- Desprotonación: Abstracción de un protón vecinal.
- Velocidad de reacción sólo dependiente del sustrato, primera etapa determinante de la velocidad. Cinética de primer orden.
- Reacción secundaria de la SN1, el nucleófilo actúa como base. Por tanto, al igual que la SN1, típica de sustratos terciarios y en algunos casos secundarios.
- Temperaturas altas favorecen la E1 frente a la SN1.
- Medio básico, baja concentración de base si no E2, favorece la E1 sobre la SN1.
- Reacciones secundarias de transposición del carbocatión.
- Dada la falta de control, no tiene gran utilidad sintética.
Regioselectividad
En sustratos asimétricos, cuando la abstracción del hidrógeno en β se puede producir en más de un carbono, existe la posibilidad de la formación de distintos alquenos.
En lo que respecta a la regioselectividad la E2 sigue la regla de Saytzev cuando no existen impedimentos estéricos importantes, ni sustrato ni base ramificados. En este caso se forma mayoritariamente el alqueno más sustituido (más estable). En cambio cuando aumenta el impedimento estérico, ya sea por ramificación del sustrato y/o aumento del volumen de la base, sigue la regla de Hofmann, de tal modo que se forma mayoritariamente el alqueno menos sustituido (menos estable), debido a la desprotonación de la posición menos impedida (más accesible). En ambos casos el motivo es cinético, transcurriendo la reacción por el estado de transición de menor energía.
En el caso de compuesto cíclicos el requisito que la E2 transcurra de forma estereoespecífica anti puede también jugar un papel importante en la regioselectividad, ya que los grupos que se eliminan deben estar situados en axial para que pueda tener lugar la reacción.
La E1 generalmente sigue la regla de Saytzev.
Referencias
- ↑ IUPAC Compendium of Chemical Terminology, Electronic version, http://goldbook.iupac.org/E02038.html.
Bibliografía
- K. Peter C. Vollhardt (1994). Química Orgánica. Barcelona: Ediciones Omega S.A.. ISBN 84-282-0882-4.
Categorías: Reacciones químicas orgánicas | Mecanismos de reacción
Wikimedia foundation. 2010.