- Oxalato (química)
-
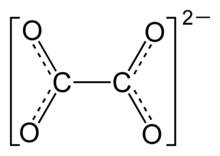
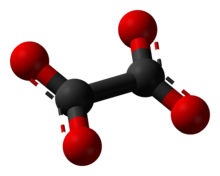
Los oxalatos son sales o ésteres del ácido oxálico. Las sales tienen en común el anión C2O42−, también escrito como (COO)22−, los ésteres tienen en común el esquema estructural R-O2CCO2R'.
Contenido
Propiedades
Se trata de sustacias habitualmente incoloras, reductoras y tóxicas; son tóxicas debido a que en presencia de iones de calcio forman el oxalato de calcio, CaC2O4, una sal muy poco soluble. De esta manera, por una parte se elimina el calcio como elemento esencial del organismo, y por otra parte si cristaliza formando un cálculo puede obstaculizar los conductos renales.
Las piedras renales también suelen ser formadas (al menos en parte) por oxalato cálcico. A los pacientes afectados de riñón se les recomienda uan dieta pobre en oxalato (poco té, pocas espinacas o ruibarbo).
Frente a cationes polivalentes, el ion oxalato suele actuar como ligando quelatante.
Su acumulación en ciertos órganos provoca la oxalosis.
Síntesis
Los oxalatos se forman por neutralización del ácido oxálico con la base correspondiente o por intercambio del catión. Así se puede obtener el oxalato potásico a partir del ácido oxálico y del hidróxido potásico:
HO2CCO2H + 2 KOH -> KO2CCO2K + 2 H2O
Los ésteres del ácido oxálico pueden obtenerse con las reacciones clásicas de esterificación a partir del ácido o del cloruro de oxalíl.
Usos
El oxalato potásico se encuentra en las formulaciones de algunos quitamanchas. Actúa complejando el hierro que puede estar presente.
El oxalato de hierro(III) (K3[Fe(O2CCO2)3 es una sustancia fotosensible. Expuesto a la luz, el hierro se reduce a hierro(II) y una parte del oxalato se oxida a dióxido de carbono (CO2). Los iones de hierro(II) reaccionan con hexacianoferato de hierro(II) (K3[Fe(CN)6) para dar un precipitado de azúl prusiano. Esta reacción fue utilizada en el pasado para hacer fotocopias. Actualmente ha sido sustituida por la xerotipía.
En la química analítica clásica se utiliza la reacción del oxalato con los iones de calcio para la determinación de estos.
Referencias
Enlaces externos
 Wikimedia Commons alberga contenido multimedia sobre Oxalato (química)Commons
Wikimedia Commons alberga contenido multimedia sobre Oxalato (química)Commons- Oxalato.com - Información sobre el oxalato
Categorías:- Compuestos orgánicos
- Grupos funcionales
- Oxalatos
- Oxoaniones
Wikimedia foundation. 2010.