- Acil-CoA deshidrogenasa
-
Acil-CoA deshidrogenasa de cadena muy larga HUGO 92 Símbolo ACADVL Datos genéticos Locus Cr. 17 p13-17p11 Bases de datos Entrez 37 OMIM 609575 PDB 2UXW RefSeq NM_000018 UniProt P49748 Acil-CoA deshidrogenasa de cadena larga HUGO 88 Símbolo ACADL Datos genéticos Locus Cr. 2 q34-q35 Bases de datos Número EC 1.3.99.13 Entrez 33 OMIM 609576 RefSeq NM_001608 UniProt P28330 Acil-CoA deshidrogenasa de cadena media HUGO 89 Símbolo ACADM Datos genéticos Locus Cr. 1 p31 Bases de datos Número EC 1.3.99.3 Entrez 34 OMIM 607008 PDB 1EGD RefSeq NM_000016 UniProt P11310 Butiril-CoA deshidrogenasa HUGO 90 Símbolo ACADS Datos genéticos Locus Cr. 12 q24.31 Bases de datos Número EC 1.3.99.2 Entrez 35 OMIM 606885 PDB 2VIG RefSeq NM_000017 UniProt P16219 Acil-CoA deshidrogenasa de cadena corta y ramificada 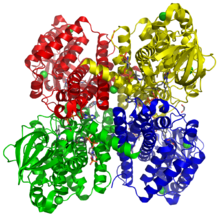
Diagrama de la acil-CoA deshidrogenasa de cadena corta ramificada humana formando complejo con FAD y coenzima A. PDB 2JIFHUGO 91 Símbolo ACADSB Datos genéticos Locus Cr. 10 q25-q26 Bases de datos Número EC 1.3.99.3 Entrez 36 OMIM 600301 PDB 2JIF RefSeq NM_001609 UniProt P45954
Las acil-CoA deshidrogenasas son enzimas que intervienen en la primera de las cuatro reacciones que constituyen la β-oxidación, la principal ruta metabólica de oxidación de los ácidos grasos. En la clasificación de las enzimas corresponde al grupo de las oxidorreductasas.Las acil-CoA deshidrogenasas catalizan la deshidrogenación de los carbonos 2 y 3 (α y β, respectivamente) de un acil-CoA graso, con lo que se forma un doble enlace entre dichos carbonos, según la reacción:

El acil-CoA graso se oxida al perder dos átomos de hidrógeno, que son captados por el FAD que se reduce a FADH2. El FAD está unido covalentemente a la enzima y actúa como cofactor.Existen al menos cinco enzimas diferentes que catalizan esta reacción, cada uno con especificidades que varían según la longitud de la cadena de los ácidos grasos:[1]
- Acil-CoA deshidrogenasa de cadena muy larga (ACADVL). Está asociada a la membrana interna de la mitocondria y actúa sobre los acil-CoA grasos de C-12 a C-24.
- Acil-CoA deshidrogenasa de cadena larga (ACADL). Parece que está implicada principalmente con la oxidación de ácidos grasos ramificados, como el 2-metilpalmitil CoA.
- Acil-CoA deshidrogenasa de cadena media (ACADM). Su máxima actividad es para los acil-CoA grasos de C-6 y C-8.
- Acil-CoA deshidrogenasa de cadena corta (ACADS). Su orden de preferencencia es C-4 > C-6 > C-8.
- Acil-CoA deshidrogenasa de cadena corta y ramificada (ACADSB).
Otros tipos son: ACAD8, ACAD9, ACAD10 y ACAD11.
Contenido
Tipos enzimáticos
ACADVL
La enzima Acil-CoA deshidrogenasa de cadena muy larga o ACADVL es activa con ésteres de ácidos grasos de cadena larga o cadena muy larga como palmitoil-CoA, miristoil-CoA y estearoil-CoA. Puede acomodar sustratos con longitudes de hasta 24 carbonos pero muestra una actividad muy pequeña para sustratos de menos de 12 carbonos. Esta enzima esta situada en la membrana interna mitocondrial y es un homodímero.
La deficiencia en ACADVL es una enfermedad recesiva autosomal. Es clínicamente heterogénea con tres fenotipos principales:
- Severa durante la infancia: Aparición temprana y alta mortalidad.
- Media durante la infancia: Aparición más tardía con hipoglucemia, baja mortalidad y raramente se presenta con una cardiomiopatía asociada.
- Durante la edad adulta: Se presenta con rabdomiólisis y mioglobinuria.
ACADL
La enzima Acil-CoA deshidrogenasa de cadena larga o ACADL EC 1.3.99.13 está situada en la matriz mitocondrial y es un homotetrámero. La deficiencia en ACADL causa hipoglucemia.
ACADM
La enzima Acil-CoA deshidrogenasa o ACADM EC 1.3.99.3 está situada en la matriz mitocondrial, es específica para cadenas acil-CoA de 4 a 16 carbonos y es un homotetrámero que interacciona con la flavoproteína de transferencia de electrones heterodimérica.
La deficiencia en ACADM es una enfermedad recesiva autosomal que causa hipoglucemia, disfunción hepática y encefalopatía, resultando frecuentemente en muerte durante la infancia. La frecuencia de la enfermedad es de 1 entre 13,000.
ACADS
La enzima Butiril-CoA deshidrogenasa o ACADS EC 1.3.99.2 está situada en la matriz mitocondrial y es un homotetrámero. La deficiencia en ACADS es una enfermedad recesiva autosomal que causa acidosis aguda, debilidad muscular en niños y una forma de miopatía realacionada con el almacenamiento de grasas.
ACADSB
La enzima Acil-CoA deshidrogenasa de cadena corta ramificada o ACADSB tiene su máxima actividad con derivados acil-CoA de cadena corta y ramificada como (s)-2-metilbutiril-CoA, isobutiril-CoA y 2-metilhexanoil-CoA, así como con derivados acil-CoA de cadena corta no ramificada como butiril-CoA y hexanoil-CoA. Puede también utilizar valproil-CoA como sustrato jugando por tanto un rol en el control del flujo metabólico del ácio valproico. Esta enzima esta situada en la matriz mitocondrial y es un homotetrámero.
La deficiencia en ACADSB es una enfermedad recesiva autosomal que consiste en un defecto en el catabolismo de la L-isoleucina que está caracterizado por un incremento en la sangre y en la orina de la 2-metilbutirilglicina y de la 2-metilbutirilcarnitina. Los individuos afectados tienen ataques de apoplejía y retraso psicomotor como principales síntomas.
Deficiencias genéticas de las acil-CoA deshidrogenasas
La deficiencias genéticas en las acil-CoA deshidrogenasas son un grupo de enfermedades hereditarias que se transmiten de manera autosómica recesiva. Cualquiera de las enzimas mencionadas puede verse afectada. La deficiencia en la MCAD se considera uno de los errores metabólicos más comunes y es posible que esté detrás de muchos casos de muerte súbita del recién nacido;[1] esta alteración se manifiesta antes de los dos años de vida y después de un período de ayuno de más de doce horas; sus síntomas más frecuentes son vómitos, letargia y a veces coma, hipoglucemia y aciduria.
Referencias
- ↑ a b Devlin, T. M. 2004. Bioquímica, 4ª edición. Reverté, Barcelona. ISBN 84-291-7208-4
Enlaces externos
Categorías:- Genes del cromosoma 17
- Genes del cromosoma 2
- Genes del cromosoma 1
- Genes del cromosoma 12
- Genes del cromosoma 10
- Oxidorreductasas
Wikimedia foundation. 2010.
