- Citoesqueleto
-
El citoesqueleto es un entramado tridimensional de proteínas que provee soporte interno en las células, organiza las estructuras internas de la misma e interviene en los fenómenos de transporte, tráfico y división celular. En las células eucariontas, consta de microfilamentos, filamentos intermedios y microtúbulos, mientras que en las procariontas está constituido principalmente por las proteínas estructurales FtsZ y MreB. El citoesqueleto es una estructura dinámica que mantiene la forma de la célula, facilita la movilidad celular (usando estructuras como los cilios y los flagelos), y desempeña un importante papel tanto en el tráfico intracelular (por ejemplo, los movimientos de vesículas y orgánulos) y en la división celular.
Luego del descubrimiento del citoesqueleto a principios de los años 80 por el biólogo Keith Porter, el Dr. Donald Ingber consideró que desde un punto de vista mecánico, la célula se comportaba de manera similar a estructuras arquitectónicas denominadas estructuras de tensegridad.
Contenido
El citoesqueleto eucariótico
El citoesqueleto es una estructura intracelular compleja importante que determina la forma y el tamaño de las células, así como se le requiere para llevar a cabo los fenómenos de locomoción y división celulares[2]. Además, en el citoesqueleto radica el control del movimiento intracelular de organelos y permite una organización adecuada para que se lleven a cabo los eventos metabólicos requeridos. La estructuración compleja del citoesqueleto está basada en la interacción de un conjunto de proteínas, las cuales se asocian y forman una red intracelular tridimensional. Es la complejidad de la red tridimensional lo que favorece los fenómenos indicados e incluso el que las células tengan la capacidad de adherirse al medio extracelular, así como el que interactúen y se comuniquen entre ellas. Gracias a tales fenómenos, en el citoesqueleto radica la efectividad con la que las células responden al microambiente en el cual se encuentren.
El citoesqueleto de las células eucariotas está basado principalmente en tres tipos de filamentos citoesqueléticos: microfilamentos, filamentos intermedios y microtúbulos. Estos filamentos son largos y se polimerizan por cada uno de sus monómeros. Los monómeros de cada filamento están codificados por los genes y las células los sintetizan de forma constitutiva en niveles basales de expresión de proteínas. Sin embargo, la estructura tridimensional que forman los polímeros al constituir el citoesqueleto no está codificada por el material genético y por lo consiguiente, se transmite de una célula a otra por ser parte de su citoplasma. Sin embargo, el citoesqueleto se considera que perdurará siempre por que funciona como una “memoria celular”, esto porque es capaz de almacenar e integrar todas las interacciones que se hayan sucedido en el, durante su interacción con el microambiente que se le presente y lo cual influirá en el futuro comportamiento celular como lo indicaron Fletcher y Mullins en el 2010.[1]
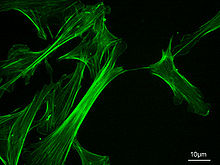
Microfilamentos (actina)
Los microfilamentos tienen un diámetro de unos 7 nm ó 5 nanometro Están formadas por una proteína globular llamada actina que puede presentarse de dos formas:
- Actina no polimerizada (G actina): la actina se encuentra asociada a la profilina que evita su polimerización. Representa la mitad de la actina de la célula y es utilizada para polimerizar microfilamentos cuando es necesario.
- Actina polimerizada (F actina): es una doble hélice dextrógira de dos hebras de actina no polimerizada. Esta actina se puede encontrar asociada a otras proteínas:
- Proteínas estructurales: que permiten la unión de los filamentos de actina
- Proteínas reguladoras: la más importante es la miosina que permite la contracción muscular al permitir que la actina se desplace sobre ella.
Las funciones de los microfilamentos de actina son la contracción muscular, la formación de pseudópodos, el mantenimiento de la morfología celular y, en la citocinesis de células animales, forma un anillo contráctil que divide la célula en dos(descubridor;eder mautino angeles)
de: juan kanguzz
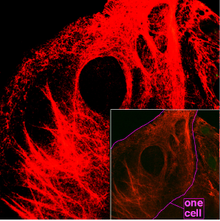
Filamentos intermedios
Son filamentos de proteína fibrosa que van de 8 a 11nm, son los componentes del citoesqueleto más estables, dando soporte a los orgánulos (por sus fuertes enlaces), y heterogéneos. Las proteínas que conforman estos filamentos, la citoqueratina, vimentina, neurofilamentos, desmina y la proteína fibrilar acídica de la glia, dependen del tejido en el que se hallen. Su función principal es la organización de la estructura tridimensional interna de la célula (por ejemplo, forman parte de la envuelta nuclear y de los sarcómeros). También participan en algunas uniones intercelulares (desmosomas).
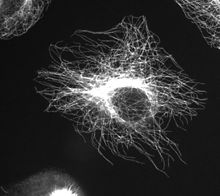
Microtúbulos
Los microtúbulos son estructuras tubulares de 25 nm de diámetro que se originan en los centros organizadores de microtúbulos y que se extienden a lo largo de todo el Citoplasma. Se pueden polimerizar y despolimerizar según las necesidades de la célula. Se hallan en las células eucariotas y están formados por la polimerización de un dímero de dos proteínas globulares, la alfa y la beta tubulina. Cada microtúbulo está compuesto de 13 protofilamentos formados por los dímeros de tubulina. Intervienen en diversos procesos celulares que involucran desplazamiento de vesículas de secreción, movimiento de orgánulos, transporte intracelular de sustancias, así como en la división celular (mitosis y meiosis), ya que forman el huso mitótico. Además, constituyen la estructura interna de los cilios y los flagelos. Los microtúbulos son más flexibles pero más duros que la actina.
El citoesqueleto procariótico
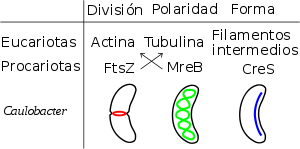 Elementos del citoesqueleto de Caulobacter crescentus. En la figura, estos elementos procarióticos se relacionan con sus homólogos eucariotas y se hipotetiza su función celular.[2] Debe tenerse en cuenta que la función de la pareja FtsZ-MreB se invirtió durante la evolución al convertirse en tubulina-actina.
Elementos del citoesqueleto de Caulobacter crescentus. En la figura, estos elementos procarióticos se relacionan con sus homólogos eucariotas y se hipotetiza su función celular.[2] Debe tenerse en cuenta que la función de la pareja FtsZ-MreB se invirtió durante la evolución al convertirse en tubulina-actina.
En el pasado se creía que el citoesqueleto era una característica única de las células eucarióticas, pero desde entonces se han encontrado homólogos bacterianos a las principales proteínas del citoesqueleto eucariota.[3] A pesar de que las relaciones evolutivas son tan distantes que no se pueden inferir analogías a partir de las secuencias de aminoácidos, la similitud de la estructura tridimendional, las funciones en el mantenimiento de la forma y en la polaridad de las células proporcionan pruebas sólidas de que los citoesqueletos eucariotas y procariotas son realmente homólogos.[4]
FtsZ
FtsZ fue la primera proteína del citoesqueleto procariota en ser identificada. Al igual que la tubulina, FtsZ forma filamentos en presencia de GTP, pero estos filamentos no se agrupan en microtúbulos. Durante la división celular, FtsZ es la primera proteína que se desplaza al lugar de la división y es esencial para organizar a las proteínas que sintetizan la nueva pared celular en las células que se dividen.
MreB y ParM
Las proteínas procariotas similares a la actina, tales como MreB, están involucradas en el mantenimiento de la forma celular. Estas proteínas forman una red helicoidal debajo de la membrana celular que guía a las proteínas que participan en la biosíntesis de la pared celular. Todas las bacterias no esféricas tienen genes que codifican este tipo de proteínas.
Algunos plásmidos codifican un sistema de particionado que envuelve una proteína similar a la actina, denominada ParM. Los filamentos de ParM exhiben una inestabilidad dinámica y pueden particionar los plásmidos de ADN durante la división celular en un mecanismo análogo al utilizado por los microtúbulos durante mitosis de los eucariotas.
Crescentina
La bacteria Caulobacter crescentus contiene una tercera proteína,llamada crescentina, que está relacionada con los filamentos intermedios de las células eucarióticas. La crescentina también participa en el mantenimiento de la forma celular, pero el mecanismo actualmente es poco claro.[5]
El citoesqueleto, la tensegridad y la mecanotransducción celular
El citoesqueleto es dinámico y no por ello pierde la capacidad del mantenimiento de la forma, la funcionalidad y la estructura de la red tridimensional que lo conforma. Uno de los sitios más recomendables de la WEB para observar mediante visualización científica lo que se ha generado al respecto, y para el cual se aplica el conocimiento generado almomento para el interior de una célula y su relación con la membrana plasmática, es el sitio de XVIVO. En este sitio si uno accede a "The inner life of the cell" [3] uno puede quedar maravillado de lo que podría suceder al interior de una células y la relación que con ello tiene el citoesqueleto. Con base a este sitio es claro que uno puede imaginarse que el citoesqueleto es una estructura intracelular que continuamente está sujeta a propiedades biomecánicas relacionadas con tensión y compresión, las cuales son medibles y explicables mediante las leyes de la física relacionadas con la biomecánica. El balance entre estas propiedades le confieren a la célula una integridad tensional (conocida en el idioma inglés como “tensegrity”) y la cual se basa en lo visualizado en 1993 por el Dr. Donald Ingber[4], científico que trasladó el concepto arquitectónico (en el cual se le conoce como tensegridad) al ámbito intracelular y que se mantiene vigente en nuestros días. En este sentido, una forma de ampliar visualmente la influencia de los fenómenos de tensión, longitud, rigidez, compresión producidas por las proteínas del citoesqueleto actina y tubulina, así como de la matriz extracelular y las integrinas, es lo presentado en la página WEB del Children´s Hospital Boston denominado "Tensegrity in a Cell" [5]; sitio en el cual las animaciones producidas de manera interactiva por la influencia de las fuerzas indicadas generan cambios en las células y los cuales pueden ser comparados con imágenes obtenidas mediante el microscopio de fluorescencia.
La estructuración y la dinámica del citoesqueleto dependen de la forma en que la célula se relaciona con la matriz extracelular y tal relación es lo que determina la biomecánica de las células. Un ejemplo de ello podría ser la dinámica con la que las células ciliadas se presentan ante su entorno como lo propuesto para las células flama de los protonefridios del céstodo Taenia solium[6] Recientemente, Hersen y Ladoux[7] han hecho referencia a que la mecanobiología es un campo emergente que investiga como las células vivas sienten y responden a las fuerzas mecánicas de su entorno. Su comentario hace referencia a que las células están continuamente percatándose de las fuerzas que se suceden a su alrededor aún cuando se encuentran en migración. Tales fuerzas inducen que las células no sólo sufran deformaciones sino que también inducen a que se presenten fenómenos como señalización por adhesión y reorganización del citoesqueleto. Estos fenómenos, en referencia a la estrategia experimental que publicaron Delanoë-Ayari y colaboradores,[8] indican que una célula tiene la capacidad de sentir tanto las fuerzas horizontales como las verticales que se presentan durante su desplazamiento y que muestran la importancia que juega la interacción tridimensional entre las células y la matriz extracelular. Las características mecánicas de la matriz extracelular (rigidez y deformabilidad) son factores importantes que influyen en la conducta y la dinámica de las células [6] tales como la diferenciación, la proliferación, la sobrevivencia, la polaridad y la migración.[9] La mecanotransducción, que se ha establecido como la transformación de fuerzas físicas en señales químicas, es capaz de generar una morfogénesis de un epitelio y ello se puede dar por la generación de modificaciones postransduccionales como la fosforilación de filamentos intermedios como lo demostrado recientemente con el estudio del nematodo Caenorhabditis elegans([10] ). Esto resulta un aspecto interesante de la dinámica de la reestructuración del citoesqueleto, ya que se ha encontrado que con los estudios que se efectuaron se muestran que los filamentos intermedios también se mueven y no sólo son de soporte y estructura celular. Esto abre un universo importante de como en un ambiente tisular las células contráctiles pueden ejercer influencia en las células de epitelio para que se diferencíen y con ello, se favorezcan aspectos de regeneración tisular o diseminación de procesos cancerosos.
La tensión con que se presenta el citoesqueleto de una célula, en un momento dado, está influenciado por la dinámica celular y la forma de su núcleo. Cualquier aspecto que induzca cambios en las fuerzas intracelulares que ejercen los componentes del citoesqueleto, derivados de su interacción con el medio extracelular, induce a que también se den cambios en la forma de los núcleos celulares.[11] La constitución del núcleo celular, relacionada con su viscoelasticidad, puede tener un papel determinante en las interacciones biomecánicas que se dan entre el núcleo, el citoesqueleto y la matriz extracelular. Además, sus propiedades viscoelásticas podrían tener importantes implicaciones en el estudio de la transducción de señales mecánicas. Se sabe que el núcleo tiene comportamiento como un sólido viscoelástico y por ello presenta propiedades distintas a las del citoplasma. Por lo consiguiente, es de esperarse que cualquier deformación que sufra, así como las propiedades mecánicas que presenta núcleo podrían estar influenciadas por el estado de tensión-compresión al que esté sometida una célula.[12] Los núcleos celulares también tienen una dinámica propia debida a su composición; cuando una célula va de un lado a otro o bien, pasa a través de un diámetro menor al suyo, la deformación del núcleo también se presenta acorde al que presenta la célula completa. El tamaño y la forma de los núcleos celulares es variable y depende del tipo celular. Su dinámica está asociada a la del citoesqueleto y por lo consiguiente, la composición del nucleoesqueleto está intrínsicamente conectado al citoesqueleto. De hecho se ha indicado que la plasticidad del núcleo celular en las células cancerosas es una determinante para que éstas se diseminen[13]
Mecanotransducción es un término que implica que las fuerzas mecánicas aplicadas a las células se transforman en sucesos bioquímicos relevantes y que debido a ellos, se generan diferentes procesos asociados al desarrollo, la fisiología y la patología.[14] Según los autores de la revisión citada, la mecanotransducción celular es un campo de estudio de rápido avance en la investigación científica actual. La relación que el citoesqueleto guarda con la mecanotransducción es estrecha: las células son materiales deformables que basan su forma y tamaño en el citoesqueleto y por lo consiguiente, cualquier fuerza que las afecte genera cambios que se traducen en distintas actividades celulares. Según lo que se ha establecido, son las propiedades de viscoelasticidad del citoesqueleto lo que define sus propiedades mecánicas y que gracias a ellas tenga la plasticidad requerida. Sin embargo, esto es un tema aún controversial. La demostración de como se presenta la mecanotransducción es un reto tecnológico muy interesante ya que son varias las formas con que este fenómeno puede ser evaluado a nivel de las células y van desde la compresión de membranas, el corte por estres, el uso de pinzas ópticas, la aplicación de fuerzas magnéticas, el uso del microscopio de fuerza atómica y la aspiración con micropipetas entre otras[15]
Papel de la mecanotransducción en la invasión por patógenos
Según Hoffman et al[16] el prendido y apagado de la mecanotransducción (del inglés "switch-like model") está integrado por tres fenómenos: la mecanosensación, la mecanotransmisión y la mecanorespuesta. Cuando las células responden a estímulos mecánicos tanto externos como internos, un conjunto molecular denominado mecanosensor sufre cambios conformacionales que le permite a las células el detectar tales estímulos. Luego estos estímulos son transmitidos al interior celular a través de los largos filamentos del citoesqueleto y esto se refiere al fenómeno de mecanotransmisión. Las señales generadas por estos estímulos se transducen en la activación de señales intracelulares en las que participan segundos mensajeros, con lo que finalmente se genera una mecanorespuesta celular. Hay que considerar que estos fenómenos se presentan de forma secuencial en un intervalo de tiempo del orden de cientos de milisegundos y que pueden ser acelerados o retrasados por cambios en la intensidad y la frecuencia de las fuerzas, así como de las condiciones del microambiente que los originaron. Un ejemplo de la importancia de la mecanotransducción en la invasión por patógenos es la propuesta para hongos como Candida albicans y Magnaporthe grisea hecha por Kumamoto en 2008.[17] Un trabajo muy interesante en el que se induce una fuerza magnética a trofozoítos de la ameba Entamoeba histolytica, los cuales previamente se activaron por la fagocitosis de perlitas magnéticas recubiertas con proteínas humanas séricas, muestra que la mecanotransducción generada induce a que la célula modifique su migración hacia un solo sitio y que la mecanosensación se dá por activación de la cinasa de fosfatidilinositol y la reestructuración de la actina.[18] Según estos autores, la mecanotransducción inducida en estos patógenos, que orienta la dirección de migración de ellos, podría estar relacionado con cambios en su virulencia, lo cual podría ser determinante en la invasión de los tejidos humanos infectados. La mecanotransducción también podría ser relevante para el comportamiento de los patógenos durante su interacción con las células de sus hospederos; recientemente, mediante la evaluación de la adhesión de protozoarios de Gardia lamblia a vidrio por marcaje fluorescente in vivo del disco suctor y de los flagelos ventrales, se encontró que la fuerza con la que el disco suctor de estos parásitos se adhiere a su sustrato es tan fuerte, lo cual podría ser suficiente para evitar que el parásito se despegue. Esta estructura celular de G. lamblia tiene un diseño tal como una copa de succión que genera un vacío gracias al cual se adhiere firmentemente al tejido intestinal. Esto si se tradujese a lo que el parásito hace con el epitelio intestinal, podría dar una explicación de porque aún cuando el intestino entre en peristalsis, este tipo de protozoarios permanezcan adheridos.[19]
El citoesqueleto durante la migración celular
La dinámica del citoesqueleto es crucial para que las células vayan de un lugar a otro como se ilustra con la serie de imágenes y videos obtenidos experimentalmente bajo la excelente composición interactiva concebida por el Dr. Vic Small y que se ha denominado como un viaje visual de la motilidad celular [7]. En este sitio uno puede percatarse de lo interesante que resultan tanto la forma como el tamaño que adoptan las células en un momento determinado durante su migración y que aún así de haber desplegado tal dinámica y reorganización, las células no pierden la capacidad de regresar a su estado original cuando éstas se encuentran en reposo. Aún así, el citoesqueleto en la célula en reposo es dinámico, no se detiene porque son perennes las funciones básicas de tráfico y movimiento intracelulares. Como ya había sido descrito anteriormente, al hacer referencia a la vida interior de las células [8] y lo que de manera animada se presenta en el sitio; una célula se desplaza de un lugar a otro, interacciona con otras células y durante estos fenómenos puede cambiar radicalmente su forma y tamaño pero no deja de tener una dinámica intracelular que le ofrece el citoesqueleto. Un excelente ejemplo de la migración celular inducida por sustancias que atraen células y que provienen de otras dañadas, con fines de reparación de estas últimas, es la migración de neutrófilos luego de su adhesión desde los sinusoides hepáticos hacia los focos de hepatocitos dañados durante el fenómeno de inflamación estéril[20] y del cual se puede observar un interesante video en la sección VideoLab[9] de la revista Science. En el video, los neutrófilos teñidos con fluorescencia en color verde, sufren modificaciones en su forma y tamaño durante su migración hacia el foco de hepatocitos dañados (teñidos fluorescentemente en color rojo) a los cuales intentan restaurar. Previo a su migración, los neutrófilos se encuentran adheridos a las paredes de los sinusoides hepáticos (teñidos fluorescentemente en color azul) y cambian su forma y tamaño al dirigirse hacia el foco mencionado.
Con la tecnología microscópica actual es posible observar y videofilmar la manera en que el citoesqueleto se reestructura durante la migración celular. Los recursos tecnológicos son diversos [10] y ellos permiten la visualización desde el nivel micrométrico hasta el nanométrico [11]. Las necesidades de conocer que eventos se suceden en el interior de una célula durante su migración es una preocupación que, por su estudio, se espera que puedan ser mejorados otros aspectos de la biología celular pocos conocidos. Un ejemplo de ello es la suma de esfuerzos de investigadores que estudian la migración celular [12]. Debido a los estudios que se han realizado en células que migran, se ha demostrado que ellas se desplazan mediante la continua interacción con la matriz extracelular que les rodea mediante la interacción continua con focos de adhesión o puntos focales. La forma en que las células interaccionan con dicha matriz, depende de la composición y forma de la misma, por lo consiguiente las células adoptan la forma del medio en el que se encuentran desplazando, como se demostró mediante videomicroscopía y el uso de marcadores fluorescentes (Doyle et al, 2009).[21] El material suplementario asociado al trabajo de estos autores, es una muestra fantástica de como las células adquieren tal migración e incluso se puede observar al mismo tiempo (ver video 4 en relación a la migración de queratinocitos) como realizan sus movimientos intracelulares [13]
Referencias
- ↑ Fletcher DA y Mullins RD. Cell mechanics and the cytoskeleton. Nature. 463: 485-491. 2010
- ↑ Gitai, Z. (2005). «The New Bacterial Cell Biology: Moving Parts and Subcellular Architecture». Cell 120 (5): pp. 577-586. doi:. http://linkinghub.elsevier.com/retrieve/pii/S0092867405001935.
- ↑ Shih YL, Rothfield L (2006). «The bacterial cytoskeleton». Microbiol. Mol. Biol. Rev. 70 (3): pp. 729–54. doi:. PMID 16959967. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pubmed&pubmedid=16959967.
- ↑ Michie KA, Löwe J (2006). «Dynamic filaments of the bacterial cytoskeleton». Annu. Rev. Biochem. 75: pp. 467–92. doi:. PMID 16756499. http://www2.mrc-lmb.cam.ac.uk/SS/Lowe_J/group/PDF/annrev2006.pdf.
- ↑ Charbon, G., Cabeen, M.T. y Jacobs-Wagner, C. (2009). «Bacterial intermediate filaments: in vivo assembly, organization, and dynamics of crescentin». Genes & development (Cold Spring Harbor Lab) 23 (9): pp. 1131.
- ↑ Valverde-Islas L, Arrangoiz E, Vega E, Robert L, Villanueva R, et al. Visualization and 3D reconstruction of flame cells of Taenia solium (Cestoda). PLoS ONE 6(3): e14754. doi:10.1371/journal.pone.0014754 [1]
- ↑ Pascal Hersen and Benoit Ladoux. Push it, pull it. Nature 470: 340-341. 2011
- ↑ Delanoë-Ayari H, Rieu JP and Sano M. Phys. Rev. Lett. 105, 248103. 2010
- ↑ Hynes RO. The extracellular matrix not just pretty fibrils. Science. 27 (236): 1216-1219. 2009.
- ↑ Zhang H, Landmann F, Zahreddine H, Rodriguez D, Koch M and Labouesse M. A tension-induced mechanotransduction pathway promotes epithelial morphogenesis. Nature 471; 99-103. 2011.
- ↑ Sims JR, Karp S and Ingber DE. J. Cell Sci. 103; 1215-1222. 1992
- ↑ Guilak F, Tedrow JR, Burgkart R. Biochem. Biophys. Res. Commun. 269; 781-786. 2000
- ↑ Friedl P, Wolf K, Lammerding J. Nuclear mechanics during cell migration. Curr. Op. Cell Biol. 23: 55-64. 2011.
- ↑ Hoffman BD, Grashoff C, Schwartz MA. Dynamic molecular processes mediate cellular mechanotransduction. Nature 475 (21) 316. 2011.
- ↑ Huang H, Kamm RD, Lee RT. Cell mechanics and mechanotransduction: pathways, probes, and physiology. Am J Physiol Cell Physiol 287: C1-C11. 2004
- ↑ Hoffman BD, Grashoff C, Schwartz MA. Dynamic molecular processes mediate cellular mechanotransduction. Nature 475 (21) 316. 2011.
- ↑ Kumamoto CA. Molecular mechanisms of mechanosensing and their roles in fungal contact sensing. Nat Rev Microbiol. 2008 Sep;6(9):667-73
- ↑ Rivierea C, Marion S, Guillen N, Bacria JC, Gazeaua F, Wilhelm C. Signaling through the phosphatidylinositol 3-kinase regulates mechanotaxis induced by local low magnetic forces in Entamoeba histolytica. Journal of Biomechanics 40: 64–77. 2007.
- ↑ House SA, Richter DJ, Pham JK, Dawson SC, 2011 Giardia Flagellar Motility Is Not Directly Required to Maintain Attachment to Surfaces. PLoS Pathog 7(8): e1002167. doi:10.1371/journal.ppat.1002167
- ↑ McDonald B, Pittman K, Menezes GB, Hirota SA, Slaba I, Waterhouse CCM, Beck PL, Muruve DA and Kubes P. Intravascular danger signals guide neutrophiles to sites of sterile inflammation. Science 3330(6002): 362-366. 2010.
- ↑ Doyle AD, Wang FW, Matsumoto K and Yamada KM. One-dimensional topography underlies three-dimensional fibrillar cell migration. JCB. 184(4): 481-490. 2009
Wikimedia foundation. 2010.