- Fenilalanina
-
Fenilalanina
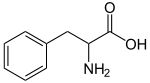
 Fenilalanina
FenilalaninaNombre (IUPAC) sistemático Ácido 2-amino-3-fenilpropanoico General Símbolo Phe, F Fórmula molecular C9H11NO2 Identificadores Número CAS 63-91-2 PubChem Propiedades físicas Densidad n/d Masa molar 165,19 g/mol Punto de fusión 556 K (282,85 °C) Punto de ebullición K (-273,15 °C) Propiedades químicas Acidez (pKa) 1,83; 9,13 Solubilidad en agua n/d Bioquímica Familia Aminoácido Esencial Sí Codón UUC, UUU Punto isoeléctrico (pH) 5,48 Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasLa fenilalanina es un aminoácido. Se encuentra en las proteínas como L-fenilalanina (LFA), siendo uno de los nueve aminoácidos esenciales para humanos. La fenilalanina es parte también de muchos psicoactivos.
Contenido
Bioquímica
La cadena lateral característica de este aminoácido contiene un anillo bencénico, y es por tanto uno de los aminoácidos aromáticos, su uso excesivo produce efectos laxantes, junto con la tirosina y el triptófano. La L-fenilalanina se puede transformar, por medio de una reacción catalizada por la enzima fenilalanina hidroxilasa, en tirosina. La L-fenilalanina es también el precursor de las catecolaminas como la L-dopa (L-3,4-dihidroxifenilalanina), la norepinefrina y la epinefrina, a través de una etapa en la que se forma tirosina. Por otro lado, la L-fenilalanina se encuentra en la estructura de neuropéptidos como la somatostatina, vasopresina, melanotropina, encefalina, hormona adrenocorticotrópica (ACTH), angiotensina, sustancia P y colecistoquinina.
Fuentes de fenilalanina
La fenilalanina se encuentra principalmente en alimentos ricos en proteínas como la carne, pescado, huevos, productos lácteos y dulces. Asimismo se encuentra en muchas de las drogas psicotrópicas usadas habitualmente. La fenilalanina, debido a su anillo aromático no es edulcorante por si mismo, necesita estar unido al ácido aspártico para este cometido.
La fenilalanina es parte de la composición del aspartamo, un edulcorante artificial que se encuentra en alimentos dietéticos y es muy habitual en bebidas refrescantes; no se recomienda el consumo de fenilalanina por embarazadas ni pacientes fenilcetonúricos. Debido a la fenilcetonuria, normalmente los productos que contienen aspartamo llevan una advertencia en el etiquetado sobre la presencia de fenilalanina. Se ha visto que la fenilalanina tiene la habilidad única de bloquear ciertas enzimas, las encefalinasas en el sistema nervioso central, que normalmente se encargan de degradar las hormonas naturales parecidas a la morfina. Estas hormonas se llaman endorfinas y encefalinas y actúan como potentes analgésicos endógenos. La fenilalanina es efectiva como tratamiento para el dolor de espalda baja, dolores menstruales, migrañas, dolores musculares, de artritis reumatoide y de osteoartritis. Asimismo es usada en tratamientos antidepresivos.
Patologías
La enfermedad genética fenilcetonuria se debe a la carencia de la enzima fenilalanina hidroxilasa o de la dihidropterina reductasa (DPHR), y esta deficiencia hace que la fenilalanina se degrade en una ruta metabólica alterna hacia fenilpiruvato, un neurotóxico que afecta gravemente al cerebro durante el crecimiento y el desarrollo. Los efectos de la acumulación de este neurotóxico causan oligofrenia fenilpirúvica, caracterizada por un cociente intelectual inferior a 20.
Una deficiencia en el metabolismo de la fenilalanina puede producir alcaptonuria, una enfermedad hereditaria que causa orinas negruzcas y frecuentes cálculos renales.[1]
Referencias
- ↑ [MedlinePlus] (julio de 2007). «Alcaptonuria» (en español). Enciclopedia médica en español. Consultado el 11 de julio, 2008.
Categorías: Aminoácidos | Aminoácidos esenciales | Aminoácidos neutros no polares | Aminoácidos glucogénicos | Aminoácidos cetogénicos | Aminoácidos aromáticos | Fenetilaminas
Wikimedia foundation. 2010.
