- Cloruro de tionilo
-
Cloruro de tionilo 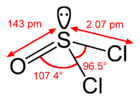
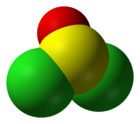
General Nombre IUPAC Cloruro de tionilo Otros nombres Oxicloruro sulfuroso
Dicloruro sulfuroso
Cloruro de sulfinilo
Óxido de sulfuro y cloruro
Dicloruro de tioniloFórmula molecular SOCl2 Masa molecular 118.97 g/mol Apariencia Incoloro a amarillo
Líquido olorosoNúmeo CAS 7719-09-7 Propiedades Densidad y Fase 1.638 g ml−1, líquido Solubilidad en agua Reactivo Punto de fusión −104.5 °C Punto de ebullición 76 °C Viscosidad 0.6 cP a ? °C Estructura Estructura molecular piramidal Momento dipolar 1.4 D Riesgos Clasifiación EU Corrosivo (C) NFPA 704 Frases R R14, R20/22, R29, R35 Frases S S1/2, S26, S36/37/39, S45 Punto Flash no inflamable Compuestos relacionados Otros aniones Bromuro de tionilo
Yoduro de tioniloCompuestos relacionados Dicloruro de sulfurilo
Oxicloruro de selenioExcepto donde se índice lo contrario, los datos se dan para materiales en sus condiciones estándar (a 25 °C, 100 kPa)
Exenciones y referenciasEl cloruro de tionilo es un compuesto inorgánico de fórmula SOCl2. El SOCl2 es un reactivo químico usado en las reacciones de cloración. Es un líquido transparente a presión y temperatura ambiente, que se descompone alrededor de 140 °C. A veces el SOCl2 es confundido con el dicloruro sulfurilo, SO2Cl2, pero las propiedades químicas de estos compuestos, S(IV) y S(VI), difieren significativamente.
Contenido
Propiedades y estructura
La molécula SOCl2 es piramidal, indicando la presencia de un par de electrones en el centro del S(IV): en contraste, el COCl2 es plana.
SOCl2 reacciona con agua liberando cloruro de hidrógeno y dióxido de azufre.
- H2O + O=SCl2 → 2 HCl + SO2
Dado que tiene una alta reactividad con el agua, el SOCl2 no se espera que se produzca en la naturaleza.
Uso industrial
El cloruro de tionilo se usa en las baterías de cloruro de litio-tionilo como el material activo positivo y el litio como el negativo. También es usado como reactivo para la producción de otros compuestos químicos o materiales.
En el uso militar, el cloruro de tionilo se utiliza en el "di-di", método de producción de agente nerviosos de la serie G.
Uso en química orgánica
El cloruro de tionilo es utilizado generalmente para convertir ácido carboxílicos[1] [2] y alcoholes[3] [4] en sus correspondientes acil cloruro y alquil cloruro respectivamente. Se prefiere a otros reactivos tales como el pentacloruro de fósforo porque los productos de la reacción del cloruro de tionilo, HCl y SO2, son gaseosos, simplificando la purificación del producto. El exceso de cloruro de tionilo puede ser eliminado por destilación.
El ácido sulfónico reacciona con el cloruro de tionilo para producir dicloruro de tionilo.[5] [6]
Reacciones varias
El cloruro de tionilo reacciona con la foramida primaria para formar isocianidas.[7]
Las amidas reaccionan con el cloruro de tionilo para formar "cloruro imidoyl". Sin embargo, las amidas primarias calentados con cloruro de tionilo continúan reaccionando para formar nitrilos.[8]
Síntesis
En la síntesis industrial más importante se lleva a cabo la reacción del trióxido de azufre y del dicloruro de azufre.[9]
Otros métodos incluyen:
- SO2 + PCl5 → SOCl2 + POCl3
- SO2 + Cl2 + SCl2 → 2 SOCl2
- SO3 + Cl2 + 2 SCl2 → 3 SOCl2
La primera de las tres reacciones anteriormente citadas también produce oxicloruro de fósforo, que se asemeja al cloruro de tionilo en muchas de sus reacciones.
Consideraciones de seguridad y toxicología
El SOCl2 es tóxico, corrosivo, y lacrimógeno. Peligroso por su inhalación y por contacto con la piel, mayor siendo oloroso.
La producción industrial está controlada bajo la Convención de Armas Químicas, donde aparece enumerada en la tabla 3 (son los productos químicos que se pueden utilizar como armas químicas tóxicas por sí mismos o utilizarlos en la fabricación de armas químicas pero que también tienen grandes aplicaciones industriales legítimas).
Referencias
- ↑ Rutenberg, M. y Horning, E. (1963). «1-METHYL-3-ETHYLOXINDOLE» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 4: pp. 620. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv4p0620.
- ↑ Allen, C.; Byers, J. y Humphlett W. (1963). «OLEOYL CHLORIDE» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 4: pp. 739. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv4p0739.
- ↑ Mondanaro, Kathleen y Dailey, William (1998). «3-CHLORO-2-(CHLOROMETHYL)-1-PROPENE» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 75: pp. 89. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=v75p0089.
- ↑ Krakowiak, Krzysztof y Bradshaw, Jerald (1998). «4-BENZYL-10,19-DIETHYL-4,10,19-TRIAZA-1,7,13,16-TETRAOXACYCLOHENEICOSANE (TRIAZA-21-CROWN-7)» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 9: pp. 34. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv9p0034.
- ↑ Weinreb, Steven; Chase, Charles; Wipf, Peter y Venkatraman, Srikanth (1998). «2-TRIMETHYLSILYLETHANESULFONYL CHLORIDE (SES-Cl)» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 75: pp. 161. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=v75p0161.
- ↑ Hazen, G.; Bollinger, F.; et ál. (1998). «4-DODECYLBENZENESULFONYL AZIDES» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 9: pp. 400. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv9p0400.
- ↑ Niznik, G.; Morrison, W. y Walborsky, H. (1998). «1-d-ALDEHYDES FROM ORGANOMETALLIC REAGENTS: 2-METHYLBUTANAL-1-d» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 6: pp. 751. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv6p0751.
- ↑ Krynitsky, John y Carhart, Homer (1963). «2-ETHYLHEXANONITRILE» (en inglés). Organic Syntheses (Nueva York: John Wiley & Sons) 4: pp. 436. ISSN 0078-6209. OCLC 01644392. http://www.orgsyn.org/orgsyn/prep.asp?prep=cv4p0436.
- ↑ Greenwood, Norman Neill; Earnshaw, Alan (1984), Greenwood, Norman Neill, ed. (en inglés), Chemistry of the Elements (primera edición), Pergamon Press, p. 820, ISBN 00-802-2056-8, http://books.google.com.ar/books?ei=8rcFTZbnI4P88Aaj8L2RDw&ct=result&id=OezvAAAAMAAJ&q=so2#search_anchor
Enlaces externos
- Usos de cloruro de tionilo en síntesis orgánica (en inglés)
- NIOSH Pocket Guide to Chemical Hazards
Categorías:- Cloruros
- Compuestos inorgánicos de azufre
Wikimedia foundation. 2010.

