- Ácido sórbico
-
Ácido sórbico
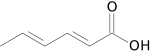
Nombre (IUPAC) sistemático Ácido (2E,4E)-hexa-2,4-dienoico General Otros nombres CC=CC=CC(O)O Fórmula semidesarrollada C6H8O2 Fórmula molecular n/d Identificadores Número CAS 110-44-1 Propiedades físicas Densidad 1.204 kg/m3; 0,001204 g/cm3 Masa molar 112.127 g/mol g/mol Punto de fusión 407,65 K (134,5 °C) Punto de ebullición 501,15 K (228 °C) Propiedades químicas Acidez (pKa) 4.76 a 25 °C Valores en el SI y en condiciones normales
(0 °C y 1 atm), salvo que se indique lo contrario.
Exenciones y referenciasEl ácido sórbico o ácido 2,4-hexadienoico es un compuesto orgánico natural empleado como conservante alimentario en su forma de sales minerales.[1] Posee de fórmula química C6H8O2. Debe su nombre a que fue aislado por primera vez en las frutas del género Sorbus (Sorbus aucuparia). El ácido se puede sintetizar por varios métodos diferentes. No debe confundirse con el ácido ascórbico (Vitamina C).
Contenido
Usos
El ácido sórbico así como parte de sus sales minerales (sorbatos), tales como el sorbato sódico, sorbato potásico y el sorbato cálcico, son empleados como agentes antimicrobianos en la industria alimentaria, más específicamente como agentes fungistáticos, es decir que reducen el desarrollo de las levaduras y de mohos en salmueras, mejorando así la vida de mercado del alimento. La duración de la estabilidad fungistática del ácido sórbico y de sus sales, está directamente relacionada con el porcentaje empleado del aditivo. La flora bacteriana se afecta solo ligeramente. El ácido sórbico por su baja constante de disociación puede ser usado en alimentos ácidos o poco ácidos, hasta un pH máximo de 6.5.
Experiencias de conservación de aceitunas de mesa (De la Borbolla et al.. 1961; Savastano y Castorina, 1965) han evidenciado que la duración de la actividad fungistática del ácido sórbico y de sus sales, está directamente relacionada con el porcentaje empleado del aditivo y que la flora bacteriana se afecta sólo ligeramente, al mismo tiempo que el color de la salmuera de las aceitunas tiende a sufrir un ligero oscurecimiento.
Por su parte, el ácido sórbico es utilizado en la conservación de alimentos en general por su acción antimicrobiana, que se explica a través de la inhibición de diferentes sistemas enzimáticos de los microorganismos respectivos, por su inocuidad fisiológica y su reducida influencia sobre las características organolépticas. Por su baja constante de disociación puede ser usado en alimentos ácidos y poco ácidos, hasta un pH máximo de 6,5 y actúa, principalmente, en forma de sal contra levaduras y mohos inhibiendo sólo parcialmente a las bacterias (Dziezak, 1986). Los resultados de las investigaciones sobre la actividad bacteriostática del ácido sórbico no siempre concuerdan (Scheneman y Costilow, 1955; Sofos, 1983; Sofos et al., 1979).
Es más, parece que en concentraciones ineficaces, algunos microorganismos, pueden metabolizarlo cuando se encuentran en una elevada densidad, produciendo CO2 y H2O (Luck. 1982; Deak y Novak, 1972; York y Vaughn, 1954). Los lactobacilos pueden reducir el ácido sórbico al alcohol correspondiente, el sorbitol, que reacciona con el etanol formando un éter que tiene un fuerte olor a geranio (Luck, 1982).
Este conservante es particularmente utilizado para los quesos, las frutas secas, productos de panadería, dulces, ensaladas especiales, bebidas, vegetales fermentados y encurtidos (King, 1981), utilizando concentraciones que oscilan del 0,01 al 0,1%. Estos porcentajes se aumentan en un 25% si dicho aditivo se utiliza en forma de sales hidrosolubles (sórbalos). En la conservación de aceitunas de mesa, la proporción máxima permitida es de 0,5 g/kg de producto, incluida la salmuera.
Es admisible por humanos siempre que su concentración no sobrepase de un 0.2% (25 mg/Kg de peso corporal).[1] Su efectividad es mayor en alimentos ácidos, siendo menor en alimentos con pH neutro. Su uso hace que se prevenga la formación de hongos, mohos o levaduras en alimentos y bebidas. Se emplea en la conservación de lácteos.[2] Investigaciones han mostrado su efectividad como bactericida. Es empleado en la industria del vino con similares intenciones bactericidias.[3]
Existencia
Se puede encontrar este ácido en muchas frutas, pero su concentración más alta es en la fruta del sorbellano (Sorbus aucuparia).
Referencias
- ↑ a b Monroe Jay, James; Martin J. Loessner, David A. Golden (2006) (en inglés). Modern Food Microbiology (7ª edición). Springer. ISBN 0387231803.
- ↑ John Gilbert Davis. Cheese (1ª edición). American Elsevier Pub. Co.
- ↑ Margalit, Yair (2004). James Crum. ed (en inglés). Concepts in Wine Chemistry (2ª edición). San Francisco: Library of Congress. ISBN 1-8912667-74-4.
Enlaces externos
Categorías:- Ácidos carboxílicos
- Aditivos alimentarios
- Conservantes
Wikimedia foundation. 2010.
