- Fuerzas de van der Waals
-
Fuerzas de van der Waals
En química física, la fuerza de van der Waals (o interacción de van der Waals), denominada así en honor al científico holandés Johannes Diderik van der Waals, es la fuerza atractiva o repulsiva entre moléculas (o entre partes de una misma molécula) distintas a aquellas debidas al enlace covalente o a la interacción electrostática de iones con otros o con moléculas neutras.[1] El término incluye:
- fuerzas dipolo permanente-dipolo permanente (fuerzas de Keesom)
- fuerzas dipolo permanente-dipolo inducido (fuerzas de Debye)
- fuerzas dipolo inducido instantáneo-dipolo inducido (fuerzas de dispersión de London)
También se usa en ocasiones como un sinónimo para la totalidad de las fuerzas intermoleculares. Las fuerzas de van der Waals son relativamente débiles comparadas con los enlaces químicos normales, pero juegan un rol fundamental en campos tan diversos como química supramolecular, biología estructural, ciencia de polímeros, nanotecnología, ciencia de superficies, y física de materia condensada. Las fuerzas de van der Waals definen el carácter químico de muchos compuestos orgánicos. También definen la solubilidad de sustancias orgánicas en medios polares y no polares. En los alcoholes inferiores, las propiedades del grupo polar hidróxilo dominan a las débiles fuerzas intermoleculares de van der Waals. En los alcoholes superiores, las propiedades del radical alquílico apolar (R) dominan y definen la solubilidad. Las fuerzas de van der Waals crecen con la longitud de la parte no polar de la sustancia.
Las fuerzas de van der Waals incluyen a atracciones entre átomos, moléculas, y superficies. Difieren del enlace covalente y del enlace iónico en que están causados por correlaciones en las polarizaciones fluctuantes de partículas cercanas (una consecuencia de la dinámica cuántica). Las fuerzas intermoleculares tienen cuatro contribuciones importantes. En general, un potencial intermolecular tiene un componente repulsivo (que evita el colapso de las moléculas debido a que al acercarse las entidades unas a otras las repulsiones dominan). También tiene un componente atractivo que, a su vez, consiste de tres contribuciones distintas:
Las interacciones electrostáticas entre las cargas (en el caso de iones moleculares), dipolos (en el caso de moléculas sin centro de inversión), cuadrupolos (todas las moléculas con simetría menor a la cúbica), y en general entre multipolos permanentes) La interacción electrostática también es denominada interacción de Keesom o fuerza de Keesom, en honor a Willem Hendrik Keesom.
- La segunda fuente de atracción es la inducción (también denominada polarización), que es la interacción entre un ultipolo permanente en una molécula, con un multipolo inducido en otra. Esta interacción se mide algunas veces en debyes, en honor a Peter Debye.
- La tercera atracción suele ser denominada en honor a Fritz London que la denominaba dispersión. Es la única atracción experimentada por átomos no polares, pero opera entre cualquier par de moléculas, sin importar su simetría.
Todas las fuerzas intermoleculares de van der Waals presentan anisotropía (excepto aquellas entre átomos de dos gases nobles), lo que significa que dependen de la orientación relativa de las moléculas. Las interacciones de inducción y dispersión son siempre atractivas, sin importar su orientación, pero el signo de la interacción cambia con la rotación de las moléculas. Esto es, la fuerza electrostática puede ser atractiva o repulsiva, dependiendo de la orientación mutua de las moléculas. Cuando las moléculas tienen movimiento térmico, como cuando están en fase gaseosa o líquida, la fuerza electrostática se reduce significativamente, debido a que las moléculas rotan térmicamente y experimentan las partes repulsiva y atractiva de la fuerza electrostática. Algunas veces, este efecto se expresa indicando que el "movimiento térmico aleatorio a temperatura ambiente puede imponerlo o anularlo" (refiriéndose al componente electrostático de la fuerza de van der Waals). Claramente, el efecto térmico promedio es mucho menos pronunciado para las fuerzas atractivas de inducción y dispersión.
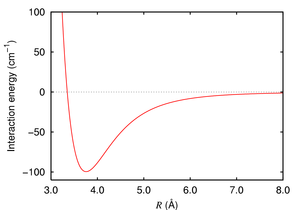
El potencial de Lennard-Jones se usa frecuentemente como un modelo aproximado para la parte isótropa de una fuerza de van der Waals total (repulsión más atracción) como una función de la distancia.
Contenido
Fuerza de dispersión de London
Las fuerzas de dispersión de London, denominadas así en honor al físico germano-americano Fritz London, son fuerzas intermoleculares débiles que surgen de fuerzas interactivas entre multipolos temporales en moléculas sin momento multipolo permanente. Las fuerzas de dispersión de London también son conocidas como fuerzas de dispersión, fuerzas de London o fuerzas dipolo-dipolo inducido.
Las fuerzas de London pueden ser exhibidas por moléculas no polares debido a que la densidad electrónica se mueve alrededor de la molécula de una manera probabilística (ver teoría mecánico cuántica de las fuerzas de dispersión). Hay una gran probablidad de que la densidad electrónica no esté distribuida por igual en una molécula apolar. Cuando los electrones están desigualmente distribuidos, existe un multipolo temporal. Este multipolo interactuará con otros multipolos cercanos e inducirá a las moléculas, pero sólo son una pequeña parte de la fuerza de interacción total.
La densidad electrónica en una molécula puede ser redistribuida por la proximidad de otro multipolo. Los electrones se acumularán en el lado de la molécula que encara a la carga positiva y se retirarán de la carga negativa. Entonces, puede producirse un multipolo transiente por una molécula polar cercana, o incluso por un multipolo transiente en otra molécula apolar.
En el vacío, las fuerzas de London son más débiles que otras fuerzas intermoleculares tales como las interacciones iónicas, el enlace de hidrógeno, o las interacciones permanentes dipolo-dipolo.
Este fenómeno es la única fuerza intermolecular atractiva a grandes distancias, presente entre átomos neutros (vg. un gas noble), y es la principal fuerza atractiva entre moléculas no polares (vg. dinitrógeno o metano). Sin las fuerzas de London, no habría fuerzas atractivas entre los átomos de un gas noble, y no podrían existir en la forma líquida.
Las fuerzas de London se hacen más fuertes a la vez que el átomo o molécula en cuestión se hace más grande. Esto es debido a la polarizabilidad incrementada de moléculas con nubes electrónicas más grandes y dispersas. Este comportamiento puede ejemplificarse por los halógenos (del más pequeño al más grande: F2, Cl2, Br2, I2). El diflúor y el dicloro son gases a temperatura ambiente, el dibromo es un líquido, y el diyodo es un sólido. Las fuerzas de London también se hacen fuertes con grandes cantidades de superficie de contacto. Una mayor área superficial significa que pueden darse más interacciones cercanas entre diferentes moléculas.
Relación con el efecto Casimir
Las fuerzas de van der Waals-London están relacionadas al efecto Casimir para los medios dieléctricos, que es la descripción microscópica de las propiedades de los últimos. Los primeros cálculos detallados fueron hechos en 1955 por E. M. Lifshitz.[2]
Notas
- ↑ International Union of Pure and Applied Chemistry (1994). "van der Waals forces". Compendium of Chemical Terminology Internet edition.(en inglés)
- ↑ IE Dzyaloshinskii, EM Lifshitz, LP Pitaevskii: General theory of van der Waals' forces
Fuentes
- Iver Brevik, V. N. Marachevsky, Kimball A. Milton, Identity of the van der Waals Force and the Casimir Effect and the Irrelevance of these Phenomena to Sonoluminescence, hep-th/9901011
- I. D. Dzyaloshinskii, E. M. Lifshitz, and L. P. Pitaevskii, Usp. Fiz. Nauk 73, 381 (1961)
- Traducción al inglés: Soviet Phys. Usp. 4, 153 (1961)
- L. D. Landau and E. M. Lifshitz, Electrodynamics of Continuous Media, Pergamon, Oxford, 1960, pp. 368–376.
- Mark Lefers, "Van der Waals dispersion force". Holmgren Lab.
- E. M. Lifshitz, Zh. Eksp. Teor. Fiz. 29, 894 (1955)
- Traducción al inglés: Soviet Phys. JETP 2, 73 (1956)
- Western Oregon University's "London force". Intermolecular Forces. (animación)
- J. Lyklema, Fundamentals of Interface and Colloid Science, p. 4.43
Categorías: Fuerzas intermoleculares | Enlace químico
Wikimedia foundation. 2010.