- Tetraterpenoides
-
 Modelo de bolas de la estructura molecular del isopreno, la unidad química de los terpenos.
Modelo de bolas de la estructura molecular del isopreno, la unidad química de los terpenos.
 Muchos terpenos son extraídos de la resina de las coníferas, aquí un pino.
Muchos terpenos son extraídos de la resina de las coníferas, aquí un pino.
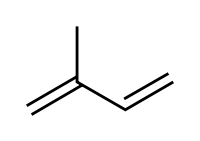
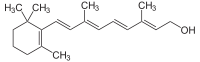
Los terpenos[1] o isoprenoides son una vasta y diversa clase de compuestos orgánicos derivados del isopreno (o 2-metil-1,3-butadieno), un hidrocarburo de 5 átomos de carbono. El nombre proviene de que los primeros miembros de esta clase fueron derivados del aguarrás ("turpentine" en inglés, "terpentin" en alemán).[2] Cuando los terpenos son modificados químicamente, por ejemplo por oxidación o reorganización del esqueleto hidrocarbonado, suelen denominarse terpenoides (como la vitamina A o retinol, que contiene un átomo de oxígeno).
Los tetraterpenoides son los terpenoides de 40 carbonos (8 unidades de isopreno). Los tetraterpenos más prevalentes son los pigmentos carotenoides accesorios que cumplen funciones esenciales en la fotosíntesis.
Contenido
Generalidades
Los terpenos se originan por polimerización enzimática de dos o más unidades de isopreno, ensambladas y modificadas de muchas maneras diferentes. La mayoría de los terpenos tienen estructuras multicíclicas, las cuales difieren entre sí no sólo en grupo funcional sino también en su esqueleto básico de carbono. Los monómeros generalmente son referidos como unidades de isopreno porque la descomposición por calor de muchos terpenos da por resultado ese producto; y porque en condiciones químicas adecuadas, se puede inducir al isopreno a polimerizarse en múltiplos de 5 carbonos, generando numerosos esqueletos de terpenos. Por eso se relaciona a los terpenos con el isopreno, si bien se sabe ya desdes hace más de 100 años que el isopreno no es el precursor biológico de esta familia de metabolitos.[2]
Estos lípidos se encuentran en toda clase de seres vivos, y son sintetizados por las plantas, donde son importantes en numerosas interacciones bióticas (Goodwin 1971).[3] En las plantas los terpenos cumplen muchas funciones primarias: algunos pigmentos carotenoides son terpenos, también forman parte de la clorofila y las hormonas giberelina y ácido abscísico. Los terpenos también cumplen una función de aumentar la fijación de algunas proteínas a las membranas celulares, lo que es conocido como isoprenilación. Los esteroides y esteroles son producidos a partir de terpenos precursores.
Los terpenos de las plantas son extensamente usados por sus cualidades aromáticas. Juegan un rol importante en la medicina tradicional y en los remedios herbolarios, y se están investigando sus posibles efectos antibacterianos y otros usos farmacéuticos. Están presentes, por ejemplo, en las esencias del eucalipto, los sabores del clavo y el jengibre. También en el citral, mentol, alcanfor, y los cannabinoides.
Clasificación
Los terpenos son hidrocarburos que pueden verse como una combinación de numerosas unidades isopreno, por lo general unidas de forma cabeza-cola, pero también pueden darse combinaciones cabeza-cabeza y algunos compuestos están formados por uniones cabeza-medio. Los terpenoides pueden ser considerados como terpenos modificados donde grupos metilo han sido reacomodados o removidos, o a los que se les han añadido átomos de oxígeno. Algunos autores usan el término terpeno para referirse a los terpenoides.
La clasificación de los terpenos según su estructura química, es similar a la de los terpenos, los cuales son clasificados en base al número de unidades isopreno presentes y en el caso de los triterpenos, si están ciclados. Se los clasifica en:
- Hemiterpenos. Los terpenos más pequeños, con una sola unidad de isopreno. Poseen 5 carbonos. El hemiterpeno más conocido es el isopreno mismo, un producto volátil que se desprende de los tejidos fotosintéticamente activos.
- Monoterpenos. Terpenos de 10 carbonos. Llamados así porque los primeros terpenos aislados del aguarrás en los 1850s, fueron considerados la unidad base, a partir de la cual se hizo el resto de la nomenclatura. Los monoterpenos son mejor conocidos como componentes de las esencias volátiles de las flores y como parte de los aceites esenciales de hierbas y especias, en los que ellos forman parte de hasta el 5 % en peso de la planta seca.
- Sesquiterpenos. Terpenos de 15 carbonos (es decir, terpenos de un monoterpeno y medio). Como los monoterpenos, muchos sesquiterpenos están presentes en los aceites esenciales. Además muchos sesquiterpenos actúan como fitoalexinas, compuestos antibióticos producidos por las plantas en respuesta a la aparición de microbios, y como inhibidores de la alimentación ("antifeedant") de los herbívoros oportunistas. La hormona de las plantas llamada ácido abscísico es estructuralmente un sesquiterpeno, su precursor de 15 carbonos, la xantosina, no es sintetizada directamente de 3 unidades isopreno sino producida por un "cleavage" asimétrico de un carotenoide de 40 unidades.
- Diterpenos. Terpenos de 20 carbonos. Entre ellos se incluye el fitol, que es el lado hidrofóbico de la clorofila, las hormonas giberelinas, los ácidos de las resinas de las coníferas y las especies de legumbres, las fitoalexinas, y una serie de metabolitos farmacológicamente importantes, incluyendo el taxol, un agente anticáncer encontrado en muy bajas concentraciones (0,01% de peso seco) en la madera del tejo ("yew"), y forskolina, un compuesto usado para tratar el glaucoma. Algunas giberelinas tienen 19 átomos de carbono por lo que no son consideradas diterpenos porque perdieron un átomo de carbono durante una reacción de "cleavage".
- Triterpenos. Terpenos de 30 carbonos. Son por lo general generados por la unión cabeza-cabeza de dos cadenas de 15 carbonos, cada una de ellas formada por unidades de isopreno unidas cabeza-cola. Esta gran clase de moléculas incluye a los brassinoesteroides, componentes de la membrana que son fitoesteroles, algunas fitoalexinas, varias toxinas y "feeding deterrents", y componentes de las ceras de la superficie de las plantas, como el ácido oleanólico de las uvas.
- Tetraterpenos. Terpenos de 40 carbonos (8 unidades de isopreno). Los tetraterpenos más prevalentes son los pigmentos carotenoides accesorios que cumplen funciones esenciales en la fotosíntesis.
- Politerpenos. Los politerpenos, que contienen más de 8 unidades de isopreno, incluyen a los "prenylated quinone electron carriers" como la plastoquinona y la ubiquinona, también poliprenoles de cadena larga relacionados con las reacciones de transferencia de azúcares (por ejemplo el dolicol), y también a enormemente largos polímeros como el "rubber", usualmente encontrado en el látex.
- Meroterpenos. Así se llama a los metabolitos secundarios de las plantas que tienen orígenes sólo parcialmente derivados de terpenos. Por ejemplo, tanto las citokininas como numerosos fenilpropanoides contienen cadenas laterales de un isoprenoide de 5 carbonos. El principio activo de la marihuana son los cannabinoides, los cuales tienen una porción molecular de origen policétido y la otra es terpénica. Algunos alcaloides, como las drogas anticáncer vincristina y vinblastina, contienen fragmentos terpenos en sus estructuras. Además algunas proteínas modificadas incluyen una cadena lateral de 15 o 20 carbonos que es un terpeno, que es el que ancla la proteína a la membrana.
- Esteroides. Triterpenos basados en el sistema de anillos ciclopentanoperhidrofenantreno ("cyclopentane perhydro-phenanthrene ring system"). Buchanan et al. no los consideran terpenos.[2]
Biosíntesis
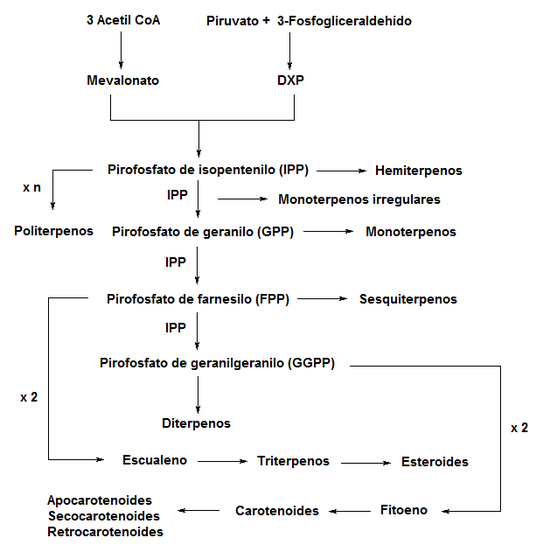
Los terpenos se forman a través de uniones de unidades biológicas de isopreno. La unión de dos monómeros de acuerdo a la Regla Isoprénica de Wallach pueden dar el precursor pirofosfato de geranilo (GPP). Los terpenos irregulares, tales como el ácido crisantémico de las piretrinas, no siguen esta regla. El pirofosfato de geranilo es precursor de los monoterpenos. La incorporación de otra unidad isoprénica da como producto el pirofosfato de farnesilo (FPP), precursor de los sesquiterpenos. Una unidad más forma el pirofosfato de geranilgeranilo (GGPP), el cual es el compuesto base para formar diterpenos. El escualeno, precursor de triterpenos y esteroides, se forma por la dimerización de dos unidades de FPP, mientras que el fitofluoeno, compuesto base para los carotenoides, se obtiene de manera homóloga por dimerización de el GGPP. Los politerpenos se forman por uniones isoprénicas múltiples y repetitivas, y por regla general no presentan ciclizaciones.
Las unidades de isopreno pueden ser biosintetizadas por medio de dos vías:
- A través de intermediarios de la Ruta del Ácido Mevalónico (MVA)
- A partir de compuestos derivados de la Ruta del 2-C-metil-D-eritritol 4-fosfato , denominada también Ruta de la 5-Fosfono-1-Desoxi-D-Xilulosa (DXP). Originalmente se pensaba que los precursores biosintéticos de todos los terpenos provenían de la ruta MVA, hasta que recientemente se descubrió que diversos terpenos en plantas y bacterias se producen mediante la ruta DXP.[4]
Ruta del ácido mevalónico
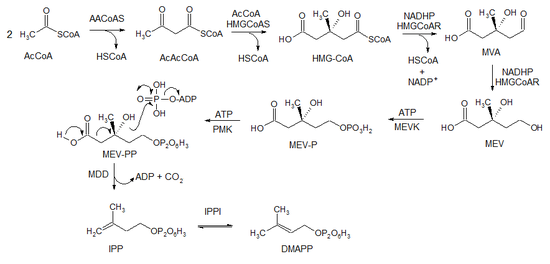
Esta ruta biosintética parte de dos unidades de acetil coenzima A (Ac-CoA), en donde se condensan por medio de una reacción tipo Claisen para dar acetoacetil-CoA (AcAcCoA). Esta molécula se vuelve a condensar con una tercera unidad de AcCoA para dar como producto 3-hidroxi-3-metilglutaril-CoA (HMG-CoA) como intermediario. El tioéster de la coenzima A se reduce para formar el aldehído correspondiente, el mevaldehído (MVA), el cual se reduce a ácido mevalónico (MEV). Por acción de dos moléculas de adenosin trifosfato (ATP) el mevalonato se fosforila (MEV-P y MEV-PP) y descarboxila para dar como productos los precursores de los terpenos, el pirofosfato de isopentenilo (IPP) y su isómero, el pirofosfato de dimetilalilo (DMAPP). La ruta del mevalonato es prácticamente universal y se lleva a cabo en el citosol. Por esta ruta se sintetizan principalmente sesquiterpenos, triterpenos y politerpenos.[5]
Enzimas:
- EC 6.2.1.16 Acetoacetil-CoA sintetasa (AACoAS).
- EC 4.1.3.5 3-Hidroxi-3-metilglutaril-CoA sintasa (HMGCoAS).
- EC 1.1.1.88 3-hidroxi-3-metilglutaril-CoA reductasa (HMGCoAR).
- EC 2.7.1.36 Mevalonato quinasa (MEVK).
- EC 2.7.4.2 Fosfomevalonato quinasa (PMK).
- EC 4.1.1.33 Mevalonate 5-difosfato descarboxilasa (MDD).
- EC 5.3.3.2 Difosfato de isopentenilo isomerasa (IPPI)
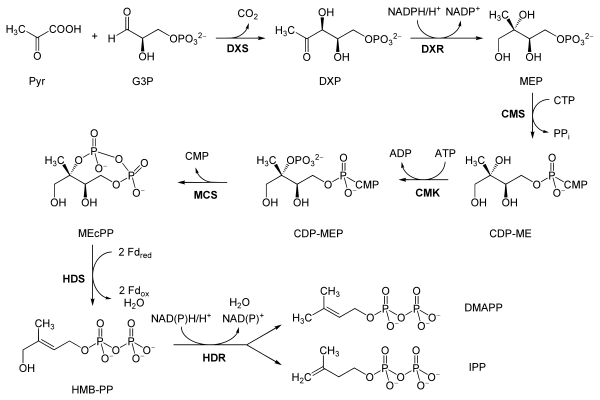
Ruta de la 5-Fosfono-1-Desoxi-D-Xilulosa
Flesch observó en 1988 que los patrones de marcaje isotópico en terpenos hopanoides de las bacteria Rhodopseudomonas no coincidían con los correspondientes por una biosíntesis mevalónica.[6] Estudios posteriores encontraron que existía una segunda alternativa independiente del mevalonato para biosintetizar unidades isoprénicas en bacterias y plantas. En esta ruta, una unidad de ácido pirúvico (Pyr), proveniente de la degradación de carbohidratos, se condensa en una reacción de Umpolung del grupo carbonilo del piruvato con el grupo carbonílico del D-gliceraldehído (G3P), para dar la 5-Fosfono-1-desoxi-D-xilulosa (DXP). Por medio de un condensación aldólica inversa, el carbono 1 transpone hacia la posición 2, generando así el 4-fosfono-2-C-metil-D-eritritol (MEP). Éste intermediario se conjuga por medio de una sustitución nucleofílica con una unidad de citidilribósido, por acción del CTP, para formar 4-(CDP)-2-C-metil-D-eritritol (CDP-ME). Este compuesto se fosforila en el carbono 2, donde se forma el intermediario fosforilado CDP-EMP y desplaza el citidilribósido para obtenerse el 2-C-metil-D-eritritol-2,4-ciclofosfato (MEcPP). Por ruptura reductiva del ciclo se da una reacción de eliminación para formar el pirofosfato de 4-hidroxi-3-metil-but-2-enilo (HMB-PP). El paso final consiste en la eliminación del grupo hidroxilo para obtenerse el catión alílico correspondiente, el cual puede transponerse de tal forma que se isomerizan de manera reversible el IPP y el DMAPP. Esta ruta se lleva a cabo sobre todo en los plástidos de las plantas y en muchas células procariontes. Por esta ruta se sintetizan sobre todo monoterpenos, diterpenos y carotenoides.
Enzimas:
- EC 2.2.1.7: 5-Fosfono-1-desoxi-D-xilulosa sintasa (DXS)
- EC 1.1.1.267 5-Fosfono-1-desoxi-D-xilulosa reductoisomerasa (DXR)
- EC 2.7.7.60 2-C-metil-D-eritritol 4-fosfato citidililtransferasa (CMS)
- EC 2.7.1.148. 4-difosfocitidil-2-C-metil-D-eritritol quinasa. (CMK)
- EC 4.6.1.12 2-C-metil-D-eritritol 2,4-ciclodifosfato sintasa (MCS)
- EC 1.17.4.3 4-hidroxi-3-metilbut-2-en-1-il difosfato sintasa (HDS)
- EC 1.17.1.2 4-hidroxi-3-metilbut-2-enil difosfato reductasa (HDR)
Funciones
Dan coloración a los órganos vegetales y participan en la síntesis de las vitaminas A, K y E. Por ejemplo el color anaranjado de la zanahoria.
La formación de terpenos en plantas, animales y microorganismos es hecha por enzimas muy similares, pero hay importantes diferencias en los procesos. En particular, las plantas producen una variedad muchísimo mayor que la que producen los animales o los microbios, y esta diferencia está reflejada en la compleja organización de la biosíntesis de los terpenos de las plantas al nivel del tejido, celular, subcelular, y genético. La biosíntesis de los terpenos está compartimentalizada, como también lo está la formación de su precursor el IPP. La producción de grandes cantidades de terpenos así como su subsecuente acumulación, emisión o secreción es casi siempre asociada con la presencia de estructuras anatómicamente altamente especializadas. Por ejemplo los tricomas glandulares y las cavidades secretorias de las hojas, y la epidermis glandular de los pétalos generan y almacenan o emiten terpenos que son aceites esenciales importantes para la polinización por insectos. Los conductos y ampollas de resina de las coníferas producen y acumulan una resina defensiva consistenteen aguarrás ("turpentine", o "monoterpene olefins") y rosina (ácidos resinosos diterpenos). Las ceras superficiales triterpenos son formadas y excretadas por una epidermis especialiada, y los laticíferos producen ciertos triterpenos y politerpenos como el "rubber". Estas estructuras especializadas secuestran a los metabolitos secundarios lejos de los procesos metabólicos sensibles y así previenen la autotoxicidad. Muchas estructuras de este tipo son no fotosintéticas y por lo tanto dependen de células adyacentes para suplirse del carbono y la energía necesarios para biosintetizar los terpenos.
Algunos terpenos que se consideran como nutrimentos: retinaldehído, el retinol, los carotenos, los tocoferoles, las quinonas y las ubiquinonas. Se utiliza el término vitamina A para el retinol y los carotenos; vitamina E para los tocoferoles y vitamina K para las quinonas. La vitamina a participa en el ciclo visual, que permite la adaptación de los bastones retinianos a la oscuridad; mantenimiento de epitelios; respuesta inmunitaria; el gusto; la audición y el crecimiento.
Rol de los terpenos en Botánica Sistemática
Algunos tipos de terpenos fueron extensamente utilizados en Botánica Sistemática para establecer relaciones de parentesco entre taxones de organismos.[7] Algunos de ellos son:
- Los aceites esenciales son característicos de los Magnoliales, Laurales, Austrobaileyales, y Piperales, y también de otros clados poco emparentados con éstos, como Myrtaceae, Rutaceae, Apiales, Lamiaceae, Verbenaceae y Asteraceae.
- Las piretrinas son una mezcla de compuestos orgánicos que se encuentran de modo natural en las flores de plantas del género Chrysanthemum, como Chrysanthemum cinerariaefolium (denominado piretro o pelitre) o Chrysanthemum coronarium.[8]
- Las lactonas sesquiterpénicas son conocidas principalmente en las Asteraceae, pero también están presentes en otras familias, como Apiaceae, Magnoliaceae y Lauraceae.
- La betulina es un triterpeno presente en Betula papyrifera y especies relacionadas.
- Las saponinas triterpénicas están presentes en las Apiaceae y Pittosporaceae.
- Los limonoides y cuasinoides son derivados de triterpenos presentes en Rutaceae, Meliaceae y Simaroubaceae de los Sapindales.
- Los cardenólidos son glicósidos de un esteroide, están presentes en las Ranunculaceae, Euphorbiaceae, Apocynaceae, Liliaceae y Plantaginaceae.
- Los iridoides son derivados de monoterpenos 9-carbonados o 10-carbonados, y usualmente están presentes como glicósidos. Los secoiridoides están presentes en muchas familias del clado de las astéridas, como Gentianales, Dipsacales, y muchas familias de Cornales y Asterales. Los iridoides carbocíclicos son característicos de los Lamiales, excepto por Oleaceae, Tetrachondraceae y Gesneriaceae.
Referencias
- ↑ Devlin, T. M. 2004. Bioquímica, 4ª edición. Reverté, Barcelona. ISBN 84-291-7208-4
- ↑ a b c R. Croteau, T. M. Kutchan, N. G. Lewis. "Natural Products (Secondary Metabolites)". En: Buchanan, Gruissem, Jones (editores). Biochemistry and Molecular Biology of Plants. American Society of Plant Physiologists. Rockville, Maryland, Estados Unidos. 2000. Capítulo 24.
- ↑ Goodwin, T.W. 1971. Aspects of terpenoid chemistry and biochemistry. Academic Press, Londres.
- ↑ Eisenreich W, Rohdich F, Bacher A. (2001). «Deoxyxylulose phosphate pathway to terpenoids.». Trends Plant Sci. 6 (2): pp. 78-84. doi:.
- ↑ Paul M. Dewick (2009). Medicinal natural products: a biosynthetic approach. John Wiley and Sons. ISBN 0470741686, 9780470741689.
- ↑ Flesch, G.; Rohmer, M. (1988). «Prokaryotic hopanoids: the biosynthesis of the bacteriohopane skeleton». European Journal of Biochemistry 175 (2): pp. 405–411. doi:.
- ↑ "Secondary Plant Compounds". en: Judd, W. S. Campbell, C. S. Kellogg, E. A. Stevens, P.F. Donoghue, M. J. 2002. Plant systematics: a phylogenetic approach, Second Edition.Sinauer Axxoc, USA. Capítulo 4.
- ↑ Pascual-Villalobos MJ. 1996. Evaluación de la actividad insecticida de extractos vegetales de Chrysanthemum coronarium. Boletín de Sanidad Vegetal y Plagas 22 (2): 411-420.
Categoría:- Terpenos
Wikimedia foundation. 2010.