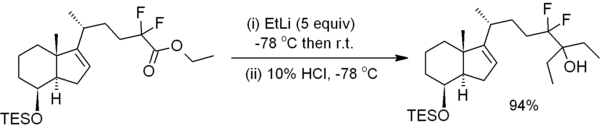- Organolitio
-
Un reactivo de organolitio es un compuesto organometálico con un enlace covalente entre un átomo de carbono y uno de litio. Como la naturaleza electropositiva del litio hace que la densidad de carga del enlace esté sobre el átomo de carbono, se crea efectivamente un carbanión. De ahí que los compuestos de organolitio sean bases y nucleófilos extremadamente potentes.
Contenido
Producción
Los reactivos de organolitio se preparan industrialmente por la reacción de un halocarbono con litio metálico, esto es: R-X + 2 Li → R-Li + LiX.[1] Una reacción secundaria de esta síntesis, especialmente con los yoduros de alquilo, es la reacción de Wurtz, en la que una especie R-Li reacciona con especies R-X formando un producto R-R. Esta reacción secundaria puede ser evitada casi completamente utilizando cloruros o bromuros.
Un segundo método es la reacción de un haluro de alquilo o sulfuro de arilo y alquilo con una sal aniónica radical de litio, como el naftaluro de litio. Estos aniones radicales pueden ser preparados por la reducción de un sistema aromático como el naftaleno con litio metálico. Como la reducción orgánica de los haluros de alquilo es mucho más rápida con los radicales aniónicos que mediante la reacción directa con metal litio, esta reacción permite la síntesis de un número más amplio de compuestos exóticos de organolitio.
Un tercer método involucra el intercambio metal-halógeno entre un compuesto de halogenuro orgánico (generalmente un yoduro o bromuro) y una especie de organolitio (generalmente n-butillitio, n-BuLi, sec-butillitio, equilibrio, la reacción es exitosa sólo si el reactivo de litio formado tiene un carbanión más estable que el reactivo de litio inicial. Este método es usado frecuentemente para preparar reactivos de vinillitio, arillitio y alquillitio primario, y es especialmente valioso para la preparación de reactivos de litio funcionalizados, donde las condiciones drásticas requeridas para la reacción con litio metálico deben ser evitadas.
Un cuarto método es un intercambio, esta vez entre un compuesto de organolitio y otro compuesto organometálico. Esta es, nuevamente, una reacción en equilirbio, donde el metal más electropositivo (litio) terminará unido al gupo orgánico más electronegativo. Un ejemplo es la síntesis de vinillitio a partir de tetravinilestaño y fenillitio. El vinillitio es muy difícil de preparar por otros métodos.
Un quinto método es la desprotonación de un compuesto orgánico con especies de organolitio, en una reacción ácido-base.
Estructura
Los reactivos de organolitio pueden agregarse de forma que el litio se coordine con más de un átomo de carbono, y cada átomo de carbono se coordine con más de un átomo de litio. Tres factores generales afectan la agregación: la interacción electrostática entre cargas opuestas, la esfera de coordinación del litio puede incluir moléculas de disolvente o base de Lewis, y el impedimento estérico de la parte hidrocarbonada.[2] Los átomos de litio tienden a formar triángulos y agregados superiores.
En el metillitio en estado sólido, 4 átomos de litio forman un tetraedro con cada cara tapada por un grupometilo que enlaza simultáneamente con 3 átomos de litio (η3 hapticidad). Interacciones de largo alcance entre las unidades (MeLi)4 se basan sobre el enlace η3-Li-CH3-η1-Li. Butillitio forma un octaedro hexamérico Li6 sin ninguna interacción de largo alcance.
La adición de una base de Lewis como los disolventes dietiléter o THF, o los ligandos nitrogenados TMEDA, PMDTA o esparteina tiende a desagregar los compuestos de organolitio, haciéndolos más solubles y reactivos. El complejo de estado sólido de MeLi con (-)-esparteina es un dímero. El complejo de butillitio con PMDTA está muy próxino al monómero BuLi.
En disolución, el metillitio en THF a concentración 1M es un tetrámero, el n-butillitio en benceno a concentración 3M es un hexámero y en THF a concentración 1M es un tetrámero. t-BuLi en THF es un dímero. Isopropillitio en ciclopentano es una mezcla de las formas hexámero, octámero y nonámero.
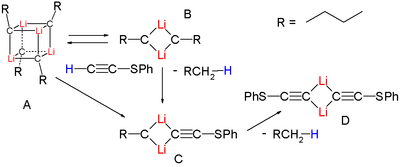
Diferentes estados de agregación de organolitio se encuentran en la desprotonación simple del alquino terminal (feniltio)acetileno por n-butillitio en THF a -135 °C, un proceso que puede ser seguido por espectroscopía NMR de 7Li:[3]
El tetrámero de una sustancia parecida al cubano A es fuertemente reactivo comparado con eldímero B que forma en primer lugar laespecie de mezcla de dímeros C y finalmente el homodímero D. De hecho, el dímero es más reactivo que el tetrámero en un factor de 3.2x108.
Usos
Los compuestos de organolitio están fuertemente polarizados debido al carácter electropositivo del litio. Son, por lo tanto, nucleófilos altamente reactivos y reaccionan con casi todos los tipos de electrófilos. Son semejantes a los reactivos de Grignard, pero son mucho más reactivos. Debido a esta reactividad, son incompatibles con agua, oxígeno (O2), y dióxido de carbono, y deben ser manejados bajo atmósfera protectora como nitrógeno o, preferiblemente, argón.
Un uso común de los compuestos de organolitio simples disponibles comercialmente (como n-BuLi, sec-BuLi, t-BuLi, MeLi ó PhLi) es como bases muy fuertes. Los compuestos de organolitio pueden desprotonar casi todos los compuestos que contienen hidrógeno (la metalación o reacción de intercambio Li/H), con la excepción de los alcanos. En principio, una desprotonación puede ir hasta la terminación si el compuesto acído tiene un pKA 2 unidades mayor (ácido 100 veces más fuerte) que el compuesto de litio, aunque en la práctica se requiere una diferencia de pKA más grande para obtener tasas de desprotonación de los ácidos con enlace C-H débilmente ácidos. Como los grupos alquilo son donantes de electrones débiles, la basicidad delcompuesto de organolitio aumenta con el número de sustituyentes alquilo sobre el átomo de carbono que soporta la carga. Esto hace que el base (química) más fuerte comercialmente disponible con un pKa mayor de 53. La reacción de metalación es un importante método de síntesis para la preparación de muchos compuestos de organolitio. A continuación se muestran algunos ejemplos:
Los compuestos de organolitio se usan también habitualmente para reacciones de adición nucleofílica a compuestos con el grupo carbonilo C=O y otros átomos de carbono electrófilos. la desprotonación puede ser una reacción colateral con compuestos de carbonilo enolizable,especialmente con reactivos de organolitio con impedimento estérico tales como t-butillitio. Los reactivos de Grignard, aunque mucho menos reactivos, son una alternativa en reacciones de adición, con menos problemas con la desprotonación.
Una utilidad importante de los reactivos de organolitio es para la preparación de otros compuestos organometálicos, habitualmente por reacción con haluros de metal. Especialmente importante en química orgánica de síntesis es la formación de reactivos de organocobre (incluido el reactivo de Gilman) por reacción de alquillitio, RLi, con yoduro de cobre (I), CuI, o con CuBr, y la preparación de reactivos de organozinc por reacción con cloruro de zinc, ZnCl2. Incluso los reactivos de Grignard se preparan a veces por reacción de alquillitio, RLi, con bromuro de magnesio, MgBr2, en situaciones donde el reactivo de litio (pero no los compuestos de Grignard) puede prepararse fácilmente por reacción de metalación. Los compuestos de Organoestaño, organosilicio, organoboro, organofósforo, y organoazufre se preparan también frecuentemente por reacción de alquillitio, RLi, con el electrófilo apropiado.
Una reciente revisión de la química de estos procesos indica que los reactivos de organolitio más frecuentemente usados son: butillitio, hexillitio, sec-butillitio, y fenillitio.[4] El Metillitio se usa también con frecuencia. Dos bases fuertes usadas muy frecuentemente y preparadas a partir butillitio son la diisopropilamida de litio (LDA), y la hexametildisilazida de litio (LiHMDS).
Los derivados de arillitio son compuestos intermedios en la matalación dirigida a la posición orto (orto-metalación) tales como Me2NCH2C6H4-2-Li obtenido a partir de dimetilbenzilamina y butillitio.
Reactividad
Algunas reacciones generales de compuestos de organolitio son::
- Protonación en reacciones con cualquier compuesto que contenga protones ácidos
- Reacción con cetonas y aldehídos para dar alcoholes.[5]
- Reacción con sales de ácido carboxílico y de ácido clorhídrico para dar las correspondientes cetona.[6]
- Reacción con ésteres carboxílicos para dar alcoholes terciarios. En el ejemplo adjunto, se demostró que el etilitio era muy eficaz, pero el bromuro de etilmagnesio dio principalmente productos de reducción.[7]
- Reacción con oximas para dar las correspondientes aminas.[5] .
- Reacción con isonitrilos para dar los correspondientes aldiminas de litio. La posterior hidrólisis efectivamente convierte el compuesto de organolitio en su aldehído.[8]
- Reacción con ciertos epóxidos para dar los correspondientes alquenos.[9]
Los reactivos de organolitio también reaccionan con los disolventes tipo éter que son muy usados en la mayoría de las reacciones. La tabla inferior muestra la vida media aproximada de varios compuestos de organilitio en disolventes típicos.:[10]
Disolvente/
Temperaturan-butillitio
( n-BuLi )s-butillitio
( s-BuLi )t-butillitio
( t-BuLi )metillitio
(MeLi )CH2=C(OEt)-Li CH2=C(SiMe3)-Li THF/-20 °C 40 min, 360 min THF/20 °C >15 hr 17 hr THF/35 °C 10 min THF/TMEDA/-20 °C 3300 min THF/TMEDA/ 0 °C 340 min THF/TMEDA/20 °C 40 min Éter/-20 °C 480 min Éter/0 °C 61 min Éter/20 °C 153 hr <30 min 17 days Éter/35 °C 31 hr Éter/TMEDA/ 20 °C 603 min DME/-70 °C 120 min 11 min DME/-20 °C 110 min 2 min <<2 min DME/0 °C 6 min Véase también
- Reactivo de Grignard
- Organometálico
Enlaces químicos del carbono con el resto de átomos
CH He CLi CBe CB CC CN CO CF Ne CNa CMg CAl CSi CP CS CCl CAr CK CCa CSc CTi CV CCr CMn CFe CCo CNi CCu CZn CGa CGe CAs CSe CBr CKr CRb CSr CY CZr CNb CMo CTc CRu CRh CPd CAg CCd CIn CSn CSb CTe CI CXe CCs CBa CHf CTa CW CRe COs CIr CPt CAu CHg CTl CPb CBi CPo CAt Rn Fr Ra Rf Db Sg Bh Hs Mt Ds Rg Uub Uut Uuq Uup Uuh Uus Uuo ↓ La CCe Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm CYb Lu Ac Th Pa CU Np Pu Am Cm Bk Cf Es Fm Md No Lr Enlaces químicos con carbono: Importancia relativa Química orgánica básica. Muchos usos en Química. Investigación académica,
pero no un amplio uso.Enlace desconocido /
no evaluado.Referencias
- ↑ Stent, M. (2002). «Generation of a Highly Basic and Nucleophilic Organolithium; Isopropyllithium». SyntheticPages (195). http://www.syntheticpages.org/browse.php?&action=1&page=6&id=195.
- ↑ Structure Formation Principles and Reactivity of Organolithium Compounds Viktoria H. Gessner, Christian Daschlein, and Carsten Strohmann Chem. Eur. J. 2009, 15, 3320 – 3334 doi 10.1002/chem.200900041
- ↑ Amanda C. Jones, Aaron W. Sanders, Martin J. Bevan, and Hans J. Reich (2007). «Reactivity of Individual Organolithium Aggregates: A RINMR Study of n-Butyllithium and 2-Methoxy-6-(methoxymethyl)phenyllithium» (Communication). J. Am. Chem. Soc. 129 (12): pp. 3492–3493. doi:.
- ↑ Wu, G. Huang, M. (2006). «Organolithium Reagents in Pharmaceutical Asymmetric Processes». Chemical Reviews 106: pp. 2596–2616. doi:.
- ↑ a b Advanced Organic Chemistry F.A. Carey R.J. Sundberg 2nd Edition ISBN 0-306-41088-5
- ↑ Thomas M. Bare and Herbert O. House (1973). "Methyl Ketones from Carboxylic Acids: Cyclohexyl Methyl Ketone". Org. Synth.; Coll. Vol. 5: 775.
- ↑ Posner, Gary H.; Jae Kyoo Lee, Qiang Wang, Sara Peleg, Martin Burke, Henry Brem, Patrick Dolan, Thomas W. Kensler (1998). «Noncalcemic, Antiproliferative, Transcriptionally Active, 24-Fluorinated Hybrid Analogues of the Hormone 1α,25-Dihydroxyvitamin D3. Synthesis and Preliminary Biological Evaluation». Journal of Medicinal Chemistry 41 (16): pp. 3008–3014. doi:.
- ↑ G. E. Niznik, W. H. Morrison, III, and H. M. Walborsky (1988). "1-d-Aldehydes from Organometallic Reagents: 2-Methylbutanal-1-d". Org. Synth.; Coll. Vol. 6: 751.
- ↑ David M. Hodgson, Philip G. Humphreys and Matthew J. Fleming (2008). "Organolithiums and Lithium 2,2,6,6-Tetramethylpiperidide in Reductive Alkylation of Epoxides: Synthesis of (E)-Alkenes". Org. Synth. 85: 1-9.
- ↑ Stanetty, P.; Koller, H.; Mihovilovic, M. (1992). «Directed Ortho-Lithiation of Phenylcarbamic Acid 1,l-Dimethylethyl Ester (N-Boc-aniline). Revision and Improvements». J. Org. Chem. 57: pp. 6833–6837. doi:.
Categoría:- Compuestos organometálicos
Wikimedia foundation. 2010.