- Activina e inhibina
-
inhibina, alfa HUGO 6065 Símbolo INHA Datos genéticos Locus Cr. 2 q33-qter Bases de datos Entrez 3623 OMIM 147380 RefSeq NM_002191 UniProt P05111 inhibina, beta A 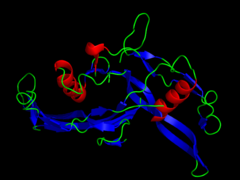
HUGO 6066 Símbolo INHBA Datos genéticos Locus Cr. 7 p15-p13 Bases de datos Entrez 3624 OMIM 147290 RefSeq NM_002192 UniProt P08476 inhibina, beta B HUGO 6067 Símbolo INHBB Datos genéticos Locus Cr. 2 cen-q13 Bases de datos Entrez 3625 OMIM 147390 RefSeq NM_002193 UniProt P09529 inhibina, beta C HUGO 6068 Símbolo INHBC Datos genéticos Locus Cr. 12 q13 Bases de datos Entrez 3626 OMIM 601233 RefSeq NM_005538 UniProt P55103 inhibina, beta E HUGO 24029 Símbolo INHBE Datos genéticos Locus Cr. 12 q13.2 Bases de datos Entrez 83729 OMIM 612031 RefSeq NM_031479 UniProt P58166 La activina e inhibina son dos complejos proteicos estrechamente relacionados que tienen efectos biológicos casi completamente opuestos. La activina aumenta la biosíntesis y secreción de la FSH, y participa en la regulación del ciclo menstrual. Se han encontrado muchas otras funciones ejercidas por la activina, incluyendo roles en la proliferación celular, diferenciación celular, apoptosis,[1] metabolismo, homeostasis, respuesta inmune, cicatrización,[2] y función endocrina. Por el contrario, la inhibina regula a la baja la síntesis de FSH e inhibe la secreción de FSH.[3]
La activina es un dímero compuesto por dos subunidades beta idénticas o muy similares. La inhibina también es un dímero en donde la primera componente es una subunidad beta similar o idéntica a la subunidad beta en la activina. Sin embargo, a diferencia con la activina, la segunda componente del dímero inhibina es más una lejanamente-relacionada subunidad alfa.[4] [5] La activina, inhibina, y un número de otras proteinas estructuralmente relacionadas tales como la hormona antimulleriana, proteína morfogénica ósea, y el factor de crecimiento de la diferenciación pertenecen a la superfamilia de proteínas TGF-β.[6]
Contenido
Estructura
Los complejos proteicos activina e inhibina son ambos diméricos en estructura, y, en cada complejo, dos monómeros están unidos entre sí por un enlace disulfuro.[7] Además, ambos complejos son derivados de la misma familia de genes y proteínas relacionada pero difieren en su composición subunitaria.[4] Abajo hay una lista de los complejos inhibina y activina más comunes y su composición subunitaria:
Clase Actividad Complejo Subunidades dímeras 1 2 Inhibina inhibe la secreción de FSH Inhibina A α Diagrama esquemático de las estructuras 1D de la inhibina y activina. La linea negra entre los monómeros representa un enlace disulfuro.
Las subunidades alfa y beta comparten una similitud de secuencia aproximadamente del 25%, mientras que la similitud entre las subinidades betas son aproximadamente del 65%.[6]
Se han descrito cuatro subunidades beta en mamíferos, llamadas called activina βA, activina βB, activina βC y activina βE. La activina βA y βB son idénticas a las dos subunidades beta de la inhibina. Se descrito una quinta subinidad, la activina βD, en Xenopus laevis.Dos subunidades activina βA dan origen a la activina A, una subunidad βA, y una βB dan origen a la activina AB, y así sucesivamente. Han sido descrito varios heterodímeros, pero no todos los teóricamente posibles.[8] [9] Las subunidades están unidas por un enlace covalente simple disulfuro.
La subunidad editar] Función
Activina
La activina es producida en las gónadas, glándula pituitaria, placenta, y otros órganos:
- En el folículo ovárico, la activina incrementa la unión de la FSH y la aromatización inducida por la FSH. Participa en la síntesis de andrógenos realzando la acción de la LH en el ovario y testículos. En el hombre, la activina realza la espermatogénesis.
- La activida es fuertemente expresada en las heridas de la piel, y la sobreexpresion de activina en la epidermis de ratones transgénicos mejora la curación de heridas y realza la formación de cicatriz. Su acción en la curación de heridas y morfogénesis de la piel es a través de la estimulación de queratinocito y células estromales de manera dosis-dependiente.[11]
- La activina también regula la morfogénesis de órganos de ramificación tales como la próstata y especialmente el riñón. La activina A incrementa los niveles de expresión de colágeno tipo I sugiriendo que la activina A actúa como un potente activador de fibroblastos.
- La falta de activina durante el desarrollo resulta en defectos de desarrollo neural.
Inhibina
En ambos mujeres y hombres, la inhibina inhibe la producción de FSH y la liberación de GnRH del hipotálamo. Sin embargo, el mecanismo en general difiere entre los géneros:
En mujeres
La inhibina es producida en las gónadas, glándula pituitaria, placenta, y otros órganos.
En las mujeres, la FSH estimula la secreción de inhibina de las células de granulosa del folículo ovárico en los ovarios. A su vez, la inhibina suprime la FSH.
- La inhibina B alcanza un máximo a principios y mediados de la fase folicular, y alcanza un segundo máximo en la ovulación.
- La inhibina A llega a su punto máximo a mediados de la fase lútea.
La secreción de inhibina es disminuida por la GnRH, e incrementada por el factor de crecimiento insulínico tipo 1 (IGF-1).
En hombres
La inhibina es secretada de las células de Sertoli,[12] ubicadas en los túbulos seminíferos dentro de los testículos. Los andrógenos estimulan la producción de inhibina; este péptido también podría regular localmente la espermatogénesis.
Mecanismo de acción
Activina
Al igual que otros miembros de la superfamilia, las activinas interactuan con dos tipos de receptores transmembranas (Tipo I y II) que tienen actividades serinas/treoninas kinasa intrínsecas en sus dominios citoplásmicos:
- Receptor de activina tipo 1: ACVR1, ACVR1B, ACVR1C
- Receptor de activina tipo 2: ACVR2A, ACVR2B
La activina se une al receptor tipo II e inicia una cascada de reacciones que llevan al reclutamiento, fosforilación, y activación del receptor de activina tipo I. Este luego interactúa con y luego fosforila la SMAD2 y SMAD3, dos de las proteínas citoplásmicas SMAD.
La SMAD3 luego se transloca al núcleo e interactúa con SMAD4 a través de multimerización, resultando en sus modulaciones como complejos de factores de transcripción responsables de la expresión de una gran variedad de genes.
Inhibina
A diferencia de la activina, se sabe mucho menos sobre el mecanismo de acción de la inhibina, pero podría involucrar la competición con la activina para unirse a los receptores de activina y/o unirse a receptores específicos de la inhibina.[5]
Significancía médica
La cuantificación de inhibina A es parte de la prueba prenatal triple test que se puede administrar durante el embarazo a una edad gestacional de 16-18 semanas. Una inhibina A elevada (junto con un aumento de beta-hCG, disminución de la AFP, y una disminución de estriol) es sugerente de la presencia de un feto con el síndrome de Down.[13] Como prueba de detección, los resultados anormales necesitan un seguimiento con pruebas más definitivas.
También se ha utilizado como un marcador de cáncer ovárico.[14] [15]
La inhibina B podría ser usada como marcador de la función espermatogénesis y esterilidad masculina. Los niveles promedio de inhibina B es significativamente mayor entre los hombres fértiles (aproximadamente 140 pg/mL) que los hombres estériles (aproximadamente 80 pg/mL).[16] En hombres con azoospermia, un test positivo para la inhibina B incrementa levemente las probabilidades de lograr un embarazo con éxito a través de la extracción de espermatozoides testiculares (TESE), aunque la asociación no es muy sustancial, teniendo una sensibilidad de 0,65 (95% intervalo de confianza [IC]: 0,56–0,74) y una especificidad de 0,83 (IC: 0,64–0,93) para la predicción de la presencia de espermatozoides en los testículos en azoospermia no obstructiva.[17]
Referencias
- ↑ Chen YG, Wang Q, Lin SL, Chang CD, Chuang J, Chung J, Ying SY (May 2006). «Activin signaling and its role in regulation of cell proliferation, apoptosis, and carcinogenesis». Exp. Biol. Med. (Maywood) 231 (5): pp. 534–44. PMID 16636301. http://www.ebmonline.org/cgi/pmidlookup?view=long&pmid=16636301.
- ↑ Sulyok S, Wankell M, Alzheimer C, Werner S (October 2004). «Activin: an important regulator of wound repair, fibrosis, and neuroprotection». Mol. Cell. Endocrinol. 225 (1-2): pp. 127–32. doi:. PMID 15451577.
- ↑ van Zonneveld P, Scheffer G, Broekmans F, Blankenstein M, de Jong F, Looman C, Habbema J, te Velde E (2003). «Do cycle disturbances explain the age-related decline of female fertility? Cycle characteristics of women aged over 40 years compared with a reference population of young women». Hum Reprod 18 (3): pp. 495–501. doi:. PMID 12615813.
- ↑ a b Burger HG, Igarashi M (April 1988). «Inhibin: definition and nomenclature, including related substances». The Journal of Clinical Endocrinology and Metabolism 66 (4): pp. 885–6. PMID 3346366.
- ↑ a b Robertson DM, Burger HG, Fuller PJ (March 2004). «Inhibin/activin and ovarian cancer». Endocrine-related Cancer 11 (1): pp. 35–49. doi:. PMID 15027884.
- ↑ a b Kingsley DM (January 1994). «The TGF-beta superfamily: new members, new receptors, and new genetic tests of function in different organisms». Genes & Development 8 (2): pp. 133–46. doi:. PMID 8299934.
- ↑ Ying SY (December 1987). «Inhibins and activins: chemical properties and biological activity». Proc. Soc. Exp. Biol. Med. 186 (3): pp. 253–64. PMID 3122219.
- ↑ Xu P, Hall AK (November 2006). «The role of activin in neuropeptide induction and pain sensation». Dev. Biol. 299 (2): pp. 303–9. doi:. PMID 16973148.
- ↑ Deli A, Kreidl E, Santifaller S, Trotter B, Seir K, Berger W, Schulte-Hermann R, Rodgarkia-Dara C, Grusch M (March 2008). «Activins and activin antagonists in hepatocellular carcinoma». World J. Gastroenterol. 14 (11): pp. 1699–709. doi:. PMID 18350601. PMC 2695910. http://www.wjgnet.com/1007-9327/14/1699.asp.
- ↑ Mellor SL, Cranfield M, Ries R, Pedersen J, Cancilla B, de Kretser D, Groome NP, Mason AJ, Risbridger GP (December 2000). «Localization of activin beta(A)-, beta(B)-, and beta(C)-subunits in humanprostate and evidence for formation of new activin heterodimers of beta(C)-subunit». The Journal of Clinical Endocrinology and Metabolism 85 (12): pp. 4851–8. doi:. PMID 11134153.
- ↑ Bamberger C, Schärer A, Antsiferova M, Tychsen B, Pankow S, Müller M, Rülicke T, Paus R, Werner S (September 2005). «Activin controls skin morphogenesis and wound repair predominantly via stromal cells and in a concentration-dependent manner via keratinocytes». Am. J. Pathol. 167 (3): pp. 733–47. PMID 16127153. PMC 1698729. http://ajp.amjpathol.org/cgi/pmidlookup?view=long&pmid=16127153.
- ↑ Skinner M, McLachlan R, Bremner W (1989). «Stimulation of Sertoli cell inhibin secretion by the testicular paracrine factor PModS». Mol Cell Endocrinol 66 (2): pp. 239–49. doi:. PMID 2515083.
- ↑ Citación Publicación | autor = Aitken D, E Wallace, Crossley J., Swanston I, van Pareren Y, van Maarle M, Groome N, Macri J, Camilo J título | = inhibina dimérica, como marcador para el síndrome de Down en el embarazo temprano Publicación | = N Engl J Med | volumen = 334 Número | = 19 | páginas = Año | 1231-6 = 1996 PMID | url = 8606718 | = http://content.nejm.org/cgi/content/short/334/ 19/1231
- ↑ Robertson D, Pruysers E, Jobling T (2007). «Inhibin as a diagnostic marker for ovarian cancer». Cancer Lett 249 (1): pp. 14–7. doi:. PMID 17320281.
- ↑ Robertson D, Pruysers E, Burger H, Jobling T, McNeilage J, Healy D (2004). «Inhibins and ovarian cancer». Mol Cell Endocrinol 225 (1-2): pp. 65–71. doi:. PMID 15451569.
- ↑ Myers GM, Lambert-Messerlian GM, Sigman M (November 2008). «Inhibin B reference data for fertile and infertile men in Northeast America». Fertil. Steril. 92 (6): pp. 1920–3. doi:. PMID 19006797.
- ↑ Por favor, pon la referencia que aparece aquí.
Enlaces externos
Wikimedia foundation. 2010.
Mira otros diccionarios:
Hormona antimulleriana — Hormona anti mulleriana HUGO 464 Símbolo AMH Símbolos alt. MIS … Wikipedia Español
Sistema endocrino — Glándulas endocrinas importantes. (masculino a la izquierda, femenino a la derecha): 1. Glándula pineal, 2. Glándula pituitaria, 3. Glándula tiroides, 4. Timo, 5. Glándula adrenal, 6. Páncreas, 7. Ovario, 8 … Wikipedia Español
Hormona antidiurética — Vasopresina (Hormona antidiurética) Modelo tridimensional de la vasopresina HUGO 894 … Wikipedia Español
Adrenalina — Para otros usos de este término, véase Adrenalina (desambiguación). Adrenalina … Wikipedia Español
Aldosterona — Nombre (IUPAC) sistemático a Identificadores … Wikipedia Español
Cortisol — Nombre (IUPAC) sistemático … Wikipedia Español
Estradiol — Nombre (IUPAC) sistemático … Wikipedia Español
Factor de crecimiento insulínico tipo 1 — (somatomedina C) HUGO 5464 … Wikipedia Español
Somatostatina — HUGO 11329 Símbolo … Wikipedia Español
Gastrina — Este artículo o sección sobre medicina y biología necesita ser wikificado con un formato acorde a las convenciones de estilo. Por favor, edítalo para que las cumpla. Mientras tanto, no elimines este aviso puesto el 31 de mayo de 2010. También… … Wikipedia Español
