- Hormona del crecimiento
-
Hormona del crecimiento 1
Hormona del crecimientoHUGO 4261 Símbolo GH1 Datos genéticos Locus Cr. 17 q22-q24 Bases de datos Entrez 2688 OMIM 139250 RefSeq NM_022562 UniProt P01241 Hormona del crecimiento 2 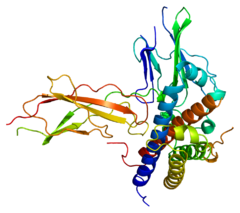
Estructura de la proteína GH2HUGO 4262 Símbolo GH2 Datos genéticos Locus Cr. 17 q22-q24 Bases de datos Entrez 2689 OMIM 139240 RefSeq NM_002059 UniProt P01242 La hormona del crecimiento (GH, del inglés: growth hormone) es una hormona peptídica a base de proteínas. La GH estimula el crecimiento, reproducción celular, y la regeneración en humanos y otros animales. La hormona de crecimiento es un polipéptido de 191 aminoácidos de una sola cadena sintetizada, almacenada, y secretada por las células somatotropas dentro de las alas laterales de la adenohipófisis. El término somatotropina se refiere a la hormona del crecimiento 1 producida naturalmente por los animales, mientras que el término somatropina se refiere a la hormona del crecimiento producida por la tecnología ADN recombinante,[1] y en humanos es abreviada "HGH".
La hormona del crecimiento es usada como medicamento con receta para tratar los trastornos de crecimiento en los niños y en adultos para tratar la deficiencia de GH. En años recientes en los Estados Unidos, algunos doctores han empezado a prescribir hormona del crecimiento a pacientes de edad con deficiencia de GH (pero no en personas saludables) para incrementar la vitalidad. Es legal, pero su eficacia y seguridad para este uso no ha sido probada en ningún ensayo clínico. En este momento, la hGH todavía se considera una hormona muy compleja, y muchas de sus funciones aún se desconocen.[2]
La GH ha sido estudiada para criar el ganado de manera más eficiente en la agricultura industrial y se han hecho varios esfuerzos para obtener una aprobación gubernamental para usar la GH en la producción ganadera. Estos usos han sido controversiales. En los Estados Unidos, el único uso de GH aprobado por la FDA es el uso de la forma exclusiva de GH para las vacas llamada somatotropina bovina, para aumentar la producción lechera de las vacas lecheras. Ahora se les permite a los comerciantes etiquetar los envases de leche como leche producida con o sin somatotropina bovina.
Contenido
Biología
Locus del gen
Los genes de la hormona del crecimiento, conocidos como hormona del crecimiento 1 (somatotropina) y hormona del crecimiento 2, están localizados en la región q22-24 del cromosoma 17[3] [4] y están estrechamente relacionados con los genes somatomamotropina coriónica humana (también conocida como lactógeno placentario). La GH, somatomamotropina coriónica humana, y prolactina pertenecen a un grupo de hormonas homologas con actividades lactogénicas y promotoras del crecimiento.
Estructura
El isoforma principal de la hormona del crecimiento es una proteína de 191 aminoácidos con un peso molecular de 22.124 daltons. La estructura incluye cuatro hélices, necesarias para la interacción funcional con el receptor de GH. Parece que, en su estructura, la GH es evolutivamente homóloga a la prolactina y somatomamotropina coriónica. A pesar de las marcadas similitudes estructurales entre las hormonas del crecimiento de diferentes especies, sólo la hormona del crecimiento humana y la de los primates tienen efectos significativos en humanos.
Existen varias isoformas moleculares de GH en la glándula pituitaria que son liberadas al torrente sanguíneo. En particular, una variante de aproximadamente 20 kDa originada por un splicing alternativo está presente en una proporción de 1:9 bastante constante,[5] mientras que recientemente una variante de ~ 23-24 kDa también ha sido encontrada en estados de post-ejercicio en proporciones más altas.[6] Esta variante no ha sido identificada, pero ha sido sugerido de coincidir con una variante glicosilada de 22 kDa de una de 23 kDa identificada en la glándula pituitaria.[7] Además, estas variantes circulan unidas parcialmente a una proteína (proteína fijadora de la hormona del crecimiento, GHBP), que es la parte truncada del receptor de la hormona del crecimiento, y una subunidad ácido-lábil (ALS).
Regulación biológica
Los péptidos liberados por los núcleos neurosecretores del hipotálamo (Hormona liberadora de la hormona del crecimiento/somatocrinina y Hormona inhibidora de la hormona del crecimiento/somatostatina) en la sangre venosa del portal hipofisiario rodeando la pituitaria son los principales controladores de la secreción de GH por las somatotropas. Sin embargo, aun cuando el balance de estos péptidos estimulantes e inhibidores determinan la secreción de la GH, este equilibrio se ve afectado por muchos estimuladores fisiológicos (por ejemplo, ejercicio, nutrición, sueño) e inhibidores de la secreción de GH (por ejemplo, ácidos grasos libres)[8]
Los estimuladores de la secreción de hGH incluyen:- hormonas peptídicas
- hormonas sexuales[11]
- el incremento en la secreción de andrógenos durante la pubertad (en los varones de los testículos y en las mujeres de corteza suprarrenal)
- estrógenos
- clonidina y levodopa al estimular la liberación de GHRH[12]
- hipoglucemia, arginina[13] y el propranolol al inhibir la liberación de somatostatina.[12]
- sueño de ondas lentas[14]
- ayuno[15]
- ejercicio vigoroso[16]
Los inhibidores de la secreción de hGH incluyen:
- somatostatina del núcleo periventricular[17]
- concentraciones circulantes de GH e IGF-1 (feedback negativo en la pituitaria e hipotálamo)[2]
- hiperglucemia[12]
- glucocorticoides[18]
- dihidrotestosterona
Además del control por parte de los procesos endógenos y estimulantes, un número de compuestos extranjeros al cuerpo (xenobióticos como medicamentos y disruptores endocrinos) son conocidos por influenciar la secreción y función de la GH.[19]
La HGH es sintetizada y secretada por la glándula adenohipófisis de manera pulsativa durante todo el día; con oleadas de secreción ocurriendo en intervalos de 3 a 5 horas.[2] Las concentración de GH en el plasma sanguíneo durante estos picos pueden variar de 5 a 45 ng/mL.[20] El pico de GH más grande y predecible ocurre alrededor de una hora después del comienzo del sueño.[21] De lo contrario existe una amplia variación entre los días y las personas. Cerca del cincuenta por ciento de las secreciones de HGH ocurre durante la tercera y cuarta etapa del sueño REM.[22] Entre los picos, los niveles basales de GH son bajos, usualmente menos de 5 ng/mL durante la mayoría del día y noche.[21] Un análisis adicional del perfil pulsátil de la GH mostró en todos los casos menos de 1 ng/ml para los niveles basales mientras que los picos máximos estaban alrededor de 10-20 ng/mL.[23] [24]
Una serie de factores son conocidos por afectar la secreción de HGH, tales como la edad, sexo, dieta, ejercicio, estrés, y otras hormonas.[2] Los adolescentes jovenes secretan HGH a una tasa de alrededor de 700 μg/día, mientras que un adulto saludable secreta HGH a una tasa de alrededor de 400 μg/día.[25]
Función normal de la GH producida por el cuerpo
Los efectos de la hormona del crecimiento pueden ser descritos de forma general como anabólicos. Como la mayoría de las otras hormonas proteicas, la GH actúa interactuando con un receptor especifico en la superficie de las células.
El incremento de la altura durante la infancia es el efecto más conocido de la GH. La altura aparenta ser estimulada por al menos dos mecanismos:
- Ya que las hormonas polipéptidas no son soluble en la grasa, no pueden penetrar la sarcolema. Por ello la GH ejerce una parte de sus efectos al unirse con los receptores de las células objetivo, donde activa la vía MAPK/ERK.[26] A través de este mecanismo la GH estimula directamente la división y multiplicación de los condrocitos del cartílago.
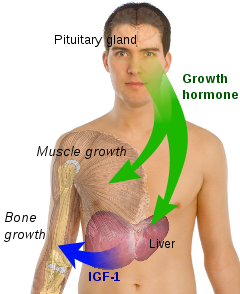
- La GH también estimula la producción del factor de crecimiento insulínico tipo 1 (IGF-1, antiguamente conocido como somatomedina C) a través de la ruta de señalización JAK-STAT,[26] la IGF-1 es una hormona homologa a la proinsulina.[27] El hígado es el órgano objetivo principal de la GH para este proceso y es el sitio principal de la producción de IGF-1. El IGF-1 tiene efectos estimulantes del crecimiento en una amplia variedad de tejidos. El IGF-1 también es generada dentro del tejido objetivo, haciendo el IGF-1 lo que parece ser una hormona endocrina y autocrina/paracrina. El IGF-1 también tiene efectos estimulantes en la actividad de los osteoblastos y condrocitos para promover el crecimiento óseo.
Además de aumentar la altura en niños y adolescentes, la hormona del crecimiento tiene muchos otros efectos en el cuerpo:
- Incrementa la retención de calcio y la mineralización de los huesos
- Incrementa la masa muscular a través de la hiperplasia sarcómera
- Promueve la lipolisis
- Incrementa la biosíntesis proteica
- Estimula el crecimiento de todos los órganos internos excluyendo al cerebro
- Juega un rol en la homeostasis
- Reduce el consumo de glucosa del hígado
- Promueve la gluconeogénesis en el hígado[28]
- Contribuye al mantenimiento y función de lo islotes pancreáticos
- Estimula el sistema inmune
Problemas causados cuando el cuerpo produce demasiada GH
La enfermedad más común de exceso de GH se debe a un tumor en la pituitaria compuesta por células somatotrofas de la adenohipófisis. Estas adenomas somatotrofas son benignas y crecen lentamente, gradualmente produciendo más y más HG. Por años, el problema clínico principal es el exceso de GH. Eventualmente, el adenoma podría hacerse lo suficientemente grande para causar dolores de cabeza, perjudicar la visión por la presión sobre los nervios ópticos, o causar deficiencia de otras hormonas pituitarias.
El exceso prolongado de GH engruesa los huesos de la mandíbula, y los dedos de pies y manos. Resultando en una pesadez mandibular y un aumento en el tamaño de los dedos (acromegalia). Problemas acompañantes pueden incluir sudoración, presión sobre nervios (por ejemplo, síndrome del túnel carpiano), debilidad muscular, exceso de globulina fijadora de hormonas sexuales (SHBG), resistencia a la insulina o incluso una extraña forma de diabetes mellitus tipo 2, y reducción de la función sexual.
Los tumores secretores de GH son típicamente reconocidos durante la quinta década de vida. Es extremadamente raro que tal tumor ocurra durante la infancia, pero, cuando lo hace, el exceso de GH puede causar un crecimiento excesivo, tradicionalmente referido como gigantismo pituitario.
La extirpación quirúrgica es usualmente el tratamiento para los tumores productores de GH. En algunas circunstancias, se podria emplear radiación enfocada o antagonistas de GH para reducir el tamaño del tumor o bloquear su función. Tambien se podria usar otros medicamentos como el octreotide (agonista de somatostatina) y bromocriptina (agonista de dopamina) para bloquear la secreción de GH ya que tanto la somatostatina como la dopamina inhiben la liberacion de GH de la adenohipófisis.
Problemas causados cuando el cuerpo produce poca GH
Los efectos de la deficiencia de la hormona del crecimiento (GHD) varían dependiendo en la edad en la que se producen. En niños, las manifestaciones principales de la deficiencia de GH son la falta de crecimiento y baja estatura, con causas comunes incluyendo condiciones genéticas y malformaciones congénitas. También puede causar demoras en la maduración sexual. En adultos, la deficiencia es rara,[29] con la causa más común siendo un adenoma pituitario, y otros incluyendo una continuación de un problema de la niñez, lesiones o traumas estructurales, y GHD idiopáticas muy raras.
Los adultos con GHD presentan problemas no específicos incluyendo obesidad troncal con una disminución relativa de masa muscular, y en muchas instancias, una disminución en la energía y calidad de vida.[29]
El diagnosis de la deficiencia de GH involucra un proceso de diagnostico de múltiples pasos, usualmente culminando en pruebas de estimulación de GH para ver si la glándula pituitaria del paciente libera GH cuando esta es provocada por varios estímulos.
GH en la medicina humana
Vea la sección de arriba para los problemas causados cuando el cuerpo produce demasiada o muy poca GH.
Tratamientos con GH relacionados con la deficiencia de GH
El tratamiento con GH exógena es sólo indicado en determinadas circunstancias,[29] y necesita un seguimiento regular debido a la frecuencia y gravedad de sus efectos secundarios. La GH es usada en terapias de reemplazo en adultos con deficiencia de GH. En estos pacientes, lo beneficios incluyen una reducción de la masa grasa, aumento de la masa magra, aumento de la densidad ósea, mejoras en el perfil lipídico, reducción en factores de riesgo cardiovascular, y mejoras en el bienestar psicológico.
Tratamientos con GH no relacionados con la deficiencia de GH
La GH puede ser usada para tratar condiciones que produzcan una baja estatura pero que no estén relacionadas con una deficiencia de GH. Sin embargo, los resultados no son tan dramáticos cuando son comparados con las estaturas bajas atribuibles a una deficiencia de GH. Ejemplos de otras causas de baja estatura que a menudo son tratadas con GH incluye el síndrome de Turner, enfermedad renal crónica, síndrome de Prader-Willi, restricción del crecimiento intrauterino, y baja estatura idiopática severa. Se requieren dosis altas para producir una aceleración significativa del crecimiento bajo estas condiciones, produciendo niveles sanguíneos más altos que los niveles fisiológicos normales. A pesar de las dosis altas, los efectos secundarios durante el tratamiento son raros, y varían dependiendo de la condición siendo tratada.
Usos experimentales
La siguiente discusión describe el uso experimental de la GH, que es legal cuando la GH es prescrita por un doctor. Sin embargo, la eficacia y seguridad del uso de GH como agente anti-envejecimiento son desconocidas ya que este uso no ha sido probada en ningun ensayo clínico doble ciego.
En años recientes en los Estados Unidos, algunos doctores han empezado a prescribir hormona del crecimiento en pacientes de edad con deficiencia de GH (pero no en personas saludables) para incrementar la vitalidad. Es legal, pero su eficacia y seguridad para este uso no ha sido probada en ningún ensayo clínico. En este momento, la hGH todavía se considera una hormona muy compleja, y muchas de sus funciones aún se desconocen.[2]
Las reclamaciones de la GH como agente anti-envejecimiento datan de 1990 cuando el New England Journal of Medicine (Revista de Medicina de Nueva Inglaterra) publicó un estudio donde la GH fue usada para trata a 12 hombres con sobre 60 años de edad.[30] Al término del estudio, todos los hombres mostraron un incremento de masa magra y mineral óseo estadísticamente significativo, mientras que el grupo control no. Los autores del estudio notaron que estas mejoras eran opuestas a los cambios que normalmente ocurren en un periodo de envejecimiento de 10 a 20 años. A pesar de que los autores nunca afirmaron que la GH había revertido el proceso del envejecimiento, los resultados fueron malinterpretados indicando que la GH era un agente anti-envejecimiento.[31] [32] [33] Esto ha llevado a organizaciones tales como la controvertida American Academy of Anti-Aging Medicine (Academia Americana de Medicina Anti-Envejecimiento) a promover el uso de esta hormona como "agente anti-envejecimiento".[34]
La Facultad de Medicina de la Universidad de Standford hizo análisis de los estudios clínicos respecto al tema, publicado a principio de 2007, mostró que la aplicación de GH en pacientes de edad avanzada aumentó la masa muscular alrededor de 2 kg y disminuyó la grasa corporal alrededor de la misma cantidad.[31] Sin embargo, estos fueron los únicos efectos positivos de la administración de GH. Ningún otro factor crítico fue afectado, tal como la densidad ósea, niveles de colesterol, perfil lipídico, consumo máximo de oxígeno, o cualquier otro factor que podría indicar un aumento de la aptitud física.[31] Los investigadores tampoco descubrieron ninguna ganancia en la fuerza muscular, que los llevaron a creer que la GH simplemente permitió que el cuerpo almacenara más agua en el tejido muscular en vez de aumentar el crecimiento muscular. Esto podría explicar el incremento de la masa magra.
La GH también ha sido usada experimentalmente para tratar la esclerosis múltiple, para mejorar la pérdida de peso en pacientes obesos, como también en fibromialgia, insuficiencia cardíaca, enfermedad de Crohn, colitis ulcerosa, y quemaduras. La GH también ha sido usada para mantener la masa muscular en pacientes con SIDA y con síndrome del intestino corto para reducir la obligación de nutrición parenteral.
Efectos secundarios
La GH es un medicamento aprobado por la FDA para tratar varias condiciones. Esto significa que este medicamento tiene una seguridad aceptable a la luz de sus beneficios cuando este es usado de manera correcta. Como todos los medicamentos, existen varios efectos secundarios causados por la GH, algunos comunes, otros raros. Reacción en la zona de inyección es común. Con menos frecuencia, los pacientes pueden experimentar inflamación de las articulaciones, dolor en las articulaciones, síndrome del túnel carpiano, y un mayor riesgo de diabetes.[31] Otros efectos secundarios pueden incluir necesitar menos sueño después de una dosis. Esto es común inicialmente y disminuye en efecto después del uso habitual de GH.
Una encuesta de adultos que habían sido tratados con remplazo de GH de cadáver (que no había sido usada en ninguna parte del mundo desde 1985) durante la infancia mostraron un leve incremento en la incidencia de cáncer de colon y cáncer de próstata, pero el vinculo con el tratamiento de GH no fue establecido.[35]
Uso no médico para la mejora atlética
Varios deportistas en muchos deportes han usado la hormona del crecimiento para intentar mejorar su rendimiento deportivo. Algunos estudios recientes no han sido capaces de acreditar que la hormona del crecimiento puede mejorar el rendimiento deportivo de hombres atletas profesionales.[36] [37] [38] Muchas sociedades atléticas prohiben el uso de GH y emitirán sanciones contra los atletas que sean encontrados usándola. En los Estados Unidos, la GH está legalmente disponible bajo prescripción médica. La Hormona de Crecimiento no beneficia en el rendimiento y/o desempeño de los atletas. No hay estudio que acredite que la GH beneficie en el rendimiento y capacidad de ejercitación del atleta.
Uso de la GH en la producción de carne y leche
En los Estados Unidos, es legal darle GH bovina a vacas lecheras para incrementar la producción de leche, pero no es legal usar la GH para la producción de carne de vacuno; véase el artículo somatotropina bovina.
Varias compañías han intentado tener una versión de la GH para su uso en cerdos (somatotropina porcina) aprobada por la FDA, pero todas las aplicaciones han sido retiradas.[39] [40]
Historia del uso y manufactura de la GH como medicamento
La identificación, purificación y posterior síntesis de la hormona del crecimiento está asociada con el bioquímico Choh Hao Li. Genentech fue el primero en usar la hormona del crecimiento recombinante para terapias humanas en 1981.
Anterior a la producción a través de la tecnología ADN recombinante, la hormona del crecimiento usada para tratar las deficiencias era extraída de la glándula pituitaria de cadáveres. Los intentos de crear una HGH totalmente sintética fallaron. Los suministros limitados de HGH resultaron en restricciones para las terapias de HGH para tratar la estatura baja idiopática.[41] Por otra parte, la hormona del crecimiento de otros primates fue encontrada ser inactiva en humanos.[42]
En 1985, casos inusuales de la enfermedad de Creutzfeldt-Jakob fueron encontrados en individuos quienes habían recibido HGH de cadáveres 10 a 15 años antes. Basados en la asunción que los priones infecciosos que causan la enfermedad fueron transferidos junto con la HGH de cadáveres, la HGH derivada de cadáveres fue removida del mercado.[25]
En 1985, la hormona del crecimiento biosintética reemplazó la hormona del crecimiento derivada de la pituitaria para uso terapéutico en los Estados Unidos y en otras partes.
A partir de 2005, la hormona del crecimiento recombinante disponible en los Estados Unidos (y sus fabricantes) incluyen a Nutropin (Genentech), Humatrope (Lilly), Genotropin (Pfizer), Norditropin (Novo), y Saizen (Merck Serono). En 2006, la FDA aprobó una versión de HGH recombinante llamada Omnitrope (Sandoz). Una forma de liberación sostenida de GH, Nutropin Depot (Genentech y Alkermes) fue aprobada por la FDA en 1999, permitiendo menos inyecciones (cada 2 a 4 semanas en ves de inyecciones diarias); sin embargo, el producto fue descontinuado por Genentech/Alkermes en 2004 por razones financieras (Nutropin Depot requería muchos más recursos para producir que el resto de la línea Nutropin[43] ).
Suplementos alimenticios que afirman relación con la GH
Para capitalizar la idea que la GH puede ser utilizada para combatir el envejecimiento ha entrado en la cultura estadounidense, las empresas que venden suplementos dietéticos tienen sitios web vendiendo productos vinculados con la GH en el texto publicitario, con nombres que parecieran médicas como "Liberadores de HGH". Los ingredientes típicos incluyen aminoácidos, minerales, vitaminas, y/o extractos hierbas, cuya combinación es descrita de causar el cuerpo a producir más GH con los correspondientes efectos beneficiosos. En los Estados Unidos, debido que estos productos son comercializados como suplementos dietéticos, es ilegal que estos contengan GH, que es un medicamento. También, bajo la ley estadounidense, los productos que se vendan como suplementos dietéticos no pueden afirmar que el suplemento trate o prevenga ningún tipo de enfermedad o condición, y el texto publicitario debe contener una declaración que las afirmaciones dichas en el texto no están aprobadas por la FDA. La FTC y FDA hacen cumplir la ley cuando se dan cuenta de cualquier tipo de violación.[44]
Véase también
- Factor de crecimiento insulínico
- IGF-1
- IGF-2
- Deficiencia de la hormona de crecimiento
- Somatotropina
- Somatostatina
- Enanismo
- Acromegalia
- Hormona del crecimiento y otras hormonas
Referencias
- ↑ Daniels ME (1992). «Lilly's Humatrope Experience». Nature Biotechnology 10 (7): pp. 812. doi:.
- ↑ a b c d e Powers M (2005). «Performance-Enhancing Drugs». En Deidre Leaver-Dunn; Joel Houglum; Harrelson, Gary L.. Principles of Pharmacology for Athletic Trainers. Slack Incorporated. pp. 331–332. ISBN 1-55642-594-5.
- ↑ «GH1 growth hormone 1 (Homo sapiens) - Gene». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ «GH2 growth hormone 2 (Homo sapiens) - Gene». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ Leung KC, Howe C, Gui LY, Trout G, Veldhuis JD, Ho KK (October 2002). «Physiological and pharmacological regulation of 20-kDa growth hormone». Am. J. Physiol. Endocrinol. Metab. 283 (4): pp. E836–43. doi:. PMID 12217902.
- ↑ Kohler M, Püschel K, Sakharov D, Tonevitskiy A, Schänzer W, Thevis M (November 2008). «Detection of recombinant growth hormone in human plasma by a 2-D PAGE method». Electrophoresis 29 (22): pp. 4495–502. doi:. PMID 19003817.
- ↑ Bustamante JJ, Gonzalez L, Carroll CA, Weintraub ST, Aguilar RM, Muñoz J, Martinez AO, Haro LS (July 2009). «O-Glycosylated 24 kDa human growth hormone has a mucin-like biantennary disialylated tetrasaccharide attached at Thr-60». Proteomics 9 (13): pp. 3474–88. doi:. PMID 19579232.
- ↑ Bartholomew, Edwin F.; Martini, Frederic; Judi Lindsley Nath (2009). Fundamentals of anatomy & physiology. Upper Saddle River, NJ: Pearson Education Inc. pp. 616–617. ISBN 0-321-53910-9.
- ↑ Lin-Su K, Wajnrajch MP (December 2002). «Growth Hormone Releasing Hormone (GHRH) and the GHRH Receptor». Rev Endocr Metab Disord 3 (4): pp. 313–23. doi:. PMID 12424433.
- ↑ Wren AM, Small CJ, Ward HL, Murphy KG, Dakin CL, Taheri S, Kennedy AR, Roberts GH, Morgan DG, Ghatei MA, Bloom SR (November 2000). «The novel hypothalamic peptide ghrelin stimulates food intake and growth hormone secretion». Endocrinology 141 (11): pp. 4325–8. doi:. PMID 11089570.
- ↑ Meinhardt UJ, Ho KK (October 2006). «Modulation of growth hormone action by sex steroids». Clin. Endocrinol. (Oxf) 65 (4): pp. 413–22. doi:. PMID 16984231.
- ↑ a b c Low LC (1991). «Growth hormone-releasing hormone: clinical studies and therapeutic aspects». Neuroendocrinology 53 Suppl 1: pp. 37–40. PMID 1901390.
- ↑ Alba-Roth J, Müller OA, Schopohl J, von Werder K (December 1988). «Arginine stimulates growth hormone secretion by suppressing endogenous somatostatin secretion». J. Clin. Endocrinol. Metab. 67 (6): pp. 1186–9. doi:. PMID 2903866.
- ↑ Van Cauter E, Latta F, Nedeltcheva A, Spiegel K, Leproult R, Vandenbril C, Weiss R, Mockel J, Legros JJ, Copinschi G (June 2004). «Reciprocal interactions between the GH axis and sleep». Growth Horm. IGF Res. 14 Suppl A: pp. S10–7. doi:. PMID 15135771.
- ↑ Nørrelund H (April 2005). «The metabolic role of growth hormone in humans with particular reference to fasting». Growth Horm. IGF Res. 15 (2): pp. 95–122. doi:. PMID 15809014.
- ↑ Kanaley JA, Weltman JY, Veldhuis JD, Rogol AD, Hartman ML, Weltman A (November 1997). «Human growth hormone response to repeated bouts of aerobic exercise». J. Appl. Physiol. 83 (5): pp. 1756–61. PMID 9375348. http://jap.physiology.org/cgi/content/full/83/5/1756.
- ↑ Guillemin R, Gerich JE (1976). «Somatostatin: physiological and clinical significance». Annu. Rev. Med. 27: pp. 379–88. doi:. PMID 779605.
- ↑ Allen DB (September 1996). «Growth suppression by glucocorticoid therapy». Endocrinol. Metab. Clin. North Am. 25 (3): pp. 699–717. doi:. PMID 8879994.
- ↑ Scarth JP (2006). «Modulation of the growth hormone-insulin-like growth factor (GH-IGF) axis by pharmaceutical, nutraceutical and environmental xenobiotics: an emerging role for xenobiotic-metabolizing enzymes and the transcription factors regulating their expression. A review». Xenobiotica 36 (2–3): pp. 119–218. doi:. PMID 16702112.
- ↑ Natelson BH, Holaday J, Meyerhoff J, Stokes PE (August 1975). «Temporal changes in growth hormone, cortisol, and glucose: relation to light onset and behavior». Am. J. Physiol. 229 (2): pp. 409–15. PMID 808970. http://ajplegacy.physiology.org/cgi/content/abstract/229/2/409.
- ↑ a b Takahashi Y, Kipnis D, Daughaday W (1968). «Growth hormone secretion during sleep». J Clin Invest 47 (9): pp. 2079–90. doi:. PMID 5675428.
- ↑ Mehta Ameeta, Hindmarsh Peter (2002). «The use of somatropin (recombinant growth hormone) in children of short stature». Pediatric Drugs 4 (1): pp. 37–47. PMID 11817985.
- ↑ Nindl BC, Hymer WC, Deaver DR, Kraemer WJ (1 de julio de 2001). «Growth hormone pulsatility profile characteristics following acute heavy resistance exercise». J. Appl. Physiol. 91 (1): pp. 163–72. PMID 11408427. http://jap.physiology.org/cgi/content/abstract/91/1/163.
- ↑ Juul A, Jørgensen JO, Christiansen JS, Müller J, Skakkeboek NE (1995). «Metabolic effects of GH: a rationale for continued GH treatment of GH-deficient adults after cessation of linear growth». Horm. Res. 44 Suppl 3 (3): pp. 64–72. doi:. PMID 8719443.
- ↑ a b Gardner, David G., Shoback, Dolores (2007). Greenspan's Basic and Clinical Endocrinology (8th edición). New York: McGraw-Hill Medical. pp. 193–201. ISBN 0-07-144011-9.
- ↑ a b Binder G, Wittekindt N, Ranke MB (February 2007). «Noonan Syndrome: Genetics and Responsiveness to Growth Hormone Therapy». Horm Res 67 (Supplement 1): pp. 45–49. doi:. ISBN 9783805582551. http://books.google.com/?id=nQ9ilbixQEgC&pg=PA46&lpg=PA46&dq=gh+growth+hormone+ras&q=gh%20growth%20hormone%20ras.
- ↑ «Actions of Anterior Pituitary Hormones: Physiologic Actions of GH». Medical College of Georgia (2007). Consultado el 16-01-2008.
- ↑ King, MW (2006). «Structure and Function of Hormones: Growth Hormone». Indiana State University. Consultado el 16-01-2008.
- ↑ a b c Molitch ME, Clemmons DR, Malozowski S, Merriam GR, Shalet SM, Vance ML; Endocrine Society's Clinical Guidelines Subcommittee, Stephens PA (May 2006). «Evaluation and treatment of adult growth hormone deficiency: an Endocrine Society Clinical Practice Guideline». J. Clin. Endocrino. Metab. 91 (5): pp. 1621–34. doi:. PMID 16636129.
- ↑ Rudman D, Feller AG, Nagraj HS, Gergans GA, Lalitha PY, Goldberg AF, Schlenker RA, Cohn L, Rudman IW, Mattson DE (July 1990). «Effects of human growth hormone in men over 60 years old». N. Engl. J. Med. 323 (1): pp. 1–6. doi:. PMID 2355952.
- ↑ a b c d Liu H, Bravata DM, Olkin I, Nayak S, Roberts B, Garber AM, Hoffman AR (January 2007). «Systematic review: the safety and efficacy of growth hormone in the healthy elderly». Ann. Intern. Med. 146 (2): pp. 104–15. PMID 17227934.
- ↑ «No proof that growth hormone therapy makes you live longer, study finds». PhysOrg.com (16-01-2007). Consultado el 16-03-2009.
- ↑ Stephen Barrett, M.D. Growth Hormone Schemes and Scams
- ↑ Kuczynski, Alex. «Anti-Aging Potion or Poison?», New York Times, 12-04-1998.
- ↑ Swerdlow AJ, Higgins CD, Adlard P, Preece MA (July 2002). «Risk of cancer in patients treated with human pituitary growth hormone in the UK, 1959-85: a cohort study». Lancet 360 (9329): pp. 273–7. doi:. PMID 12147369.
- ↑ Liu H, Bravata DM, Olkin I, Friedlander A, Liu V, Roberts B, Bendavid E, Saynina O, Salpeter SR, Garber AM, Hoffman AR (May 2008). «Systematic review: the effects of growth hormone on athletic performance». Ann. Intern. Med. 148 (10): pp. 747–58. PMID 18347346.
- ↑ Randall T (17-03-2008). «Athletes Don't Benefit From Human Growth Hormone, Study Finds». Bloomberg. Consultado el 28-08-2011.
- ↑ Gaffney G (17-03-2008). «Steroid Nation: Review from Stanford says HGH no benefit as PED». Steroid Nation. Consultado el 28-08-2011.
- ↑ «Center for Veterinary Medicine Master» (pdf). www.fda.gov (06-04-2011). Consultado el 28-08-2011.
- ↑ «Growth Promoters in Animal Production» (pdf) (2006). Consultado el 28-08-2011.
- ↑ Maybe, Nancy G (1984). «Direct expression of human growth in Escherichia coli with the lipoprotein promoter». En Arthur P. Bollon. Recombinant DNA products: insulin, interferon, and growth hormone. Boca Raton: CRC Press. ISBN 0-8493-5542-7.
- ↑ Hintz, Raymond L. (1984). «Biological actions in humans of recombinant DNA synthesized human growth hormone». En Arthur P. Bollon. Recombinant DNA products: insulin, interferon, and growth hormone. Boca Raton: CRC Press. ISBN 0-8493-5542-7.
- ↑ «Genentech and Alkermes Announce Decision to Discontinue Commercialization of Nutropin Depot». Press Release. Business Wire (01-06-2004). Consultado el 28-08-2011.
- ↑ Singleton ER (04-06-2010). «Atlas Operations, Inc.». Warning Letter. U.S. Food and Drug Administration. Consultado el 28-08-2011.
Bibliografía
- MARTIN CUENCA, E. "Fundamentos de fisiología" Ed. Thomson (2006)
- RHOADES, R. A.; TANNER, G. A. "Fisiología médica" eD. Elsevier (1997)
Categorías:- Genes del cromosoma 17
- Hormonas peptídicas
- Hipófisis
- Código ATC H
- Hormonas hipofisiarias
Wikimedia foundation. 2010.