- Eicosanoide
-
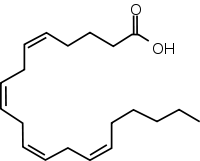 Estructura química del ácido araquidónico, del cual derivan la gran mayoría de los eicosanoides.
Estructura química del ácido araquidónico, del cual derivan la gran mayoría de los eicosanoides.
Los eicosanoides o icosanoides[1] [2] son un grupo de moléculas de carácter lipídico originadas de la oxigenación de los ácidos grasos esenciales de 20 carbonos tipo omega-3 y omega-6. Cumplen amplias funciones como mediadores para el sistema nervioso central, los eventos de la inflamación y de la respuesta inmune tanto en vertebrados como en invertebrados.
Todos los eicosanoides son moléculas de 20 átomos de carbono y están agrupados en prostaglandinas, tromboxanos, leucotrienos, y ciertos hidroxiácidos precursores de los leucotrienos. Constituyen las moléculas involucradas en las redes de comunicación celular más complejas del organismo animal, incluyendo el ser humano.
Contenido
Historia
El término fue usado por primera vez por E. J. Corey y sus colaboradores en 1980, para nombrar un grupo de moléculas que procedían de cierto ácido graso compuesto por 20 carbonos.[3]
Cincuenta años antes, en 1930, el ginecólogo Raphael Kurzrok y el farmacólogo Charles Leib describieron la prostaglandina como un componente del semen (prosta de próstata) capaz de hacer contraer la musculatura lisa del útero. Entre 1929 y 1932, Burr y Burr demostraron que la eliminación de las grasas de la dieta de un animal genera deficiencias nutritivas, de donde describieron por primera vez el concepto de ácidos grasos esenciales.[4]
En 1935, Ulf von Euler identificó la prostaglandina. En 1964 Sune Karl Bergström y Bengt Samuelsson enlazaron las observaciones previas al demostrar que los eicosanoides derivaban del ácido araquidónico, considerado recientemente uno de los ácidos grasos esenciales[5] y componente de los fosfolípidos de la membrana plasmática.
En 1971, Vane encontró que sustancias como la aspirina ejercen su efecto a través del bloqueo de la síntesis de prostaglandinas, una de las agrupaciones de los eicosanoides.[6] Von Euler recibió el Premio Nobel en medicina en 1970, y posteriormente en 1982 lo recibieron Samuelsson, Vane y Bergström. E. J. Corey ganó el Premio Nobel de Química en 1990, principalmente por la síntesis de las prostaglandinas.
Bioquímica
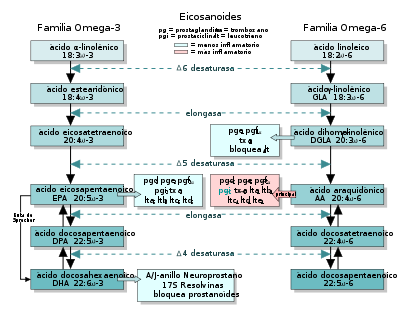
De cada tipo de molécula agrupada dentro de los eicosanoides derivan dos o tres moléculas producidas, bien sea a raíz de un ácido graso esencial tipo ω-3 o del tipo ω-6. Se notará que las actividades metabólicas de los derivados de eicosanoides dependen de su estructura bioquímica y, por lo general, su estructura individual explica los efectos orgánicos del omega-3 y del omega-6.[7] [8] [9] [10]
Los eicosanoides son ácidos carboxílicos, virtud del cual obtienen sus propiedades metabólicas.[11] Aquellos derivados del omega-3 (ω-3) por lo general tienen peculiaridades antiinflamatorias, no tanto así los derivados del omega-6 (ω-6). De los eicosanoides, las prostaglandinas y los tromboxanos incluyen anillos saturados y heterocíclicos, mientras que los leucotrienos y los hidroxiácidos son lineales (abiertas de principio a fin de su cadena). Todos ellos derivan del ácido araquidónico (AA), y son ácidos grasos esenciales. Además del ácido araquidónico, otros ácidos grasos esenciales también pueden servir como precursores en la formación de estas moléculas, por ejemplo, el ácido linoleico y el ácido linolénico.
- Las prostaglandinas tienen 20 átomos de carbono, un grupo de ácido carboxílico y un anillo de cinco carbonos como parte de su estructura. Todas las prostaglandindas tienen un ciclopentano (un anillo de cinco (penta) carbonos), excepto la prostaglandina I2, que tiene un anillo adicional.
- Los tromboxanos son moléculas cíclicas (heterociclo) bien sea de 6 carbonos ó de 5 carbonos con 1 oxígeno, formando éste último un pequeño anillo de oxano—un anillo que contiene 5 átomos de carbono y un átomo de oxígeno. Tienen estructuras parecidas a las prostaglandinas y siguen la misma nomenclatura. Constan de un anillo y dos colas. Se encontraron primeramente en los trombocitos (plaquetas), de allí su nombre tromboxano.
- Los leucotrienos son moléculas lineales. Se identificaron en leucocitos y por ello se les conoce como leucotrieno. Aunque tienen cuatro enlaces dobles, inicialmente se pensaba que tenían 3 dobles enlaces conjugados (de allí trieno). Su producción en el cuerpo forma parte de una compleja secuencia metabólica que incluye la producción de histamina.
- El ácido linoleico (un ω-6) tiene la última insaturación a seis posiciones del final y producen el ácido araquidónico y pueden formar directamente la prostaglandina G2 (pro-inflamatorios). La palabra linoleico viene de la planta lino y -oleico relacionado con los aceites oleicos.
- El ácido linolénico (un ω-3) tiene la última insaturación a 3 posiciones del final, impidiéndoles producir ácido araquidónico por sí mismos. Son capaces de producir la prostaglandina G3 (lo que les otorga propiedades antiinflamatorias). Debido a la carencia de las enzimas que sintetizan este ácido graso esencial, los seres humanos no producen ácido linolénico y deben obtenerlo a través de la dieta. El peso de evidencias científicas sugiere que consumir una dieta rica en ácido linolénico (2-3 gramos cada día) es útil en la prevención de cardiopatías isquémicas.[12]
Nomenclatura
Un "eicosanoide" (eicosa-, griego: veinte; véase icosaedro) es el término general[13] para los moléculas oxigenadas derivadas de ácidos grasos esenciales todas de 20 carbonos:
- Ácido eicosapentaenoico (EPA, por sus siglas en inglés), es un ω-3 con cinco enlaces dobles;
- Ácido araquidónico (AA), es un ω-6 con cuatro enlaces doble;
- Ácido dihomo-gamma-linolénico (DGLA), es un ω-6 con tres enlaces dobles
El uso de la palabra se limita a los leucotrienos (LT) y a tres tipos de prostanoides: prostaglandinas (PG), prostaciclinas (PGI) y tromboxanos (TX). En algunos casos se usa el término para incluir otros productos, entre ellos lipoxinas, lipoxenos, lipoxinoides, variantes del ácido epoxieicosatrienoico (EET) y hepoxilinas.[14]
Un eicosanoide cualquiera se denota con una abreviación de cuatro caracteres, compuesta de:
- Caracteres 1 y 2. Una abreviación de dos letras del nombre del compuesto (tromboxano = TX).[15]
- Carácter 3. Una letra que denote secuencia y no necesariamente relacionada con el nombre del compuesto.[16]
- Carácter 4. Un subíndice que representa el número de enlaces dobles en la molécula.
Por ejemplo:
- - Derivados prostanoides del EPA tienen tres dobles enlaces, por ejemplo: PGG3, PGH3, PGI3, TXA3, mientras que los leucotrienos tienen cinco: LTB5.
- - Los prostanoides derivados del AA tienen dos enlaces dobles: PGG2, PGH2, PGI2, TXA2 mientras que los leucotrienos tienen cuatro: LTB4.
La PGF2a/b se refiere a la orientación de los hidroxilos (-OH) en comparación con el anillo: a = los hidroxilos están orientados hacia el mismo lado, y b = hacia lados opuestos.
Biosíntesis
La oxidación catalítica de ácidos grasos es un requisito para la producción de eicosanoides, y tiene lugar gracias a dos familias de enzimas:
- Ciclooxigenasa (COX) de tipos 1, 2 y 3; conducen a la formación de prostanoides.[17]
- Lipooxigenasa, en sus variadas formas. La 5-lipoxigenasa (5-LO) genera leucotrienos.[18]
Vías de los eicosanoides Eicosanoides 'clásicos' Otras moléculas derivadas de ácidos grasos esenciales de 20 carbonos Los ácidos grasos tienen
dos destinos eicosanoides:- Vía de la 5-lipoxigenasa:
- Vía de la ciclooxigenasa
("prostanoides"):- Prostaglandinas
- Prostaciclina
- Tromboxanos
Otras rutas oxidativas generan
productos similares:- Vía de la 12-lipoxigenasa:
- Hepoxilinas
- Lipoxinas
- Vía del citocromo P450:
- Ácido epoxieicosatrienoico
- Peroxidación por radicales libres:
- Isoprostanos
- Isofuranos
Está también la adición por
etanolamina o glicerol:- Anandamida y otros
endocanabinoides
El primer paso de la biosíntesis de eicosanoides ocurre cuando la célula es activada por lesión celular, citocinas, factores de crecimiento u otros estímulos. La vía es tan compleja que el estímulo puede ser un eicosanoide mismo producido por una célula vecina. Esos estímulos provocan la liberación de fosfolipasa a nivel de la membrana celular el cual viaja a la membrana del núcleo celular. Una vez allí, este biocatalizador, dependiendo del isotipo, produce la hidrólisis (1) del enlace fosfodiéster de los fosfolípidos (por la enzima fosfolipasa A2) o (2) del diacilglicerol (por la fosfolipasa C). Esas interacciones libera de la membrana un ácido graso esencial de 20 carbonos. La hidrólisis de los fosfolípidos parece ser la reacción limitante, y por ende, la más regulada en la formación de eicosanoides.
Aquellas células que no posean en su citoplasma la enzima fosfolipasa A2, por lo general son células deprovisatas de síntesis de eicosanoides. Es una fosfolipasa específica para ciertos fosfolípidos que contengan bien sea AA, EPA o DGLA en una posición determinada de la molécula. La fosfolipasa citoplasmática es la liberadora de precusores del factor activador de plaquetas (PAF).[19]
Peroxidación lipídica y otras especies reactivas de oxígeno
En el paso siguiente, los ácidos grasos libres de la membrana son oxigenados por cualquier vía reactiva del oxígeno. Las vías específicas de eicosanoides son las de la lipoxigenasa, de la ciclooxigenasa y del O2 (véase tabla arriba). A pesar de que el ácido graso es simétrico, los eicosanoides resultantes de él son compuestos quirales, pues el proceso de oxidación ocurre con alta estereoespecificidad.
La oxidación lipídica es una reacción potencialmente peligrosa para la célula, en particular si ocurre cerca del núcleo. Sin embargo, la célula está provista de mecanismos que evitan las oxidaciones innecesarias. La ciclooxigenasa (COX), las lipoxigenasas y las fosfolipasas son enzimas fuertemente reguladas; por ejemplo, existen al menos ocho proteínas activadas para coordinar la producción de leucotrienos, algunas en múltiples conformaciones.[10]
La oxidación tanto por COX como por lipoxigenasa libera especies reactivas de oxígeno (ROS), de hecho los productos iniciales de los eicosanoides son también altamente peroxidantes. El leucotrieno LTA2 puede formar aductos con tejido nuclear. Otras reacciones con lipoxigenasas generan lesión celular: ciertos modelos con múridos implican a la 15-lipoxigenasa en la patogénesis de la aterosclerosis.[20] [21]
La oxidación en la producción de eicosanoides está compartimentada, limitando aún más la posibilidad de lesión por peróxidos reactivos. Las enzimas biosintéticas de eicosanoides (como la glutatión S-transferasa, la epóxido hidrolasa y transportadores proteicos) pertenecen a familias cuyas funciones están involucradas en la desintoxicación celular. Esto sugiere que las señales eicosanoides pudieron haber evolucionado de la desintoxicación de los amenazantes ROS.
De algún modo la célula encuentra ventajoso generar hidroperóxidos lipídicos cerca de su núcleo. En ese estado, las PG y los LT pueden enviar señales intracelulares o bien regular la transcripción genética de ADN, mientras que LTB4 es el ligando del receptor nuclear llamado "receptores activados por la proliferación de los peroxisomas" (PPAR).[8]
Biosíntesis de prostanoides
- Varios fármacos reducen la inflamación bloqueando la síntesis de prostanoides; por ejemplo, la ciclooxigenasa, la aspirina y otros AINES.
 Compuesto inicial: (Prostaglandina H2) Compuestos derivados Reacción mediada por enzima Numerales = Compuestos prostanoides:
Compuesto inicial: (Prostaglandina H2) Compuestos derivados Reacción mediada por enzima Numerales = Compuestos prostanoides:
1 Prostaglandina H2; 2 Prostaglandina E2; 3 Prostaglandina F2; 4 Prostaglandina A2; 5 Prostaglandina B2; 6 Prostaglandina D2; 7 Prostaglandina J2; 8 Prostaglandina I2 (prostaciclina); 9 6-ceto-prostaglandina Fα; 10 Tromboxano A2.
Texto = Enzimas:
A. Prostaglandina E sintasa; B. Prostaglandina E 9-cetorreductasa; C. Prostaglandina D sintasa; D. Prostaciclina sintasa; E. Tromboxano-A sintasa.Los precursores prostanoides son ácidos grasos esenciales que provienen de la dieta y son incorporados a los fosfolípidos, normalmente en la posición 2. Los corticoides son inhibidores de las fosfolipasas que inhiben la síntesis de prostaglandinas. También producidos por el ácido araquidónico, éste se puede incorporar por dos vías: la vía cíclica, por la que se sintetizan las prostaglandinas y los tromboxanos, y la vía lineal, productora de hidroxiácidos y leucotrienos.
Las prostaglandinas son, entre otros, agentes proinflamatorios y anticoagulantes. Las células endoteliales, por ejemplo, producen prostaciclina (PGI2), que tiene un efecto vasodilatador y de inhibición de la agregación plaquetaria.
El ácido araquidónico se transforma en PGH2 mediante la prostaglandina sintasa, que tiene 2 actividades enzimáticas diferentes: ciclooxigenasa e hidroperoxidasa.
La ciclooxigenasa (COX) cataliza la conversión de ácidos grasos libres a prostanoides en un proceso que consta de dos pasos (Nota: el ácido araquidónico (AA) es la fuente más abundante de eicosanoides de modo que las siguientes reacciones son descritas en términos de AA, aunque el ácido eicosapentaenoico (EPA) y DGLA producen sus metabolitos de manera similar):
La primera etapa de la reacción es catalizada por la actividad ciclooxigenasa que rompe el ciclopentano, se añaden dos moléculas de O2 molecular como enlaces peróxidos y las cargas negativas hacen que se corra el electrón formando el ciclopentano, un anillo de 5 carbonos cercano a la mitad de la cadena del ácido graso. Ello forma la inestable prostaglandina G (PGG) de vida corta. Luego, la gran inestabilidad de la PGG hace que rápidamente se transforme, catalizado por la actividad hidroperoxidasa, a PGH2 porque se rompe el grupo peróxido liberando un oxígeno, formando así la PGH.
La PGH2 da lugar a todas las prostaglandinas y a todos los tromboxanos (TX). Todas tienen un anillo único en su centro, por lo que difieren levemente en estructura. Los compuestos de la PGH y sus metabolitos tienen un anillo de 5 carbonos enlazados por dos oxígenos. Las prostaciclinas resultantes tienen su anillo articulado a otro anillo oxigenado. El anillo de los tromboxanos se convierte en uno de 6 con un oxígeno y los leucotrienos no tienen anillos. La especificidad de la síntesis de PG es que cada tejido sólo tiene una enzima y sólo puede sintetizar una única PG.
Biosíntesis de leucotrienos
La enzima 5-lipoxigenasa (5-LO) usa una proteína activadora llamada FLAP para introducir un oxígeno en el ácido araquidónico y así convierte éste en el hidroxiácido HPETE (ácido hidroperoxieicosatetraenoico), que espontáneamente se reduce, generando los HETE (ácidos 5-hidroxieicosatetraenoicos). La misma enzima 5-LO actúa de nuevo, esta vez sobre el 5-HETE para convertirlo en leucotrieno A4 (LTA4), que puede ser convertido a LTB4 por la enzima A4 epóxido-hidrolasa, si la necesidad celular así lo requiere. Varias células usan la enzima leucotrieno C4 sintetasa para conjugar el glutatión con LTA4 y producir LTC4, que es transportado al exterior de la célula, donde el grupo funcional del ácido glutámico es extraído para generar LTD4. Ciertas peptidasas cortan el leucotrieno LTD4 para formar LTE4. Entre las células que usan esta enzima están los macrófagos alveolares, los eosinófilos, y los mastocitos. Los leucotrienos LTE4, LTD4 y LTC4 contienen cisteína por lo que se los llama colectivamente leucotrienos cisteinilos.[22]
== La seriecar algunos de los efectos beneficiosos de la mayor ingesta de ω-3." Kevin Fritsche[23] }}
El ácido araquidónico (AA; 20:4 ω-6) está al tope de la cascada del ácido araquidónico, la cual está compuesta por más de veinte tipos de señales eicosanoideas, que controlan una amplia gama de funciones celulares, específicamente las que regulan la inflamación, la inmunidad y el sistema nervioso central.[9]
En la respuesta inflamatoria, dos grupos adicionales de ácidos grasos esenciales de la dieta forman cascadas similares y compiten con la cascada del ácido araquidónico. El ácido eicosapentaenoico (EPA, 20:5 ω-3) provee la cascada competidora más importante. El ácido dihomogammalinolénico (DGLA 20:3 ω-6) provee una tercera y menos prominente cascada. Estas dos cascadas alternativas menguan los efectos inflamatorios del ácido araquidónico y sus productos. La baja ingesta en la dieta de estos ácido grasos esenciales menos inflamatorios, especialmente los ω-3, se ha vinculado con diversas enfermedades proinflamatorias, y probablemente algunas enfermedades mentales.
Tanto el Instituto Nacional de Salud como la Biblioteca Nacional de Medicina de los Estados Unidos afirman que existen evidencias científicas sugiriendo que el incremento de ω-3 en la dieta mejora los casos con hipertrigliceridemia, la prevención secundaria de enfermedad cardiocascular e hipertensión. La administración de ω-3 a ω-6 de 3:1 a perros con heridas cutáneas sanan sus lesiones con considerablemente menos síntomas y signos inflamatorios, como edema.[24]
Otras evidencias sugieren que el incrementar el ω-3 dietético previene enfermedades cardiovasculares, artritis reumatoide y protege contra la toxicidad por ciclosporina en pacientes con trasplante de órgano. Se ha notado igualmente ciertas evidencias preliminares que demuestran que los ω-3 pueden mejorar los síntomas de ciertos desórdenes psiquiátricos.[25]
Además de la influencia sobre los eicosanoides, las grasas poliinsaturadas modulan la respuesta inmunitaria por medio de tres mecanismos adicionales: (a) alteran la composición y función de la membrana, incluyendo la composición de la capa bilipídica; (b) disrumpen la biosíntesis de citocinas; y (c) activan directamente la transcripción genética.[23] De todas estas, la acción de las grasas poliinsaturadas sobre los eicosanoides es la más explorada.
Mecanismos de acción del ω-3
Los eicosanoides provenientes del ácido araquidónico generalmente promueven la aparición de inflamación. Aquellos del EPA y el ácido γ-linolénico (vía DGLA), por su parte, son por lo general menos inflamatorias, o mejor dicho inactivas e incluso anti-inlfamatorias.
El ω-3 y el DGLA se oponen a los efectos inflamatorios de los eicosanoides del ácido araquidónico (AA) en tres maneras a lo largo de las vías metabólicas:
- Desplazamiento. El ω-3 de la dieta disminuye las concentraciones de AA en los tejidos y, por ende, disminuyen los procesos inflamatorios. Estudios con animales muestran que el incremento de ω-3 en la dieta resulta en una disminución de AA en el cerebro y otros tejidos.[26] El ácido linolénico (18:3 ω-3) contribuye en ello, al desplazar el ácido linoleico (18:2 ω-6) de las enzimas elongasa y desaturasa que producen al AA. EPA, otro ω-3, inhibe la liberación de AA de la membrana celular por medio de fosfolipasa A2.[27] Es posible que otros mecanismos que involucran el transporte de EPA tengan una función importante aquí. Pero también se cumple lo contrario: la elevación del ácido linoleico en la dieta disminuye la conversión en el cuerpo de ácido α-linolénico en EPA. Sin embargo, el efecto no es tan potenciado; la desnaturasa tiene una mayor afinidad por el ácido α-linolénico que por el ácido linoleico.[28]
- Inhibición competitiva: DGLA y EPA compiten con el AA por el acceso a las enzimas sintetizadoras ciclooxigenasa (COX) y lipoxigenasa. De modo que la presencia de DGLA y de EPA en los tejidos disminuye la producción de eicosanoides derivados del AA. Por ejemplo, el ácido gamma-linolénico (GLA) en la dieta incrementa el DGLA en los tejidos y disminuye al tromboxano TXB2 (un derivado del AA).[29] [30] De igual manera, EPA inhibe la producción de las PG de serie 2 y de los TX (también derivados del AA).[31] A pesar de que DGLA no forma LT, un derivado del DGLA bloquea la transformación de AA a LT.[32] EPA disminuye la formación de leucotrienos cisteinilos derivados del AA (LTC de serie 4, LTD y LTE) formando en vez la menos activa serie 5.[33] Otra grasa ω-3, el ácido docosahexaenoico (DHA) (22:5 ω-3), no produce eicosanoides pero inhibe la formación de prostanoides derivados del AA.[34]
- Oposición. Ciertos eicosanoides derivados del DGLA y EPA se oponen a sus homólogos derivados del AA. Por ejemplo, DGLA produce PGE1, que poderosamente contrarresta al descendiente araquidónico PGE2.[35] También produce leucotrieno LTB5 que impide la acción de los LTB4 derivados del AA.[36]
Los peces y otros animales marinos que consumen fitoplancton, tienen un elevado contenido en ω-3, de modo que una dieta rica en pescado tiende a disminuir los problemas inflamatorios, cardiovasculares, etc. Los esquimales de Groenlandia, por ejemplo, a pesar de su alto consumo de grasas y baja ingesta de carbohidratos, presentan baja incidencia de alto colesterol, triglicéridos y lipoproteínas de baja densidad, y mayores valores de lipoproteínas de alta densidad. Sufren menos problemos cardíacos, y quienes tienen cardiopatías manifiestan un bajo índice de mortalidad (apróx. 10%), en comparación con la población norteamericana (50%). Entre los esquimales también se nota menor incidencia de asma, diabetes, psoriasis y enfermedades autoinmunes, entre otras.[37]
Función y farmacología
La cantidad de estas grasas presentes en la dieta individual afecta las funciones controladas por el tipo específico de eicosanoide, teniendo repercusiones sobre el riesgo de enfermedades cardíacas, la concentración de triglicéridos en sangre, la presión arterial, y la artritis. Ciertas drogas como la aspirina y otros antiinflamatorios (no esteroideos) ejercen su acción por medio de una regulación negativa sobre (disminuyendo) la síntesis de ciertos eicosanoides, en particular los pro-inflamatorios. Los eicosanoides se hallan en una gran variedad de microorganismos, plantas y animales. En los humanos, son hormonas locales liberadas por la mayoría de las células, actuando sobre la misma célula u otras cercanas para ser luego rápidamente inactivadas. Son potentes en concentraciones nanomolares, no son almacenadas dentro de las células y su biosíntesis es activada solo según sea requerida.
Acciones metabólicas de ciertos prostanoides y leucotrienos†[19] PGD2 Promueven el sueño TXA2 Estimulación de agregación
plaquetaria; vasoconstricciónPGE2 Contracción de musculatura lisa;
inducen dolor, calor, fiebre;
broncoconstricción15d-PGJ2 Diferenciación de Adipocitos PGF2α Contracciones uterinas LTB4 Quimiotaxis de leucocitos PGI2 Inhibición de la agregación plaquetaria;
vasodilatación; implantación del embriónLT-Cisteinlos Anafilaxis; contracción de la
musculatura lisa bronquial.†Los eicosanoides aquí señalados son derivados del AA; los derivados del EPA generalmente tienen actividad más débil Los eicosanoides tienen una vida media de segundos a minutos. Los antioxidantes dietéticos inhiben la producción de algunos eicosanoides inflamatorios (por ej: Resveratrol en contra del tromboxano y algunos leucotrienos).[38] Las prostaglandinas (PG) se utilizan para provocar partos, contracción muscular lisa (PGE2). Si se consigue una dieta con la relación adecuada, se consigue estimular la producción de prostaglandinas E1, las cuales tienen propiedades antiinflamatorias, en oposición a las acciones utero-contráctiles de la PGE2.[39] La mayoría de los receptores de eicosanoides están acoplados a la superfamilia de las proteínas G.
Complejidad metabólica
"Es argumentable que la cascada del ácido araquidónico sea la más elaborada de los sistemas de comunicación celular que un neurobiólogo tenga que enfrentar."Daniele Piomelli[9]Receptores: Cada eicosanoide tienen un receptor específico Leukotrienos: - CysLT1 (leucotrieno cisteinilo
receptor tipo 1) - CysLT2 (leucotrieno cisteinilo
receptor tipo 2) - BLT1 (Receptor leukotrieno B4)
Prostanoides: - PGD2: DP-(PGD2)
- PGE2:
- Receptor EP1-(PGE2)
- Receptor EP2-(PGE2)
- Receptor EP3-(PGE2)
- Receptor EP4-(PGE2)
- PGF2α: FP-(PGF2α)
- PGI2 (prostaciclina): IP-(PGI2)
- TXA2 (tromboxano): TP-(TXA2)
Las vías de señalización de los eicosanoides son complejas, por lo que resulta difícil caracterizar la acción de un eicosanoide en particular. Por ejemplo la PGE2 se une a cuatro receptores, nombrados EP1–4. Cada uno es codificado por un gen individual, y algunos existen en varias formas (isoformas). Cada receptor EP a su vez se parea con una proteína G. El receptor EP2, EP4 y una de las isofromas del EP3 tienden a acoplarse con la variedad Gs. El hacerlo incrementa el AMP cíclico y resulta antiinflamatorio. El receptor EP1 y otra isoforma del EP3 se unen a la proteína Gq, incrementando el calcio intracelular y ello es pro-inflamatorio. Finalmente, otra isoforma del receptor EP3se une a la proteína Gi, disminuyendo el cAMP y al mismo tiempo incrementando el calcio intracelular. Muchas células del sistema inmune expresan múltiples receptores que se unen a estos aparentemente opuestos sistemas.[40]
Se presume que la PGE3 derivado del EPA tiene un efecto algo distinto en este sistema, pero no se conocen bien las características de ello.
Papel en la inflamación
Por mucho tiempo se han conocido los signos cardinales de la inflamación, tales como: calor, dolor, rubor (enrojecimiento) y tumor (hinchazón). Los eicosanoides están involucrados en cada uno de esos signos.
- Enrojecimiento—La picadura de insecto inicia la respuesta clásica de la inflamación. Ciertos vasoconstrictores de corta duración, como la PGI2 y el TXA2—se liberan rápidamente después de la lesión. haciendo que, inicialmente, el sitio pueda tornarse momentariamente pálido. Luego TXA2 actúa como mediador de la liberación de vasodilatadores como PGE2 y LTB4. Los vasos sanguíneos se llenan y la lesión se enrojece (rubor).
- Inflamación—El LTB4 hace que los vasos sanguíneos se vuelvan más permeables. El plasma sanguíneo sale a los tejidos conjuntivos, hinchándolos. El proceso también libera citocinas proinflamatorias.
- Dolor—Las citocinas incrementan la actividad de COX-2. Ello eleva los niveles de PGE2, haciendo a los nervios del dolor mas sensitivos.
- Calor—Las PG2 son compuestos proinflamatorios, son producidos como respuesta de defensa del organismo frente a una infección: incrementan la temperatura del organismo, provocan vasodilatación. La PGE2 es un potente agente pirético. La aspirina es un inhibidor de las prostaglandinas e inhibe la síntesis de PG inflamatorias. La aspirina y los AINES (paracetamol, butiprofeno, ibuprofeno) bloquean la acción de COX y detienen la síntesis de prostanoides, limitando así la fiebre o el calor de la inflamación localizada.Farmacia: Eicosanoide, análogos eicosanoideos y receptores antagonistas usados como medicamentos Medicamento Tipo Uso o circunstancia médica Alprostadil PGI1 Disfunción eréctil, preservar
un conducto arterioso
presente del fetoBeraprost análogo PGI1 Hipertensión pulmonar, evitar
lesión por reperfusiónBimatoprost análogo PG Glaucoma, hipertensión ocular Carboprost análogo PG Partos inducidos,
aborto inducidoDinoprostone PGE2 Partos inducidos Iloprost PGI2 analog Hipertensión arteria pulmonar Latanoprost análogo PG Glaucoma, hipertensión ocular Misoprostol análogo PGE1 Úlcera del esómago, Parto
inducidos, aborto inducidoMontelukast receptor antagonista del LT Asma, alergias Travoprost análogo PG Glaucoma, hipertensión ocular Treprostinil análogo PGI Hipertensión pulmonar U46619 Longer lived
análogo TXPara investigaciones Zafirlukast receptor antagonista del LT Asma Acción de los prostanoides
Los prostanoides juegan un papel principal como mediadores de los síntomas locales de la inflamación: vasoconstricción o vasodilatación, coagulación, dolor y fiebre. La inhibición de la ciclooxigenasa, especialmente la forma inducible COX-2, es el fundamento de los antiinflamatorios no-esteroideos (AINES), como la aspirina. COX-2 es responsable del dolor y la inflamación, mientras que el COX-1 es el responsable por las acciones agregadoras de plaquetas. Los prostanoides activan receptores hormonales en el núcleo, de la familia esteroidea/tiroidea, como el ya mencionado PPARγ, al influenciar directamente la transcripción genética.[41] Cuando se daña un vaso sanguíneo, disminuye la producción de PGI2, aumentan los TXA2 y se produce la agregación plaquetaria (coagulación).
Los tromboxanos (TX) son vasoconstrictores e incrementan la agregación de las plaquetas. Las plaquetas producen específicamente TXA2. La aspirina inactiva la enzima de las plaquetas, acción que es irreversible. Por eso, el efecto total de la aspirina es anticoagulante porque afecta más a las plaquetas ya que no tienen núcleo y no pueden fabricar nuevas enzimas. El efecto que tiene a dosis bajas es beneficioso en las personas con riesgo alto de trombosis o infartos. La aspirina está contraindicado a personas con úlcera de estómago porque además de anticoagulantes, también intervienen en una segregación más elevada de HCl de las células estomacales. Se está empezando a asociar a las prostaglandinas a ciertas patologías inflamatorias, como la PGE2 con la porfiria cutánea tarda.[42]
Acción de los leucotrienos
Los leucotrienos juegan un papel importante en la inflamación. Existe un rol neuroendocrino para el LTC4 en la secreción de la hormona luteinizante.[43] El LTB4 causa adhesión y quimiotaxis de leucocitos y estimula la agregación, liberación enzimática y generación de superóxido en neutrófilos.[44] El bloqueo de los receptores para los leucotrienos pueden participar en el tratamiento de enfermedades inflamatorias tales como el asma (montelukast y zafirlukast), psoriasis y artritis reumatoide.
Ciertas sustancias anafiláticas se incluyen entre los leucotrienos cisteinilos. Estos tienen un claro rol en las condiciones fisiopatológicas tales como asma, rinitis alérgica y otras alergias nasales, y se les ha implicado en la aterosclerosis y enfermedades inflamatorias del tracto gastrointestinal.[45]
Los leucotrienos son potentes broncoconstrictores, incrementan la permeabilidad vascular y vénulas post-capilares y estimulan la secreción de moco. Por lo general son liberados por el tejido pulmonar en sujetos asmáticos expuestos a alérgenos específicos y juegan un papel fisiopatológico en reacciones inmediatas de hipersensibilidad.[44]
Junto con la PGD, los leucotrienos funcionan en las células efectoras inmunes, en la presentación de antígeno y la activación de inmunocitos, osteocitos y fibrosis.[46]
Véase también
- Aceite de hígado de bacalao
- Analgésico
- Inhibidores selectivos de la COX-2
- Lista de ácidos grasos omega 3
- Pescado azul
Referencias
- ↑ Webster's Online Dictionary. «Specialty Definition: EICOSANOID» (en inglés). Consultado el 23 de marzo de 2008.
- ↑ Aaron J. Marcus, Lenore B. Safier, Harris L. Ullman, M. Johan Broekman, Naziba Islam, Thomas D. Oglesby, Robert R. Gorman. 12S,20-dihydroxyicosatetraenoic Acid: A New Icosanoid Synthesized by Neutrophils from 12S-hydroxyicosatetraenoic Acid Produced by Thrombin- or Collagen-Stimulated Platelets (en inglés). Proceedings of the National Academy of Sciences of the United States of America, Vol. 81, No. 3, [Part 1: Biological Sciences] (Feb. 1, 1984), pp. 903-907. Último acceso 23 de marzo, 2008.
- ↑ David W. Stanley, et al. Eicosanóides na Biologia de Insetos. Neotrop. Entomol. v.31 n.3 Londrina jul./sep. 2002. [1]
- ↑ Burr, G.O. and Burr, M.M. (1930). «On the nature and role of the fatty acids essential in nutrition». J. Biol. Chem. 86 (587). http://www.jbc.org/cgi/reprint/97/1/1.pdf.
- ↑ Bergström, S., Danielsson, H. and Samuelsson, B. (1964). «The enzymatic formation of prostaglandin E2 from arachidonic acid». Biochim. Biophys. Acta 90 (207). PMID 14201168.
- ↑ Vane, J. R. (23 June 1971). «Inhibition of prostaglandin synthesis as a mechanism of action for aspirin-like drugs». Nature New Biol. 231 (25): pp. 232-5. PMID 5284360.
- ↑ DeCaterina, R and Basta, G (June, 2001). «n-3 Fatty acids and the inflammatory response – biological background». European Heart Journal Supplements 3, Suppl D: pp. D42-D49. http://eurheartjsupp.oxfordjournals.org/cgi/reprint/3/suppl_D/D42.pdf.
- ↑ a b Funk, Colin D. (30 November 2001). «Prostaglandins and Leukotrienes: Advances in Eicosanoid Biology». Science 294 (5548): pp. 1871 - 1875. doi:. http://www.sciencemag.org/cgi/content/full/294/5548/1871.
- ↑ a b c Piomelli, Daniele (2000). «Arachidonic Acid». Neuropsychopharmacology: The Fifth Generation of Progress. http://www.acnp.org/g4/GN401000059/Default.htm.
- ↑ a b Soberman, Roy J. and Christmas, Peter (2003). «The organization and consequences of eicosanoid signaling». J. Clin. Invest 111: pp. 1107-1113. doi:. http://www.jci.org/cgi/content/full/111/8/1107.
- ↑ Consejo General de Colegios Oficiales de Farmacéuticos. [2]
- ↑ Mozaffarian D (2005). «Does alpha-linolenic acid intake reduce the risk of coronary heart disease? A review of the evidence». Alternative therapies in health and medicine 11 (3): pp. 24–30; quiz 31, 79. PMID 15945135.
- ↑ Beare-Rogers (2001). «IUPAC Lexicon of Lipid Nutrition». Consultado el June 1 de 2006.
- ↑ Universidad Nacional del Nordeste - Facultad de Medicina. [3]
- ↑ Con la excepción de Prostaciclina, la cual fue previamente clasificada con tres letras: PGI.
- ↑ Grosso modo, la tercera letra indica el orden en que los eicosanoides fueron descritos por primera vez en la literatura. Para ver diagramas de las PG [A–H] véase Cyberlipid Center. «Prostanoids». Consultado el 05-02-2007.
- ↑ Warner, Timothy D. and Mitchell, Jane A. (October 8, 2002). «Cyclooxygenase-3 (COX-3): Filling in the gaps toward a COX continuum?». PNAS 99 (21): pp. 13371-13373. doi:. http://www.pnas.org/cgi/content/extract/99/21/13371.
- ↑ Fundación Clínica Valle del Lili - Unidad Cardiovascular. [4]
- ↑ a b University of Kansas Medical Center (2004). «Eicosanoids and Inflammation». Consultado el 05-01-2007.
- ↑ Cyrus, Tillmann (June 1999). «Disruption of the 12/15-lipoxygenase gene diminishes atherosclerosis in apo E–deficient mice». J Clin Invest 103 (11): pp. 1597-1604n. http://www.jci.org/cgi/content/abstract/103/11/1597.
- ↑ Schewe T. (2002 Mar-Apr). «15-lipoxygenase-1: a prooxidant enzyme». Biol Chem. 383 (3-4). http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Retrieve&db=PubMed&list_uids=12033428.
- ↑ Revista Electrónica de PortalesMedicos.com - Asma Bronquial y su terapéutica. [5]
- ↑ a b Fritsche, Kevin (August 2006). «Fatty Acids as Modulators of the Immune Response». Annual Review of Nutrition 26: pp. 45-73. doi:. http://arjournals.annualreviews.org/doi/abs/10.1146/annurev.nutr.25.050304.092610?journalCode=nutr.
- ↑ Scardino, Swaim, Sartin, Hoffman, Oglivie, Hanson, Coolman, Davenport (1999). The effects of omega-3 fatty acid diet enrichment on wound healing. Veterinary Dermatology 10 (4), 283–290. [6]
- ↑ National Institute of Health (August 1, 2005). «Omega-3 fatty acids, fish oil, alpha-linolenic acid». Consultado el March 26 de 2006.
- ↑ Medical Study News (25-May-2005). «Brain fatty acid levels linked to depression». Consultado el February 10 de 2006.
- Estos autores citan a su vez a Pnina Green, Iris Gispan-Herman and Gal Yadid (June 2005). Increased arachidonic acid concentration in the brain of Flinders Sensitive Line rats, an animal model of depression. http://www.jlr.org/cgi/content/abstract/46/6/1093.
- ↑ KP Su, SY Huang, CC Chiu, WW Shen (2003). Omega-3 fatty acids in major depressive disorder. A preliminary double-blind, placebo-controlled .... http://nutri.tmu.edu.tw/slide/b2.pdf.
- ↑ Phinney, SD, RS Odin, SB Johnson and RT Holman (1990). «Reduced arachidonate in serum phospholipids and cholesteryl esters associated with vegetarian diets in humans». American Journal of Clinical Nutrition 51: pp. 385-392. http://intl.ajcn.org/cgi/content/abstract/51/3/385.
- "El ácido araquidónico de la dieta enriquece su colección circulante en humanos, sin embargo, la isoforma 20:5n-3 tiende a no responder igual a la restricción dietética."
- ↑ Guivernau M, Meza N, Barja P, Roman O. (Nov 1994). Clinical and experimental study on the long-term effect of dietary gamma-linolenic acid on plasma lipids, platelet aggregation, thromboxane formation, and prostacyclin production.. PMID 7846101.
- GLA disminuye los triglicéridos, LDL, incrementa el HDL y disminuye el TXB2 así como otros marcadores inflamatorios. Artículo de revisión; estudios en humanos y ratas.
- ↑ Karlstad MD, DeMichele SJ, Leathem WD, Peterson MB. (Nov 1993). Effect of intravenous lipid emulsions enriched with gamma-linolenic acid on plasma n-6 fatty acids and prostaglandin biosynthesis after burn and endotoxin injury in rats. PMID 8222692.
- Suplemento intravenoso (IV) con ácido gamma-linolénico incrementó el GLA sérico pero no incrementó el porcentaje plasmático de ácido araquidónico (estudio en ratas), disminuyó TXB2.
- ↑ Calder, Philip C. (September 2004). «n-3 Fatty Acids and Inflammation – New Twists in an Old Tale». Consultado el February 8 de 2006.
- Invited review article, PUFA Newsletter.
- ↑ Belch, Jill JF and Alexander Hill (January 2000). Evening primrose oil and borage oil in rheumatologic conditions. http://www.ajcn.org/cgi/content/full/71/1/352S.
- "El mismo DGLA no puede ser convertido en leucotrienos (LT), pero puede producir un derivado 15-hidroxilado que bloquea la transforamción de ácido araquidónico en LT. El incrementar el consumo de DGLA puede permitir que el DGLA actúe como inhibidor competitivo de las PG de serie 2 y los leucotrienos de serie 4, suprimiendo así la inflamación."
- ↑ Lee TH, Mencia-Huerta JM, Shih C, Corey EJ, Lewis RA, Austen KF (Dec 1984). «Effects of exogenous arachidonic, eicosapentaenoic, and docosahexaenoic acids on the generation of 5-lipoxygenase pathway products by ionophore-activated human neutrophils.». : J Clin Invest 74 (6): pp. 1922-33.. PMID 6096400. http://www.pubmedcentral.nih.gov/picrender.fcgi?artid=425378&blobtype=pdf.
- ↑ Corey E, Shih C, Cashman J (1983). «Docosahexaenoic acid is a strong inhibitor of prostaglandin but not leukotriene biosynthesis». Proc Natl Acad Sci U S A 80 (12): pp. 3581-4. PMID 6304720. http://www.pnas.org/cgi/reprint/80/12/3581.pdf.
- ↑ Fan, Yang-Yi and Robert S. Chapkin (9 September 1998). «Importance of Dietary gamma -Linolenic Acid in Human Health and Nutrition». Journal of Nutrition 128 (9): pp. 1411-1414. http://jn.nutrition.org/cgi/content/full/128/9/1411.
- "El GLA dietético incrementa el contenido de su producto elongasa, el ácido dihomo-gamma linolénico (DGLA), en las membranas celulares sin cambios concomitantes en el ácido araquidónico (AA). Subsecuentemente, al ser estimulado, el DGLA puede ser convertido por células inflamatorias en ácido 15-(S)-hidroxi-8,11,13-eicosatrienoico y prostaglandina E1. Ello tiene su importancia por razón de que estos compuestos poseen propiedades tanto anti-inflamatorias como antiproliferativas."
- ↑ Prescott S (1984). «The effect of eicosapentaenoic acid on leukotriene B production by human neutrophils». J Biol Chem 259 (12): pp. 7615-21. PMID 6330066. http://www.jbc.org/cgi/reprint/259/12/7615.pdf.
- ↑ IMeN - Instituto de Metabolismo e Nutrição, São Paulo. [7]
- ↑ Pace-Asciak CR, Hahn S, Diamandis EP, Soleas G, Goldberg DM. (1995 Mar 31). «The red wine phenolics trans-resveratrol and quercetin block human platelet aggregation and eicosanoid synthesis: implications for protection against coronary heart disease.». Clin Chim Acta. 235 (2): pp. 207-19. PMID 7554275.
- ↑ Revista Consumer (español). Alimentación para aliviar los dolores menstruales. Último acceso 4 de marzo, 2008.
- ↑ Tilley S, Coffman T, Koller B (2001). «Mixed messages: modulation of inflammation and immune responses by prostaglandins and thromboxanes». J Clin Invest 108 (1): pp. 15-23. PMID 11435451. http://www.jci.org/cgi/reprint/108/1/15.
- ↑ Bos C, Richel D, Ritsema T, Peppelenbosch M, Versteeg H (2004). «Prostanoids and prostanoid receptors in signal transduction». Int J Biochem Cell Biol 36 (7): pp. 1187-205. PMID 15109566.
- ↑ VIEIRA, Fátima Mendonça Jorge and MARTINS, José Eduardo Costa. Porphyria cutanea tarda. An. Bras. Dermatol. [online]. 2006, vol. 81, no. 6 [citado marzo de 2008], pp. 573-584. Disponible en la World Wide Web: [8]. ISSN 0365-0596. doi: 10.1590/S0365-05962006000600010
- ↑ Samuelsson, SE Dahlen, JA Lindgren, CA Rouzer, and CN Serhan (09-04 1987). «Leukotrienes and lipoxins: structures, biosynthesis, and biological effects». Science 237 (4819): pp. 1171-1176. doi:. http://www.sciencemag.org/cgi/content/abstract/237/4819/1171.
- ↑ a b Samuelsson B (May 1983). «Leukotrienes: mediators of immediate hypersensitivity reactions and inflammation». Science 220 (4597): pp. 568 - 575. doi:. http://www.sciencemag.org/cgi/content/abstract/sci;220/4597/568.
- ↑ Capra V (2004). «Molecular and functional aspects of human cysteinyl leukotriene receptors». Pharmacol Res 50 (1): pp. 1-11. PMID 15082024.
- ↑ Boyce J (2005). «Eicosanoid mediators of mast cells: receptors, regulation of synthesis, and pathobiologic implications». Chem Immunol Allergy 87: pp. 59-79. PMID 16107763.
Enlaces externos
- En MedlinePlus puede encontrar más información sobre Eicosanoide
- En Medline hay más información sobre Eicosanoide (en inglés)
- Universidad Nacional del Nordeste — Farmacología de los Eicosanoides.
Categoría:- Eicosanoides
Wikimedia foundation. 2010.