- Elemento químico
-
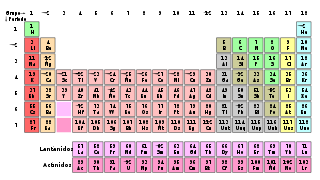 Tabla periódica de los elementos químicos.
Tabla periódica de los elementos químicos.
Un elemento químico es un tipo de materia, constituida por átomos de la misma clase. En su forma más simple posee un número determinado de protones en su núcleo, haciéndolo pertenecer a una categoría única clasificada con el número atómico, aun cuando este pueda ostentar distintas masas atómicas. Es un átomo con características físicas únicas, aquella sustancia que no puede ser descompuesta mediante una reacción química, en otras más simples. No existen dos átomos de un mismo elemento con características distintas y, en el caso de que estos posean masa distinta, pertenecen al mismo elemento pero en lo que se conoce como uno de sus isótopos. También es importante diferenciar entre un «elemento químico» de una sustancia simple.
El ozono (O3) y el oxígeno (O2) son dos sustancias simples, cada una de ellas con propiedades diferentes. Y el elemento químico que forma estas dos sustancias simples es el oxígeno (O). Otro ejemplo es el elemento químico carbono, que se presenta en la naturaleza como grafito o como diamante (estados alotrópicos).
Algunos elementos se han encontrado en la naturaleza, formando parte de sustancias simples o de compuestos químicos. Otros han sido creados artificialmente en los aceleradores de partículas o en reactores atómicos. Estos últimos son inestables y sólo existen durante milésimas de segundo. A lo largo de la historia del universo se han ido generando la variedad de elementos químicos a partir de nucleosíntesis en varios procesos, fundamentalmente debidos a estrellas.
Contenido
Elementos químicos en la tabla periódica de los elementos
Los elementos químicos se encuentran clasificados en la tabla periódica de los elementos. A continuación se detallan los elementos conocidos, ordenados por su número atómico.
Número atómico Nombre Símbolo Periodo,
GrupoMasa atómica
(g/Mol)Densidad
(g/cm³)
a 20°CFusión
(°C)Ebullición
(°C)Año de su
descubrimientoDescubridor 1 Hidrógeno H 1, 1 1.00794(7)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 0.084 g/l -259.1 -252.69 1766 Cavendish 2 Helio He 1, 18 4.002602(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 0.17 g/l -272.2 -268.9 1895 Ramsay y Cleve 3 Litio Li 2, 1 6.941(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (5)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 0.53 180.5 1317 1817 Arfwedson 4 Berilio Be 2, 2 9.012182(3) 1.85 1278 2970 1797 Vauquelin 5 Boro B 2, 13 10.811(7)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2.46 2300 2550 1808 Davy y Gay-Lussac 6 Carbono C 2, 14 12.0107(8)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 3.51 3550 4827 Prehistoria Desconocido 7 Nitrógeno N 2, 15 14.0067(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1.17 g/l -209.9 -195.8 1772 Rutherford 8 Oxígeno O 2, 16 15.9994(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1.33 g/l -218.4 -182.9 1774 Priestly y Scheele 9 Flúor F 2, 17 18.9984032(5) 1.58 g/l -219.6 -188.1 1886 Moissan 10 Neón Ne 2, 18 20.1797(6)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 0.84 g/l -248.7 -246.1 1898 Ramsay y Travers 11 Sodio Na 3, 1 22.98976928(2) 0.97 97.8 892 1807 Davy 12 Magnesio Mg 3, 2 24.3050(6) 1.74 648.8 1107 1755 Black 13 Aluminio Al 3, 13 26.9815386(8) 2.70 660.5 2467 1825 Oersted 14 Silicio Si 3, 14 28.0855(3)(4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2.33 1410 2355 1824 Berzelius 15 Fósforo P 3, 15 30.973762(2) 1.82 44 (P4) 280 (P4) 1669 Brand 16 Azufre S 3, 16 32.065(5)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2.06 113 444.7 Prehistoria Desconocido 17 Cloro Cl 3, 17 35.453(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2.95 g/l -34.6 -101 1774 Scheele 18 Argón Ar 3, 18 39.948(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1.66 g/l -189.4 -185.9 1894 Ramsay y Rayleigh 19 Potasio K 4, 1 39.0983(1) 0.86 63.7 774 1807 Davy 20 Calcio Ca 4, 2 40.078(4)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1.54 839 1487 1808 Davy 21 Escandio Sc 4, 3 44.955912(6) 2.99 1539 2832 1879 Nilson 22 Titanio Ti 4, 4 47.867(1) 4.51 1660 3260 1791 Gregor y Klaproth 23 Vanadio V 4, 5 50.9415(1) 6.09 1890 3380 1801 del Río 24 Cromo Cr 4, 6 51.9961(6) 7.14 1857 2482 1797 Vauquelin 25 Manganeso Mn 4, 7 54.938045(5) 7.44 1244 2097 1774 Gahn 26 Hierro Fe 4, 8 55.845(2) 7.87 1535 2750 Prehistoria Desconocido 27 Cobalto Co 4, 9 58.933195(5) 8.89 1495 2870 1735 Brandt 28 Níquel Ni 4, 10 58.6934(2) 8.91 1453 2732 1751 Cronstedt 29 Cobre Cu 4, 11 63.546(3)(4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 8.92 1083.5 2595 Prehistoria Desconocido 30 Zinc Zn 4, 12 65.409(4) 7.14 419.6 907 Prehistoria Desconocido 31 Galio Ga 4, 13 69.723(1) 5.91 29.8 2403 1875 Lecoq de Boisbaudran 32 Germanio Ge 4, 14 72.64(1) 5.32 937.4 2830 1886 Winkler 33 Arsénico As 4, 15 74.92160(2) 5.72 613 613
(sublimación)ca. 1250 Albertus Magnus 34 Selenio Se 4, 16 78.96(3)(4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 4.82 217 685 1817 Berzelius 35 Bromo Br 4, 17 79.904(1) 3.14 -7.3 58.8 1826 Balard 36 Kriptón Kr 4, 18 83.798(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 3.48 g/l -156.6 -152.3 1898 Ramsay y Travers 37 Rubidio Rb 5, 1 85.4678(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1.53 39 688 1861 Bunsen y Kirchhoff 38 Estroncio Sr 5, 2 87.62(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2.63 769 1384 1790 Crawford 39 Itrio Y 5, 3 88.90585(2) 4.47 1523 3337 1794 Gadolin 40 Circonio Zr 5, 4 91.224(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.51 1852 4377 1789 Klaproth 41 Niobio Nb 5, 5 92.906 38(2) 8.58 2468 4927 1801 Hatchett 42 Molibdeno Mo 5, 6 95.94(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 10.28 2617 5560 1778 Scheele 43 Tecnecio Tc 5, 7 [98.9063](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 11.49 2172 5030 1937 Perrier y Segrè 44 Rutenio Ru 5, 8 101.07(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 12.45 2310 3900 1844 Klaus 45 Rodio Rh 5, 9 102.90550(2) 12.41 1966 3727 1803 Wollaston 46 Paladio Pd 5, 10 106.42(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 12.02 1552 3140 1803 Wollaston 47 Plata Ag 5, 11 107.8682(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 10.49 961.9 2212 Prehistoria Desconocido 48 Cadmio Cd 5, 12 112.411(8)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 8.64 321 765 1817 Strohmeyer y Hermann 49 Indio In 5, 13 114.818(3) 7.31 156.2 2080 1863 Reich y Richter 50 Estaño Sn 5, 14 118.710(7)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 7.29 232 2270 Prehistoria Desconocido 51 Antimonio Sb 5, 15 121.760(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.69 630.7 1750 Prehistoria Desconocido 52 Telurio Te 5, 16 127.60(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.25 449.6 990 1782 von Reichenstein 53 Yodo I 5, 17 126.90447(3) 4.94 113.5 184.4 1811 Courtois 54 Xenón Xe 5, 18 131.293(6)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 4.49 g/l -111.9 -107 1898 Ramsay y Travers 55 Cesio Cs 6, 1 132.9054519(2) 1.90 28.4 690 1860 Kirchhoff y Bunsen 56 Bario Ba 6, 2 137.327(7) 3.65 725 1640 1808 Davy 57 Lantano La 6 138.90547(7)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.16 920 3454 1839 Mosander 58 Cerio Ce 6 140.116(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.77 798 3257 1803 W. Hisinger y Berzelius 59 Praseodimio Pr 6 140.90765(2) 6.48 931 3212 1895 von Welsbach 60 Neodimio Nd 6 144.242(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 7.00 1010 3127 1895 von Welsbach 61 Prometio Pm 6 [146.9151](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 7.22 1080 2730 1945 Marinsky y Glendenin 62 Samario Sm 6 150.36(2)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 7.54 1072 1778 1879 Lecoq de Boisbaudran 63 Europio Eu 6 151.964(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 5.25 822 1597 1901 Demarçay 64 Gadolinio Gd 6 157.25(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 7.89 1311 3233 1880 de Marignac 65 Terbio Tb 6 158.92535(2) 8.25 1360 3041 1843 Mosander 66 Disprosio Dy 6 162.500(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 8.56 1409 2335 1886 Lecoq de Boisbaudran 67 Holmio Ho 6 164.93032(2) 8.78 1470 2720 1878 Soret 68 Erbio Er 6 167.259(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 9.05 1522 2510 1842 Mosander 69 Tulio Tm 6 168.93421(2) 9.32 1545 1727 1879 Cleve 70 Iterbio Yb 6 173.04(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 6.97 824 1193 1878 de Marignac 71 Lutecio Lu 6, 3 174.967(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 9.84 1656 3315 1907 Urbain 72 Hafnio Hf 6, 4 178.49(2) 13.31 2150 5400 1923 Coster y de Hevesy 73 Tantalio Ta 6, 5 180.9479(1) 16.68 2996 5425 1802 Ekeberg 74 Wolframio W 6, 6 183.84(1) 19.26 3407 5927 1783 Elhuyar 75 Renio Re 6, 7 186.207(1) 21.03 3180 5627 1925 Noddack, Tacke y Berg 76 Osmio Os 6, 8 190.23(3)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 22.61 3045 5027 1803 Tennant 77 Iridio Ir 6, 9 192.217(3) 22.65 2410 4130 1803 Tennant 78 Platino Pt 6, 10 195.084(9) 21.45 1772 3827 1557 Scaliger 79 Oro Au 6, 11 196.966569(4) 19.32 1064.4 2940 Prehistoria Desconocido 80 Mercurio Hg 6, 12 200.59(2) 13.55 -38.9 356.6 Prehistoria Desconocido 81 Talio Tl 6, 13 204.3833(2) 11.85 303.6 1457 1861 Crookes 82 Plomo Pb 6, 14 207.2(1)(2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (4)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 11.34 327.5 1740 Prehistoria Desconocido 83 Bismuto Bi 6, 15 208.98040(1) 9.80 271.4 1560 1540 Geoffroy 84 Polonio Po 6, 16 [208.9824](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 9.20 254 962 1898 Marie y Pierre Curie 85 Astato At 6, 17 [209.9871](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 302 337 1940 Corson y MacKenzie 86 Radón Rn 6, 18 [222.0176](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 9.23 g/l -71 -61.8 1900 Dorn 87 Francio Fr 7, 1 [223.0197](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 27 677 1939 Perey 88 Radio Ra 7, 2 [226.0254](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 5.50 700 1140 1898 Marie y Pierre Curie 89 Actinio Ac 7 [227.0278](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 10.07 1047 3197 1899 Debierne 90 Torio Th 7 232.03806(2)(1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 11.72 1750 4787 1829 Berzelius 91 Protactinio Pa 7 231.03588(2)(1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 15.37 1554 4030 1917 Soddy, Cranston y Hahn 92 Uranio U 7 238.02891(3)(1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (2)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. (3)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 18.97 1132.4 3818 1789 Klaproth 93 Neptunio Np 7 [237.0482](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 20.48 640 3902 1940 McMillan y Abelson 94 Plutonio Pu 7 [244.0642](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 19.74 641 3327 1940 Seaborg 95 Americio Am 7 [243.0614](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 13.67 994 2607 1944 Seaborg 96 Curio Cm 7 [247.0703](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 13.51 1340 1944 Seaborg 97 Berkelio Bk 7 [247.0703](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 13.25 986 1949 Seaborg 98 Californio Cf 7 [251.0796](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 15.1 900 1950 Seaborg 99 Einsteinio Es 7 [252.0829](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 860 1952 Seaborg 100 Fermio Fm 7 [257.0951](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1952 Seaborg 101 Mendelevio Md 7 [258.0986](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1955 Seaborg 102 Nobelio No 7 [259.1009](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1958 Seaborg 103 Lawrencio Lr 7, 3 [260.1053](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1961 Ghiorso 104 Rutherfordio Uhc 7, 4 [261.1087](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1964/69 Flerov 105 Dubnio Unp 7, 5 [262.1138](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1967/70 Flerov 106 Seaborgio Unh 7, 6 [263.1182](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1974 Flerov 107 Bohrio Bh 7, 7 [262.1229](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1976 Oganessian 108 Hassio Hs 7, 8 [265](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1984 GSI (*) 109 Meitnerio Mt 7, 9 [266](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1982 GSI 110 Darmstadtio Ds 7, 10 [269](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1994 GSI 111 Roentgenio Rg 7, 11 [272](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1994 GSI 112 Copernicio Cn 7, 12 [285](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1996 GSI 113 Ununtrio Uut 7, 13 [284](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2004 JINR (*), LLNL (*) 114 Ununquadio Uuq 7, 14 [289](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 1999 JINR 115 Ununpentio Uup 7, 15 [288](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2004 JINR, LLNL 116 Ununhexio Uuh 7, 16 [290](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2006 JINR, LLNL(**) 117 Ununseptio Uus 7, 17 (1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2009-2010 JINR 118 Ununoctio Uuo 7, 18 [294](1)La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. 2006 JINR, LLNL(**) (**)El descubrimiento del elemento 118 por un equipo del Lawrence Berkeley National Laboratory en 1999 fue más tarde revocado porque no fue posible repetir tal experimento.
[1] Anulación de LBNL por el descubrimiento de 1999.
[2] Experimento de JINR/LLNL (2005)
Acrónimos incluidos en la tabla
- GSI, Gesellschaft für Schwerionenforschung (Sociedad para la Investigación de Iones Pesados), Wixhausen, Darmstadt, Alemania
- JINR, Joint Institute for Nuclear Research (Instituto Unido para la Investigación Nuclear), Dubna, Moskvá Oblast, Rusia
- LLNL, Lawrence Livermore National Laboratory (Laboratorio Nacional Lawrence Livermore) Livermore, California, Estados Unidos
- LBNL, Lawrence Berkeley National Laboratory (Laboratorio Nacional Lawrence de Berkeley) Berkeley, California, Estados Unidos
Notas sobre la tabla
- El H2O es el químico complejo de las sustancias químicas
- Nota 1: La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. El elemento no tiene un nucleoide estable, y su valor entre corchetes, (por ejemplo, [209]), indica el número másico del isótopo con mayor duración de dicho elemento.
- Nota 2: La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. La composición isotópica de algunos elementos presentes en ciertos fragmentos geológicos puede variar de la facilitada en la tabla.
- Nota 3: La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. La composición isotópica puede variar en los materiales comerciales, por lo que el peso atómico puede variar del dado significativamente.
- Nota 4: La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. La composición isotópica de varios metales terrestres que necesitan una precisión mayor en su peso atómico no puede ser facilitada.
- Nota 5: La plantilla {{Fn}} está obsoleta, véase el nuevo sistema de referencias. El peso atómico del litio comercializado puede variar entre 6.939 y 6.996—en análisis futuros se tratará de especificar más el dato.
Procedencia de los nombres de elementos químicos
Los nombres de los elementos proceden de sus nombres en griego, latín, inglés o llevan el nombre de su descubridor o ciudad en que se descubrieron.
- Hidrógeno (H): del griego ‘engendrador de agua’.
- Helio (He): de la atmósfera del Sol (el dios griego Helios). Se descubrió por primera vez en el espectro de la corona solar durante un eclipse en 1868, aunque la mayoría de los científicos no lo aceptaron hasta que se aisló en la Tierra.
- Litio (Li): del griego lithos, roca de color rojo muy intenso a la flama
- Berilio (Be) de beriio, esmeralda de color verde
- Boro (B): del árabe buraq.
- Carbono (C): carbón.
- Nitrógeno (N): en griego nitrum, ‘engendrador de nitratos’
- Oxígeno (O): en griego ‘engendrador de óxidos’ (oxys).
- Flúor (F): del latín fluere.
- Neón (Ne): nuevo (del griego neos).
- Sodio (Na): Del latín sodanum (sosa). El símbolo Na viene del latín nátrium (nitrato de sodio)color amarillo a la flama
- Magnesio (Mg): de Magnesia, comarca de Tesalia (Grecia).
- Aluminio (Al): del latín alumen.
- Silicio (Si): del latín sílex, sílice.
- Fósforo (P) del griego phosphoros, ‘portador de luz’ (el fósforo emite luz en la oscuridad porque arde al combinarse lentamente con el oxígeno del aire).
- Azufre (S) del latín sulphurium.
- Cloro (Cl) del griego chloros (amarillo verdoso).
- Argón (Ar) del griego argos, ‘inactivo’ (debido a que los gases nobles son poco reactivos).
- Potasio (K): del inglés pot ashes (‘cenizas’), ya que las cenizas de algunas plantas son ricas en potasio. El símbolo K proviene del griego kalium.
- Calcio (Ca) del griego calx, ‘caliza’. La caliza está formada por Ca2CO3.
- Escandio (Sc) de Scandia (Escandinavia).
- Titanio (Ti): de los Titanes, los primeros hijos de la Tierra según la mitología griega.
- Vanadio (V): de diosa escandinava Vanadis.
- Cromo (Cr): del griego chroma, ‘color’.
- Manganeso (Mn): de magnes, magnético.
- Hierro (Fe): del latín ferrum.
- Cobalto (Co): según una versión, proviene del griego kobalos, ‘mina’. Otra versión dice que proviene del nombre de un espíritu maligno de la mitología alemana.
- Níquel (Ni): proviene del término sueco koppar nickel y del alemán kupfer nickel, ‘cobre del demonio Nick’ o cobre falso (metal que aparece en las minas de cobre, pero no es cobre).
- Cobre (Cu): de cuprum, nombre de la isla de Chipre.
- Zinc (Zn): del alemán zink, que significa origen oscuro.
- Galio (Ga): de Gallia (nombre romano de Francia).
- Germanio (Ge): de Germania (nombre romano de Alemania).
- Arsénico (As): arsenikon, oropimente (auripigmentum) amarillo.
- Selenio (Se):de Selene (nombre griego de la Luna).
- Bromo (Br): del griego bromos, ‘hedor’.
- Kriptón (Kr): del griego kryptos, ‘oculto, secreto’.
- Rubidio (Rb): del latín rubidius, rojo muy intenso (a la llama).
- Estroncio (Sr): de Strontian, ciudad de Escocia.
- Itrio (Y): de Ytterby, pueblo de Suecia.
- Circonio o Zirconio (Zr): del árabe zargun, ‘color dorado’.
- Niobio (Nb): de Níobe (hija de Tántalo).
- Molibdeno (Mo): de molybdos, ‘plomo’. (Al parecer, los primeros químicos lo confundieron con mena de plomo).
- Tecnecio (Tc): de technetos, ‘wikt:artificial’, porque fue uno de los primeros sintetizados.
- Rutenio (Ru): del latín Ruthenia (nombre romano de Rusia).
- Rodio (Rh): del griego rhodon, color rosado.
- Paladio (Pd): de la diosa griega de la sabiduría, Palas Atenea.
- Plata (Ag): del latín argéntum.
- Cadmio (Cd): del latín cadmia, nombre antiguo del carbonato de zinc. (Probablemente porque casi todo el cadmio industrial se obtiene como subproducto en el refinado de los minerales de zinc).
- Indio (In): debido al color índigo (añil) que se observa en su espectro.
- Estaño (Sn): del latín stannum.
- Telurio (Te): de tel-lus, ‘tierra’.
- Antimonio (Sb): del latín antimonium. El símbolo Sb, del latín stibium.
- Yodo (I): del griego iodes, violeta.
- Xenón (Xe): del griego xenon, ‘extranjero, extraño, raro’.
- Cesio (Cs): del latín caesius, color azul celeste.
- Bario (Ba): del griego barys, ‘pesado’.
- Lantano (La): del griego lanthanein, ‘yacer oculto’.
- Cerio (Ce): por el asteroide Ceres, descubierto dos años antes. El cerio metálico se encuentra principalmente en una aleación de hierro que se utiliza en las piedras de los encendedores.
- Praseodimio (Pr): de prasios, ‘verde’, y dídymos, ‘gemelo’.
- Neodimio (Nd): de neos-dýdimos, ‘nuevo gemelo (del lantano)’.
- Prometio (Pm): del dios griego Prometeo.
- Europio (Eu): de Europa.
- Gadolinio (Gd): del mineral gadolinita, del químico finlandés Gadolin.
- Terbio (Tb): de Ytterby, pueblo de Suecia.
- Disprosio (Dy): del griego dysprositos, de difícil acceso.
- Holmio (Ho): del latín Holmia (nombre romano de Estocolmo).
- Tulio (Tm): de Thule, nombre antiguo de Escandinavia.
- Lutecio (Lu): de Lutecia, antiguo nombre de París.
- Hafnio (Hf): de Hafnia, nombre latín de Copenhague.
- Tantalio (Ta): de Tántalo, un personaje de la mitología griega.
- Wolframio (W): del inglés wolfrahm; o Tungsteno, del sueco tung sten, ‘piedra pesada’.
- Renio (Re): del latín Rhenus (nombre romano del río Rin).
- Osmio (Os): del griego osme, olor (debido al fuerte olor del OsO4).
- Iridio (Ir): de arco iris.
- Platino (Pt): por su similitud a la plata (cuando en 1748 Antonio de Ulloa lo encontró en una expedición lo llamó "platina").
- Oro (Au): de aurum, aurora resplandeciente
- Mercurio (Hg): su nombre se debe al planeta del mismo nombre, pero su abreviatura es Hg porque Dioscórides lo llamaba «plata acuática» (en griego hydrárgyros, hydra: ‘agua’, gyros: ‘plata’).
- Talio (Tl): del griego thallos, tallo, vástago o retoño verde.
- Plomo (Pb): del latín plumbum.
- Bismuto (Bi): del alemán weisse masse, masa blanca.
- Polonio (Po): de Polonia, en honor al país de origen de Marie Curie, codescubridora del elemento, junto con su marido Pierre.
- Astato (At): del griego astatos, inestable.
- Radón (Rn): del inglés radium emanation (‘emanación radiactiva’).
- Francio (Fr): de Francia.
- Radio (Ra): del latín radius, ‘rayo’.
- Actinio (Ac): del griego aktinos, ‘destello o rayo’.
- Torio (Th): de Thor, dios de la guerra escandinavo.
- Protactinio (Pa): del griego protos (primer) y actinium.
- Uranio (U): del planeta Urano.
- Neptunio (Np): del planeta Neptuno.
- Plutonio (Pu): del planetoide Plutón.
- Americio (Am): de América.
- Curio (Cm): en honor de Pierre y Marie Curie.
- Berkelio (Bk): de Berkeley, donde se encuentra una importante universidad californiana.
- Californio (Cf): del estado estadounidense de California.
- Einstenio (Es): en honor de Albert Einstein.
- Fermio (Fm): en honor de Enrico Fermi.
- Mendelevio (Md): en honor al químico ruso Dmitri Ivánovich Mendeléiev, precursor de la actual tabla periódica.
- Nobelio (No): en honor de Alfred Nobel.
- Lawrencio (Lr): en honor de E. O. Lawrence.
- Rutherfordio (Rf):en honor a Ernest Rutherford, científico colaborador del modelo atómico y física nuclear.
- Dubnio (Db): en honor al Joint Institute for Nuclear Research, un centro de investigación ruso localizado en Dubna.
- Seaborgio (Sg): en honor a Glenn T. Seaborg.
- Bohrio (Bh): en honor a Niels Bohr.
- Hassio (Hs): se debe al estado alemán de Hesse en el que se encuentra el grupo de investigación alemán Gesellschaft für Schwerionenforschung (GSI).
- Meitnerio (Mt): en honor a Lise Meitner, matemática y física de origen austríaco y sueco.
- Darmstadtio (Ds): en honor al lugar donde fue descubierto, Darmstadt, en donde se localiza el GSI.
- Roentgenio (Rg): en honor a Wilhelm Conrad Roentgen, descubridor de los rayos X.
- Copernicio (Cn): en honor a Nicolás Copérnico, astrónomo polaco formulador de la teoría heliocéntrica.
A partir del número atómico 112, se nombra a los elementos con la nomenclatura temporal de la IUPAC, en la que a cada elemento le corresponde como nombre su número en latín.
Relación entre los elementos y la tabla periódica
La relación que tienen los elementos con la tabla periódica es que la tabla periódica contiene los elementos químicos en una forma de ordenada de acuerdo a su peso atómico, estableciendo más de 118 elementos conocidos. Algunos se han encontrado en la naturaleza, formando parte de sustancias simples o compuestos químicos. Otros han sido creados artificialmente en los aceleradores de partículas o en reactores atómicos. Estos últimos son inestables y sólo existen durante milésimas de segundo.
Conceptos básicos
- Elementos: sustancia que no puede ser descompuesta, mediante una reacción química, en otras más simples
- Tabla periódica de los elementos: Es la organización que, atendiendo a diversos criterios, distribuye los distintos elementos químicos conforme a ciertas características.
El descubrimiento de los elementos
Descubrimiento de los elementos químicos H He Li Be B C N O F Ne Na Mg Al Si P S Cl Ar K Ca Sc Ti V Cr Mn Fe Co Ni Cu Zn Ga Ge As Se Br Kr Rb Sr Y Zr Nb Mo Tc Ru Rh Pd Ag Cd In Sn Sb Te I Xe Cs Ba La Ce Pr Nd Pm Sm Eu Gd Tb Dy Ho Er Tm Yb Lu Hf Ta W Re Os Ir Pt Au Hg Tl Pb Bi Po At Rn Fr Ra Ac Th Pa U Np Pu Am Cm Bk Cf Es Fm Md No Lr Rf Db Sg Bh Hs Mt Ds Rg Cn Uut Uuq Uup Uuh Uus Uuo Antes de 1800 1800-1849 1850-1899 1900-1949 1950-2000 2001-presente Leyenda
- Antes de 1800 (34 elementos): descubrimientos durante y antes del Siglo de las Luces.
- 1800-1849 (+24 elementos): Revolución científica y Revolución industrial.
- 1850-1899 (+26 elementos): el periodo de las clasificaciones de los elementos recibió el impulso del análisis de los espectros: Boisbaudran, Bunsen, Crookes, Kirchhoff, y otros "cazadores de trazas en las líneas de emisión de los espectros".
- 1900-1949 (+13 elementos): impulso con la antigua teoría cuántica y la mecánica cuántica.
- 1950-2000 (+17 elementos): descubrimientos "después de la bomba atómica": elementos de números atómicos 98 y posteriores (colisionadores, técnicas de bombardeo).
- 2001-presente (+4 elementos): descubrimientos muy recientes, que no están confirmados.
Metales, no metales y metaloides
La primera clasificación de elementos conocida fue propuesta por Antoine Lavoisier, quien propuso que los elementos se clasificaran en metales, no metales y metaloides o metales de transición. Aunque muy práctico y todavía funcional en la tabla periódica moderna, fue rechazada debido a que había muchas diferencias en las propiedades físicas como químicas.
Metales
La mayor parte de los elementos metálicos exhibe el lustre brillante que asociamos a los metales. Los metales conducen el calor y la electricidad, son maleables (se pueden golpear para formar láminas delgadas) y dúctiles (se pueden estirar para formar alambres). Todos son sólidos a temperatura ambiente con excepción del mercurio (punto de fusión =-39 °C), que es un líquido. Dos metales se funden ligeramente arriba de la temperatura ambiente: el cesio a 28.4 °C y el galio a 29.8 °C. En el otro extremo, muchos metales se funden a temperaturas muy altas. Por ejemplo, el cromo se funde a 1900 °C.
Los metales tienden a tener energías de ionización bajas y por tanto se oxidan (pierden electrones) cuando sufren reacciones químicas. Los metales comunes tienen una relativa facilidad de oxidación. Muchos metales se oxidan con diversas sustancias comunes, incluidos O2 y los ácidos.
Se utilizan con fines estructurales, fabricación de recipientes, conducción del calor y la electricidad. Muchos de los iones metálicos cumplen funciones biológicas importantes: hierro, calcio, magnesio, sodio, potasio, cobre, manganeso, cinc, cobalto, molibdeno, cromo, estaño, vanadio, níquel,....
No metales
Los no metales varían mucho en su apariencia, no son lustrosos y por lo general son malos conductores del calor y la electricidad. Sus puntos de fusión son más bajos que los de los metales (aunque el diamante, una forma de carbono, se funde a 700 °C en condiciones normales de presión y temperatura). Varios no metales existen en condiciones ordinarias como moléculas diatómicas. En esta lista están incluidos cinco gases (H2, N2, O2, F2 y Cl2), un líquido (Br2) y un sólido volátil (I2). El resto de los no metales son sólidos que pueden ser duros como el diamante o blandos como el azufre. Al contrario de los metales, son muy frágiles y no pueden estirarse en hilos ni en láminas. Se encuentran en los tres estados de la materia a temperatura ambiente: son gases (como el oxígeno), líquidos (bromo) y sólidos (como el carbono). No tienen brillo metálico y no reflejan la luz. Muchos no metales se encuentran en todos los seres vivos: carbono, hidrógeno, oxígeno, nitrógeno, fósforo y azufre en cantidades importantes. Otros son oligoelementos: flúor, silicio, arsénico, yodo, cloro.
Comparación de los metales y no metales
Metales
- Tienen un lustre brillante; diversos colores, pero casi todos son plateados.
- Los sólidos son maleables y dúctiles
- Buenos conductores del calor y la electricidad
- Casi todos los óxidos metálicos son sólidos iónicos básicos.
- Tienden a formar cationes en solución acuosa.
- Las capas externas contienen pocos electrones habitualmente tres o menos.
- Es preciso advertir que estos caracteres aunque muy generales tienen algunas excepciones como por ejemplo , el manganeso que siendo metal forma ácidos
No Metales
- No tienen lustre; diversos colores.
- Los sólidos suelen ser quebradizos; algunos duros y otros blandos.
- Malos conductores del calor y la electricidad
- La mayor parte de los óxidos no metálicos son sustancias moleculares que forman soluciones ácidas
- Tienden a formar aniones u oxianiones en solución acuosa.
- Las capas externas contienen cuatro o más electrones*. Excepto hidrógeno y helio
Localización en la tabla periódica
Metales
Corresponde a los elementos situados a la izquierda y centro de la Tabla Periódica (Grupos 1 (excepto hidrógeno) al 12, y en los siguientes se sigue una línea quebrada que, aproximadamente, pasa por encima de Aluminio (Grupo 13), Germanio (Grupo 14), Antimonio (Grupo 15) y Polonio (Grupo 16) de forma que al descender aumenta en estos grupos el carácter metálico).
No Metales
Los no metales son los elementos situados a la derecha en la Tabla Periódica por encima de la línea quebrada de los grupos 14 a 17 y son tan solo 25 elementos. (Incluyendo el Hidrógeno). Colocados en orden creciente de número atómico, los elementos pueden agruparse, por el parecido de sus propiedades, en 18 familias o grupos (columnas verticales). Desde el punto de vista electrónico, los elementos de una familia poseen la misma configuración electrónica en la última capa, aunque difieren en el número de capas (periodos). Los grupos o familias son 18 y se corresponden con las columnas de la Tabla Periódica.
Elementos químicos y número atómico
Un elemento químico es una sustancia pura formada por átomos que tienen el mismo número atómico, es decir, el mismo número de protones. Cada elemento se distingue de los demás por sus propiedades características. Se denomina número atómico al número de protones que tiene el núcleo de un átomo. Este número es igual al número de electrones que el átomo neutro posee alrededor del núcleo.
Véase también
Referencias
- WebElements.com (los pesos atómicos de los elementos 110 a 116 fueron extraídos de esta fuente).
Enlaces externos
 Wikiquote alberga frases célebres de o sobre Elemento químico. Wikiquote
Wikiquote alberga frases célebres de o sobre Elemento químico. Wikiquote Wikimedia Commons alberga contenido multimedia sobre Elementos químicos. Commons
Wikimedia Commons alberga contenido multimedia sobre Elementos químicos. Commons
Categoría:- Elementos químicos
Wikimedia foundation. 2010.
